Trắc nghiệm Tổng hợp bài tập CO2 tác dụng với dung dịch kiềm - Hóa 12Đề bài
Câu 1 :
Hấp thụ hoàn toàn 3,36 lít (đktc) CO2 vào 500 ml dung dịch Ba(OH)2 nồng độ 0,2M thu được dung dịch X. Sau khi gạn bỏ kết tủa, khối lượng dung dịch X so với khối lượng dung dịch ban đầu
Câu 2 :
Sục 7,84 lít CO2 (đktc) vào 500 ml dung dịch hỗn hợp NaOH 0,4M và Ba(OH)2 0,2M, phần nước lọc sau khi phản ứng xảy ra hoàn toàn lần lượt cho tác dụng với các chất HNO3, NaCl, Ba(OH)2, NaHSO4, Mg(NO3)2. Số trường hợp có phản ứng hoá học xảy ra là
Câu 3 :
Hấp thụ hết 0,2 mol CO2 vào dung dịch chứa 0,025 mol NaOH và 0,1 mol Ba(OH)2, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là
Câu 4 :
Hấp thụ hoàn toàn 0,336 lít khí CO2 (đktc) vào 200 ml dung dịch gồm NaOH 0,1M và KOH 0,1M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan?
Câu 5 :
Sục từ từ V lít khí CO2 (đktc) từ từ vào 500 ml dung dịch hỗn hợp NaOH 0,6M; KOH 0,2M và Ba(OH)2 0,4M. Kết thúc phản ứng thu được 27,58 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị lớn nhất của V thỏa mãn điều kiện của bài toán là
Câu 6 :
Hấp thụ hoàn toàn 1,12 lít khí CO2 (đktc) vào 200 ml dung dịch KOH 1M thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là
Câu 7 :
Cho V lít CO2 (đktc) hấp thụ hết trong dung dịch chứa 0,2 mol Ba(OH)2; 0,05 mol NaOH và 0,05 mol KOH. Sau phản ứng hoàn toàn thu được kết tủa và dung dịch chứa 22,15 gam muối. Giá trị của V là
Câu 8 :
Sục khí CO2 từ từ cho đến dư vào 100 ml dung dịch hỗn hợp NaOH 0,6M và Ba(OH)2 0,5M thu được dung dịch A. Cô cạn dung dịch A rồi nhiệt phân đến khối lượng không đổi thu được m gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
Câu 9 :
Hấp thụ hoàn toàn 8,96 lít CO2 (đktc) vào V ml dung dịch chứa NaOH 2,75M và K2CO3 1M. Cô cạn dung dịch sau phản ứng ở nhiệt độ thường thu được 64,5 gam chất rắn khan gồm 4 muối. Giá trị của V là
Câu 10 :
Hấp thụ hoàn toàn V lít CO2 (đktc) vào bình đựng 200 ml dung dịch NaOH 1M và Na2CO3 0,5M. Cô cạn dung dịch sau phản ứng thu được 19,9 gam chất rắn khan. Giá trị của V là :
Câu 11 :
Dẫn từ từ 5,6 lít CO2 (đktc) vào 400 ml dung dịch chứa đồng thời các chất NaOH 0,3M; KOH 0,2M; Na2CO3 0,1875M; K2CO3 0,125M thu được dung dịch X. Thêm dung dịch CaCl2 dư vào dung dịch X, số gam kết tủa thu được là:
Câu 12 :
Khi sục từ từ đến dư CO2 vào dung dịch hỗn hợp gồm a mol NaOH và b mol Ca(OH)2, kết quả thí nghiệm được biểu diễn trên đồ thị sau 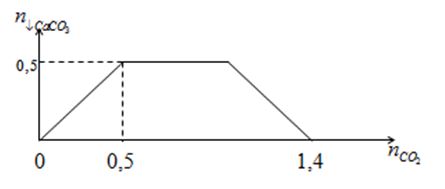 Tỉ lệ a : b là
Câu 13 :
Sục 13,44 lít CO2 (đktc) vào 200 ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M. Sau phản ứng thu được m1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với 200 ml dung dịch BaCl2 1,2M; KOH 1,5M thu được m2 gam kết tủa. Giá trị của m2 là:
Câu 14 :
Hấp thụ hoàn toàn 8,96 lít khí CO2 (đktc) vào dung dịch chứa x mol Ba(OH)2, x mol KOH, y mol NaOH. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 32,15 gam muối và 19,7 gam kết tủa. Bỏ qua sự thủy phân của các ion. Tỉ lệ x : y có thể là
Câu 15 :
Hấp thụ hoàn toàn V lít CO2 vào dung dịch Ca(OH)2 a M thì thu được m1 gam kết tủa. Nếu hấp thụ (V + 3,36) lít CO2 vào dung dịch Ca(OH)2 trên thì thu được m2 gam kết tủa. Nếu thêm (V + V1) lít CO2 vào dung dịch Ca(OH)2 đã cho thì thu được lượng kết tủa cực đại. Biết m1 : m2 = 3 : 2; m1 bằng 3/7 khối lượng kết tủa cực đại, các khí đều ở đktc. Giá trị của V1 là
Câu 16 :
Hấp thụ hết 8,96 lít CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 400 ml dung dịch X. Lấy 200 ml dung dịch X cho từ từ vào 600 ml dung dịch HCl 0,5M, thu được 5,376 lít khí (đktc). Mặt khác, 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư thu được 39,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của x là
Câu 17 :
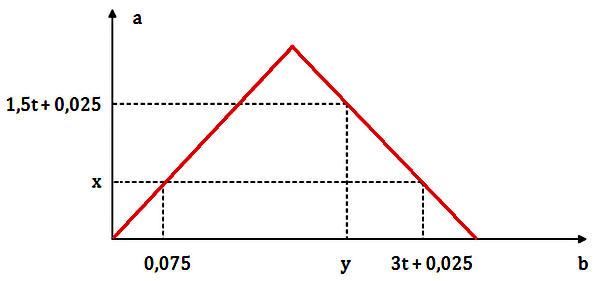
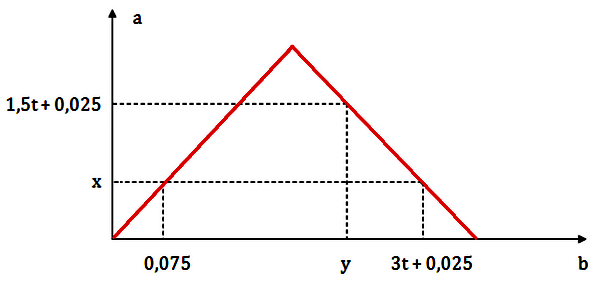
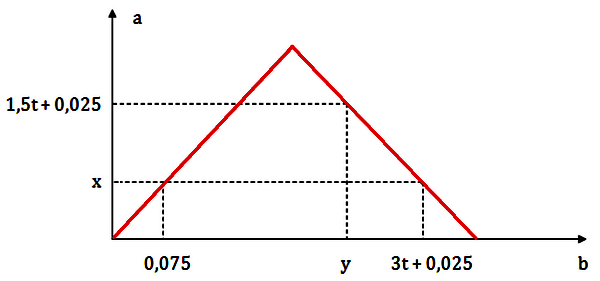
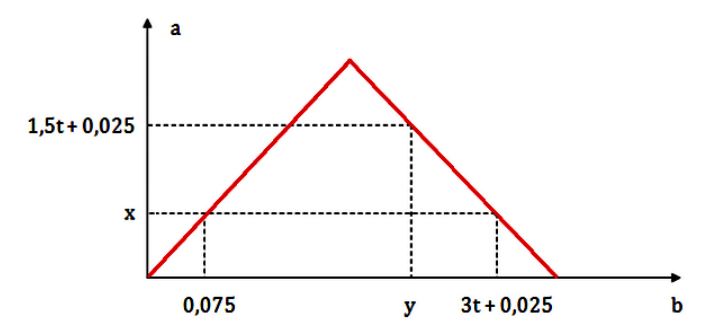
Dẫn từ từ đến dư khí CO2 vào dung dịch chứa 0,2 mol Ba(OH)2. Sự phụ thuộc của số mol kết tủa (a mol) vào số mol khí CO2 tham gia phản ứng (b mol) được biểu diễn như đồ thị sau:
Tỉ lệ y : x là
Câu 18 :
Hấp thụ hoàn toàn khí CO2 vào dung dịch Ca(OH)2, khối lượng kết tủa tạo và phụ thuộc vào thể tích khí CO2 (đktc) được biểu diễn như sau:
Biết Va, là thể tích CO2 cần dùng để có khối lượng kết tủa lớn nhất Va > V. Giá trị của Va là:
Câu 19 :
Hấp thụ hoàn toàn V lít khí CO2 (đktc) vào dung dịch Ca(OH)2 dư. Sau phản ứng thu được 10 gam kết tủa. Giá trị của V là
Câu 20 :
Hấp thụ hết V lít khí CO2 (đktc) vào dung dịch chứa 0,3 mol NaOH và 0,2 mol Ba(OH)2 thu được a gam kết tủa và dung dịch X. Để thu được lượng kết tủa lớn nhất cần cho thêm 4000 ml dung dịch Ba(OH)2 0,1M vào X. Giá trị của V là
Câu 21 :
Cho dung dịch A chứa Ca(OH)2 0,1 mol và NaOH 0,2 mol tác dụng với V lít CO2 (đktc). Giá trị lớn nhất của V để thu được kết tủa lớn nhất là
Câu 22 :
Sục CO2 vào dung dịch hỗn hợp gồm Ca(OH)2 và NaOH ta thu được kết quả sau
Giá trị của x là
Câu 23 :
Sục V lít khí CO2 (đktc) vào bình đựng 2 lít dung dịch Ca(OH)2 0,01M, thu được 1 g kết tủa. Xác định V.
Câu 24 :
Thổi từ từ khí CO2 đến dư vào dung dịch chứa 0,12 mol Ca(OH)2 . Sự phụ thuộc của số mol kết tủa thu được vào số mol CO2 phản ứng được biểu điễn theo đồ thị sau:
Mối quan hệ của a và b là:
Câu 25 :
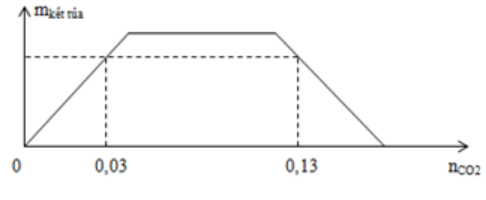
Sục khí CO2 vào V ml dung dịch hỗn hợp NaOH 0,2M và Ba(OH)2 0,1M. Đồ thị biểu diễn khối lượng kết tủa theo số mol CO2 phản ứng như sau:
Giá trị của V là:
Lời giải và đáp án
Câu 1 :
Hấp thụ hoàn toàn 3,36 lít (đktc) CO2 vào 500 ml dung dịch Ba(OH)2 nồng độ 0,2M thu được dung dịch X. Sau khi gạn bỏ kết tủa, khối lượng dung dịch X so với khối lượng dung dịch ban đầu
Đáp án : B Phương pháp giải :
+) nCO2 < nOH < 2.nCO2 => nCO3 = nOH – nCO2 +) ∆m = mCO2 – mBaCO3 Lời giải chi tiết :
nCO2 = 0,15 mol ; nBa(OH)2 = 0,1 mol => nOH = 0,2 mol Nhận thấy: nCO2 < nOH < 2.nCO2 => nCO3 = nOH – nCO2 = 0,05 mol Ta có: ∆m = mCO2 – mBaCO3 = 0,15.44 – 0,05.197 = -3,25 gam => khối lượng dung dịch giảm 3,25 gam
Câu 2 :
Sục 7,84 lít CO2 (đktc) vào 500 ml dung dịch hỗn hợp NaOH 0,4M và Ba(OH)2 0,2M, phần nước lọc sau khi phản ứng xảy ra hoàn toàn lần lượt cho tác dụng với các chất HNO3, NaCl, Ba(OH)2, NaHSO4, Mg(NO3)2. Số trường hợp có phản ứng hoá học xảy ra là
Đáp án : C Phương pháp giải :
- Sử dụng bảo toàn nguyên tố C: nCO2=nHCO−3+nCO2−3 - Sử dụng bảo toàn điện tích: nOH−=nHCO−3+2nCO2−3 Lời giải chi tiết :
nCO2 = 0,35 mol; nOH- = 0,4 mol => nCO2 < nOH- < 2.nCO2 => phản ứng sinh ra 2 muối HCO3- (x mol) và CO32- (y mol) - Sử dụng bảo toàn nguyên tố C: nCO2=nHCO−3+nCO2−3=>x+y=0,35 (1) - Sử dụng bảo toàn điện tích: nOH−=nHCO−3+2nCO2−3 => x + 2y = 0,4 (2) Từ (1) và (2) => x = 0,3; y = 0,05 mol Vì nBa2+>nCO2−3 => CO32- tạo hết thành kết tủa => dung dịch thu được gồm Na+, Ba2+, HCO3- => dung dịch sau phản ứng tác dụng được với HNO3, Ba(OH)2, NaHSO4 Chú ý
bẫy bài toán ở đây là số mol Ca2+ lớn hơn số mol CO32- nên dung dịch sau thí nghiệm 1 sẽ chỉ có muối axit
Câu 3 :
Hấp thụ hết 0,2 mol CO2 vào dung dịch chứa 0,025 mol NaOH và 0,1 mol Ba(OH)2, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là
Đáp án : D Phương pháp giải :
Xét nCO2 < nOH- < 2.nCO2 +) nCO3 = nOH – nCO2 = 0,025 mol Vì nCO3 < nBa2+ => nBaCO3 = nCO3 Lời giải chi tiết :
nOH- = 0,225 mol ; nCO2 = 0,2 mol => nCO2 < nOH- < 2.nCO2 => nCO3 = nOH – nCO2 = 0,025 mol Vì nCO3 < nBa2+ => nBaCO3 = nCO3 = 0,025 mol => mkết tủa = 4,925 gam
Câu 4 :
Hấp thụ hoàn toàn 0,336 lít khí CO2 (đktc) vào 200 ml dung dịch gồm NaOH 0,1M và KOH 0,1M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan?
Đáp án : C Phương pháp giải :
+) nOH > 2nCO2=> OH‑ dư => nCO3 = nCO2 = 0,015 mol Và nOH- dư = nOH- ban đầu – nOH- phản ứng = nOH- ban đầu -2nCO2−3 +) mrắn = mNa + mK + mCO3 + mOH dư Lời giải chi tiết :
nCO2 = 0,015 mol; nOH = nNaOH + nKOH = 0,04 mol > 2nCO2 => OH‑ dư => nCO3 = nCO2 = 0,015 mol Và nOH- dư = nOH- ban đầu – nOH- phản ứng = nOH- ban đầu -2nCO2−3= 0,01 mol => mrắn = mNa + mK + mCO3 + mOH dư = 2,31 gam
Câu 5 :
Sục từ từ V lít khí CO2 (đktc) từ từ vào 500 ml dung dịch hỗn hợp NaOH 0,6M; KOH 0,2M và Ba(OH)2 0,4M. Kết thúc phản ứng thu được 27,58 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị lớn nhất của V thỏa mãn điều kiện của bài toán là
Đáp án : A Phương pháp giải :
+) V lớn nhất khi có hiện tượng hòa tan kết tủa nBaCO3 < nBa2+ => CO32- tạo hết thành kết tủa => nCO2 = nOH – nBaCO3 Lời giải chi tiết :
V lớn nhất khi có hiện tượng hòa tan kết tủa nOH = nNaOH + nKOH + 2nBa(OH)2 = 0,8 mol nBaCO3 = 0,14 mol < nBa2+ = 0,2 mol => CO32- tạo hết thành kết tủa => nCO2 = nOH – nBaCO3 = 0,66 mol => V = 14,784 lít
Câu 6 :
Hấp thụ hoàn toàn 1,12 lít khí CO2 (đktc) vào 200 ml dung dịch KOH 1M thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là
Đáp án : B Phương pháp giải :
+) nKOH > 2nCO2 => OH- dư => dung dịch sau phản ứng gồm K2CO3 0,05 mol và KOH dư 0,1 mol Nhỏ từ từ HCl đến khi có khí thì dừng, có các phản ứng sau : HCl + KOH → KCl + H2O HCl + K2CO3 → KHCO3 + KCl +) nHCl = nKOH + nK2CO3 Lời giải chi tiết :
nCO2 = 0,05 mol; nKOH = 0,2 mol > 2nCO2 => OH- dư => dung dịch sau phản ứng gồm K2CO3 0,05 mol và KOH dư 0,1 mol Nhỏ từ từ HCl đến khi có khí thì dừng, có các phản ứng sau : HCl + KOH → KCl + H2O K2CO3 + HCl → KHCO3 + KCl => nHCl = nKOH + nK2CO3 = 0,15 mol => V = 0,06 lít = 60 ml
Câu 7 :
Cho V lít CO2 (đktc) hấp thụ hết trong dung dịch chứa 0,2 mol Ba(OH)2; 0,05 mol NaOH và 0,05 mol KOH. Sau phản ứng hoàn toàn thu được kết tủa và dung dịch chứa 22,15 gam muối. Giá trị của V là
Đáp án : D Phương pháp giải :
Xét dung dịch sau phản ứng chứa : x mol Ba2+ ; 0,05 mol K+ ; 0,05 mol Na+ và HCO3- Bảo toàn điện tích : nHCO3 = 2.nBa2+ + nK+ + nNa+ +) mmuối =mBa2+ + mK+ + mNa+ + nHCO3 = 22,15 gam => x = 0,05 mol +) Bảo toàn C : nCO2 = nCO3 + nHCO3 Lời giải chi tiết :
Xét dung dịch sau phản ứng chứa : x mol Ba2+ ; 0,05 mol K+ ; 0,05 mol Na+ và HCO3- Bảo toàn điện tích : nHCO3 = 0,1 + 2x mol => mmuối = mBa2+ + mK+ + mNa+ + nHCO3 = 22,15 gam => x = 0,05 mol => nBaCO3 = 0,2 – 0,05 = 0,15 mol +) Bảo toàn C : nCO2 = nCO3 + nHCO3 = 0,35 mol => VCO2 = 7,84 lít
Câu 8 :
Sục khí CO2 từ từ cho đến dư vào 100 ml dung dịch hỗn hợp NaOH 0,6M và Ba(OH)2 0,5M thu được dung dịch A. Cô cạn dung dịch A rồi nhiệt phân đến khối lượng không đổi thu được m gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
Đáp án : A Phương pháp giải :
CO2 đến dư thì dung dịch gồm 0,06 mol NaHCO3 và 0,05 mol Ba(HCO3)2 Khi nhiệt phân hoàn toàn thu được : 0,03 mol Na2CO3 và 0,05 mol BaO Lời giải chi tiết :
CO2 đến dư thì dung dịch gồm 0,06 mol NaHCO3 và 0,05 mol Ba(HCO3)2 Khi nhiệt phân hoàn toàn thu được : 0,03 mol Na2CO3 và 0,05 mol BaO => m = 0,03.106 + 0,05.153 = 10,83 gam
Câu 9 :
Hấp thụ hoàn toàn 8,96 lít CO2 (đktc) vào V ml dung dịch chứa NaOH 2,75M và K2CO3 1M. Cô cạn dung dịch sau phản ứng ở nhiệt độ thường thu được 64,5 gam chất rắn khan gồm 4 muối. Giá trị của V là
Đáp án : D Phương pháp giải :
+) mrắn = mNa + mK + mCO3 + mHCO3 => 64,5 (1) +) Bảo toàn điện tích : nNa++ nK+= nHCO−3+2.nCO2−3 (2) +) Bảo toàn C : nCO2 + nK2CO3 = x + y (3) Từ (1), (2) và (3) ta có : v = 0,2 lít = 200 ml Lời giải chi tiết :
Vì phản ứng tạo 4 muối => có tạo x mol CO32- và y mol HCO3- => mrắn = mNa + mK + mCO3 + mHCO3 => 64,5 = 23.2,75V + 39.2V + 60x + 61y (1) Bảo toàn điện tích : nNa++ nK+= nHCO−3+2.nCO2−3 => 2,75V + 2V = 2x + y (2) Bảo toàn C : nCO2 + nK2CO3 = x + y = 0,4 + V (3) Từ (1), (2) và (3) ta có : V = 0,2 lít = 200 ml
Câu 10 :
Hấp thụ hoàn toàn V lít CO2 (đktc) vào bình đựng 200 ml dung dịch NaOH 1M và Na2CO3 0,5M. Cô cạn dung dịch sau phản ứng thu được 19,9 gam chất rắn khan. Giá trị của V là :
Đáp án : B Phương pháp giải :
TH1: Giả sử CO2 phản ứng hết, sau phản ứng thu được NaHCO3 và Na2CO3 +) Bảo toàn nguyên tử Na: nNa+ trước phản ứng = nNaHCO3 + 2.nNa2CO3 TH2: Giả sử CO2 hết, NaOH dư => sau phản ứng thu được Na2CO3 (x mol) và NaOH dư (y mol) +) Bảo toàn Na: nNa+ trước phản ứng = 2.nNa2CO3 + nNaOH dư +) mrắn khan = mNa2CO3 + mNaOH +) Bảo toàn C: nCO2 + nNa2CO3 phản ứng = nNa2CO3 sau phản ứng Lời giải chi tiết :
nNaOH = 0,2 mol ; nNa2CO3 = 0,1 mol TH1: Giả sử CO2 phản ứng hết, sau phản ứng thu được NaHCO3 và Na2CO3 Đặt nNaHCO3 = a mol, nNa2CO3 = b mol Bảo toàn nguyên tử Na: nNa+ trước phản ứng = nNaHCO3 + 2.nNa2CO3 => a + 2b = 0,4 (1) => mrắn = 84a + 106b = 19,9 (2) Từ (1) và (2) => loại vì a < 0 TH2: Giả sử CO2 hết, NaOH dư => sau phản ứng thu được Na2CO3 (x mol) và NaOH dư (y mol) Bảo toàn Na: nNa+ trước phản ứng = 2.nNa2CO3 + nNaOH dư => 2x + y = 0,4 (1) mrắn khan = mNa2CO3 + mNaOH => 106x + 40y = 19,9 (2) Từ (1) và (2) => x = 0,15 mol; y = 0,1 mol Bảo toàn C: nCO2 + nNa2CO3 phản ứng = nNa2CO3 sau phản ứng => nCO2 = 0,15 – 0,1 = 0,05 mol => V = 1,12 lít
Câu 11 :
Dẫn từ từ 5,6 lít CO2 (đktc) vào 400 ml dung dịch chứa đồng thời các chất NaOH 0,3M; KOH 0,2M; Na2CO3 0,1875M; K2CO3 0,125M thu được dung dịch X. Thêm dung dịch CaCl2 dư vào dung dịch X, số gam kết tủa thu được là:
Đáp án : A Phương pháp giải :
Vì nOH- < nCO2 => CO2 phản ứng với OH- tạo HCO3- CO2 + OH- → HCO3- CO2 + CO32- + H2O → 2HCO3- => nCO3 = 0,125 – 0,05 = 0,075 mol => nCaCO3 = nCO3 = 0,075 => mCaCO3 = 7,5g Lời giải chi tiết :
nCO2 = 0,25 mol; nNaOH = 0,12 mol; nKOH = 0,08 mol; nNa2CO3 = 0,075 mol; nK2CO3 = 0,05 mol => nCO3 = 0,125 mol ; nOH = 0,2 mol Vì nOH- < nCO2 => CO2 phản ứng với OH- tạo HCO3- CO2 + OH- → HCO3- 0,2 ← 0,2 CO2 + CO32- + H2O → 2HCO3- 0,05 → 0,05 => nCO3 = 0,125 – 0,05 = 0,075 mol => nCaCO3 = nCO3 = 0,075 => mCaCO3 = 7,5g
Câu 12 :
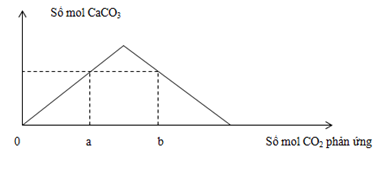
Khi sục từ từ đến dư CO2 vào dung dịch hỗn hợp gồm a mol NaOH và b mol Ca(OH)2, kết quả thí nghiệm được biểu diễn trên đồ thị sau  Tỉ lệ a : b là
Đáp án : D Phương pháp giải :
Tại điểm nCO2 = 0,5 mol, lượng kết tủa đạt tối đa => nCa(OH)2 = nCaCO3 Tại điểm nCO2 = 1,4 mol thì kết tủa bị hòa tan hết, dung dịch thu được gồm Ca(HCO3)2 và NaHCO3 Bảo toàn C: nCO2 = 2.nCa(HCO3)2 + nNaHCO3 Lời giải chi tiết :
Tại điểm nCO2 = 0,5 mol, lượng kết tủa đạt tối đa => nCa(OH)2 = nCaCO3 = 0,5 mol => b = 0,5 (1) Tại điểm nCO2 = 1,4 mol thì kết tủa bị hòa tan hết, dung dịch thu được gồm Ca(HCO3)2 và NaHCO3 Bảo toàn C: nCO2 = 2.nCa(HCO3)2 + nNaHCO3 => 2b + a = 1,4 (2) Thay (1) vào (2) => a = 0,4 => a : b = 0,4 : 0,5 = 4 : 5
Câu 13 :
Sục 13,44 lít CO2 (đktc) vào 200 ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M. Sau phản ứng thu được m1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với 200 ml dung dịch BaCl2 1,2M; KOH 1,5M thu được m2 gam kết tủa. Giá trị của m2 là:
Đáp án : D Phương pháp giải :
nCO2 < nOH- < 2.nCO2 => tạo 2 muối HCO3- (x mol) và CO32- (y mol) +) Bảo toàn điện tích: nOH- = nHCO3 + 2.nCO3 +) dung dịch X gồm: 0,1 mol Ba2+; 0,4 mol HCO3-; 0,2 mol Na+ Lời giải chi tiết :
nOH- = 0,8 Bảo toàn điện tích: nOH- = nHCO3 + 2.nCO3 => x + 2y = 0.8 => x = 0,4 và y = 0,2 => m2 = 0,3.197 = 59,1 gam
Câu 14 :
Hấp thụ hoàn toàn 8,96 lít khí CO2 (đktc) vào dung dịch chứa x mol Ba(OH)2, x mol KOH, y mol NaOH. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 32,15 gam muối và 19,7 gam kết tủa. Bỏ qua sự thủy phân của các ion. Tỉ lệ x : y có thể là
Đáp án : C Lời giải chi tiết :
nCO2 = 0,4 mol; nBaCO3 = 0,1 mol Giả sử muối chứa Ba(HCO3)2 => dung dịch thu được gồm K+ (x mol); Na+ (y mol); Ba2+ và HCO3- (a mol) Bảo toàn điện tích: nBa2+ = 0,5a – 0,5x – 0,5y Bảo toàn nguyên tố C: nCO2 = nHCO3 + nBaCO3 => 0,4 = a + 0,1 => a = 0,3 (1) Bảo toàn nguyên tố Ba: nBa(OH)2 = nBa2+ + nBaCO3 => x = 0,5a – 0,5x – 0,5y + 0,1 (2) mmuối = mK+ + mNa+ + mBa2+ + mHCO3- => 39x + 23y + 137.(0,5a – 0,5x – 0,5y) + 61a = 32,15 (3) Từ (1), (2) và (3) => a = 0,3; x = 0,15; y = 0,05 => x : y = 3 : 1
Câu 15 :
Hấp thụ hoàn toàn V lít CO2 vào dung dịch Ca(OH)2 a M thì thu được m1 gam kết tủa. Nếu hấp thụ (V + 3,36) lít CO2 vào dung dịch Ca(OH)2 trên thì thu được m2 gam kết tủa. Nếu thêm (V + V1) lít CO2 vào dung dịch Ca(OH)2 đã cho thì thu được lượng kết tủa cực đại. Biết m1 : m2 = 3 : 2; m1 bằng 3/7 khối lượng kết tủa cực đại, các khí đều ở đktc. Giá trị của V1 là
Đáp án : C Phương pháp giải :
Từ : m1 = 1,5m2 và m1 = 3/7mmax => 0,15 = mmax−m1+mmax−m2100→{m1=5mmax=35/3 +) nCaCO3 max = n + n1 (với n, n1 là số mol ứng với V, V1 lít CO2) Nếu hấp thụ V lít CO2 thì Ca(OH)2 còn dư => nCO2 = n = nCaCO3 (m1) Lời giải chi tiết :
Ta thấy lượng 0,15 mol CO2 đưa vào làm 2 nhiệm vụ : +) Đưa kết tủa từ m1 lên cực đại +) Đưa kết tủa từ cực đại đến m2 Từ : m1 = 1,5m2 và m1 = 3/7mmax => ta có : 0,15 = mmax−m1+mmax−m2100→{m1=5mmax=35/3 => nCaCO3 max = n + n1 = 7/60 mol Nếu hấp thụ V lít CO2 thì Ca(OH)2 còn dư => nCO2 = n = nCaCO3 (m1) = 0,05 mol => n1 = 1/15 mol => V1 = 1,493 lít
Câu 16 :
Hấp thụ hết 8,96 lít CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 400 ml dung dịch X. Lấy 200 ml dung dịch X cho từ từ vào 600 ml dung dịch HCl 0,5M, thu được 5,376 lít khí (đktc). Mặt khác, 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư thu được 39,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của x là
Đáp án : B Phương pháp giải :
+) nBaCO3 = nC(100 ml X) = 0,2 mol +) Bảo toàn C : nCO2 bđ + nK2CO3 = nC(100 ml X) Giả sử trong 200 ml X có a mol K2CO3 và b mol KHCO3 Bảo toàn C: a + b = 0,2.2 = 0,4 mol Cho từ từ X vào nHCl = 0,3 mol tạo nCO2 = 0,24 mol => K2CO3 và KHCO3 phản ứng đồng thời (vì HCl lúc đầu dư) theo tỉ lệ mol a : b Gọi nK2CO3 pứ = ax và nKHCO3 pứ = bx => 2ax + bx = nHCl = 0,3 mol ; ax + bx = nCO2 = 0,24 mol +) Bảo toàn K : x + 2y = 2.(2a + b) Lời giải chi tiết :
nCO2 bđ = 0,4 mol 100 ml X + Ba(OH)2 => nBaCO3 = nC(100 ml X) = 0,2 mol => Trong 400 ml X có 0,8 mol C => Bảo toàn C : nCO2 bđ + nK2CO3 = nC(X) => nK2CO3 = y = 0,4 mol Giả sử trong 200 ml X có a mol K2CO3 và b mol KHCO3 Bảo toàn C: a + b = 0,2.2 = 0,4 mol Cho từ từ X vào nHCl = 0,3 mol tạo nCO2 = 0,24 mol => K2CO3 và KHCO3 phản ứng đồng thời (vì HCl lúc đầu dư) theo tỉ lệ mol a : b Gọi nK2CO3 pứ = ax và nKHCO3 pứ = bx => 2ax + bx = nHCl = 0,3 mol ; ax + bx = nCO2 = 0,24 mol => ax = 0,06 và bx = 0,18 mol => a : b = 1 : 3 => a = 0,1 ; b = 0,3 mol => Bảo toàn K : x + 2y = 2.(2a + b) => x = 0,2 mol
Câu 17 :
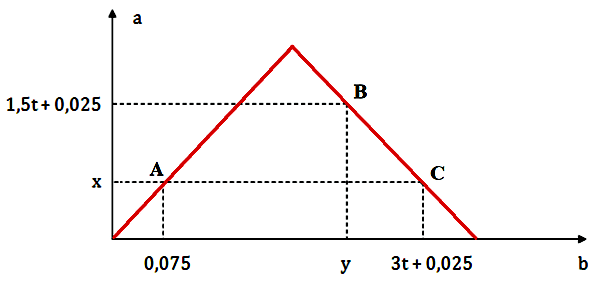
Dẫn từ từ đến dư khí CO2 vào dung dịch chứa 0,2 mol Ba(OH)2. Sự phụ thuộc của số mol kết tủa (a mol) vào số mol khí CO2 tham gia phản ứng (b mol) được biểu diễn như đồ thị sau:
Tỉ lệ y : x là
Đáp án : C Phương pháp giải :
Giai đoạn 1: Đoạn đồ thị đi lên xảy ra phản ứng hình thành kết tủa: CO2 + Ba(OH)2 → BaCO3 + H2O → nBaCO3 = nCO2 pư Giai đoạn 2: Đoạn đồ thị đi xuống xảy ra phản ứng hòa tan kết tủa: BaCO3 + CO2 + H2O → Ba(HCO3)2
Lời giải chi tiết :
CO2 + Ba(OH)2 → BaCO3 + H2O → nBaCO3 = nCO2 pư Vậy tại A thì x = 0,075 Giai đoạn 2: Đoạn đồ thị đi xuống xảy ra phản ứng hòa tan kết tủa: BaCO3 + CO2 + H2O → Ba(HCO3)2 + Tại điểm C(3t+0,025; 0,075) thì thu được: BaCO3: 0,075 Ba(HCO3)2: 0,2 - 0,075 = 0,125 (bảo toàn Ba) Bảo toàn C → nCO2 = nBaCO3 + 2nBa(HCO3)2 = 0,075 + 2.0,125 = 0,325 mol ⟹ 3t + 0,025 = 0,325 ⟹ t = 0,1 + Tại điểm B(y; 1,5t+0,025) = B(y; 0,175) thu được: BaCO3: 0,175 Ba(HCO3)2: 0,2 - 0,175 = 0,025 Bảo toàn C → nCO2 = nBaCO3 + 2nBa(HCO3)2 = 0,175 + 2.0,025 = 0,225 mol Vậy y = 0,225 ⟹ y : x = 0,225 : 0,075 = 3
Câu 18 :
Hấp thụ hoàn toàn khí CO2 vào dung dịch Ca(OH)2, khối lượng kết tủa tạo và phụ thuộc vào thể tích khí CO2 (đktc) được biểu diễn như sau:
Biết Va, là thể tích CO2 cần dùng để có khối lượng kết tủa lớn nhất Va > V. Giá trị của Va là:
Đáp án : B Phương pháp giải :
*Khi dùng Va lít CO2 thì kết tủa cực đại: nCa(OH)2 = nCaCO3 *Khi dùng V lít CO2 thì kết tủa chưa cực đại (vì theo giả thiết V < Va): nCO2 = nCaCO3 *Khi dùng (V + 12,32) lít CO2 thì kết tủa bị tan một phần (do tại đây thể tích CO2 nhiều hơn nhưng thu được ít kết tủa hơn) Lời giải chi tiết :
Giả sử a gam ứng với x mol CaCO3 *Khi dùng Va lít CO2 thì kết tủa cực đại ⟹ nCa(OH)2 = nCaCO3 = 8x (mol) *Khi dùng V lít CO2 thì kết tủa chưa cực đại (vì theo giả thiết V < Va) ⟹ nCO2 = nCaCO3 = 3x (mol) *Khi dùng (V + 12,32) lít CO2 (ứng với 3x + 0,55 mol) thì kết tủa bị tan một phần (do tại đây thể tích CO2 nhiều hơn nhưng thu được ít kết tủa hơn): nCaCO3 = 2x (mol) nCa(HCO3)2 = nCa(OH)2 - nCaCO3 = 8x - 2x = 6x (mol) Bảo toàn C → nCO2 = nCaCO3 + 2nCa(HCO3)2 ⇔ 3x + 0,55 = 2x + 2.6x ⇔ x = 0,05 mol Vậy Va = 22,4 . 8x = 8,96 lít
Câu 19 :
Hấp thụ hoàn toàn V lít khí CO2 (đktc) vào dung dịch Ca(OH)2 dư. Sau phản ứng thu được 10 gam kết tủa. Giá trị của V là
Đáp án : C Phương pháp giải :
Tính theo PTHH: CO2 + Ca(OH)2 → CaCO3 + H2O Lời giải chi tiết :
Phản ứng CO2 và Ca(OH)2 dư: CO2 + Ca(OH)2 → CaCO3 + H2O → nCO2 = nCaCO3 = 10/100 = 0,1 mol → VCO2 = 0,1.22,4 = 2,24 lít
Câu 20 :
Hấp thụ hết V lít khí CO2 (đktc) vào dung dịch chứa 0,3 mol NaOH và 0,2 mol Ba(OH)2 thu được a gam kết tủa và dung dịch X. Để thu được lượng kết tủa lớn nhất cần cho thêm 4000 ml dung dịch Ba(OH)2 0,1M vào X. Giá trị của V là
Đáp án : A Phương pháp giải :
Sử dụng bảo toàn nguyên tố Ba, C Kết tủa thu được lớn nhất khi tất cả C trong CO2 chuyển thành C trong BaCO3 BTNT “Ba”: nBaCO3 = nBa(OH)2 lần 1+ nBa(OH)2 lân 2 = ? (mol) BTNT “C”: nCO2 = nBaCO3 = ? ⟹ VCO2(đktc) = ? Lời giải chi tiết :
4000 ml = 4 lít nBa(OH)2 = V.CM = 4.0,1 = 0,4 (mol) Kết tủa thu được lớn nhất khi tất cả C trong CO2 chuyển thành C trong BaCO3 BTNT “Ba”: nBaCO3 = nBa(OH)2 lần 1+ nBa(OH)2 lân 2 = 0,2 + 0,4 = 0,6 (mol) BTNT “C”: nCO2 = nBaCO3 = 0,6 (mol) ⟹ VCO2 (đktc)= 0,6.22,4 = 13,44 (lít)
Câu 21 :
Cho dung dịch A chứa Ca(OH)2 0,1 mol và NaOH 0,2 mol tác dụng với V lít CO2 (đktc). Giá trị lớn nhất của V để thu được kết tủa lớn nhất là
Đáp án : C Phương pháp giải :
Để thu được kết tủa lớn nhất thì tất cả Ca2+ chuyển về dạng CaCO3 Để giá trị V lớn nhất khi dd muối thu được chỉ chứa muối NaHCO3 Viết PTHH xảy ra, tính số mol CO2 theo số mol Ca(OH)2 và NaOH. Lời giải chi tiết :
Để thu được kết tủa lớn nhất thì tất cả Ca2+ chuyển về dạng CaCO3 Để giá trị V lớn nhất khi dd muối thu được chỉ chứa muối NaHCO3 PTHH: Ca(OH)2 + CO2 → CaCO3↓ + H2O (1) NaOH + CO2 → NaHCO3 (2) Theo PTHH (1): nCO2 = nCa(OH)2 = 0,1 (mol) Theo PTHH (2): nCO2 = nNaOH = 0,2 (mol) → ∑nCO2 = 0,1 + 0,2 = 0,3 (mol) → VCO2(đktc) = 0,3×22,4 = 6,72 (lít)
Câu 22 :
Sục CO2 vào dung dịch hỗn hợp gồm Ca(OH)2 và NaOH ta thu được kết quả sau
Giá trị của x là
Đáp án : A Phương pháp giải :
Thứ tự phản ứng khi cho CO2 là CO2 + Ca(OH)2 → CaCO3 + H2O (1) 2NaOH + CO2 → Na2CO3 + H2O (2) Na2CO3 + CO2 + H2O → 2NaHCO3 (3) CaCO3 + CO2 + H2O → Ca(HCO3)2 (4) Trong mỗi trường hợp, xác định mức độ phản ứng trong mối trường hợp => Tại thời điểm x mol, sau phản ứng có sinh ra những muối gì Từ phương trình tìm ra x. Lời giải chi tiết :
Thứ tự phản ứng khi cho CO2 là CO2 + Ca(OH)2 → CaCO3 + H2O (1) 2NaOH + CO2 → Na2CO3 + H2O (2) Na2CO3 + CO2 + H2O → 2NaHCO3 (3) CaCO3 + CO2 + H2O → Ca(HCO3)2 (4) Tại thời điểm kết nCO2 = a mol thì kết tủa bắt đầu cực đại => chỉ xảy ra phản ứng (1) => nCaCO3 = nCa(OH)2 = nCO2 = a = 0,1 mol Tại thời điểm nCO2 = a + 0,5 mol = 0,6 mol thì kết tủa bắt đầu tan => xảy ra phản ứng (1)(2)(3) với sản phẩm tạo ra là CaCO3 : 0,1 mol và NaHCO3 Bảo toàn C có nNaHCO3 = nCO2 – nCaCO3 = 0,6 – 0,1 = 0,5 mol Bảo toàn Na có nNaOH = nNaHCO3 = 0,5 mol Tại thời điểm x mol thì kết tủa có 0,06 mol => xảy ra cả 4 phản ứng với kết tủa CaCO3 bị hòa tan một phần => muối có NaHCO3, Ca(HCO3)2 và CaCO3 Thì nNaHCO3 = 0,5 mol; nCa(HCO3)2 = 0,1 – 0,06 = 0,04 mol Bảo toàn C có nCO2 = x = nNaHCO3 + 2nCa(HCO3)2 + nCaCO3 = 0,5 + 2.0,04 + 0,06 = 0,64 mol
Câu 23 :
Sục V lít khí CO2 (đktc) vào bình đựng 2 lít dung dịch Ca(OH)2 0,01M, thu được 1 g kết tủa. Xác định V.
Đáp án : A Phương pháp giải :
Trường hợp 1: Phản ứng chỉ tạo 1 gam kết tủa CO2 + Ca(OH)2 → CaCO3 + H2O Trường hợp 2: Phản ứng tạo ra nhiều hơn 1 gam kết tủa, sau đó tan bớt trong CO2 dư còn lại 1 gam CO2 + Ca(OH)2 → CaCO3 + H2O CaCO3 + CO2 + H2O → Ca(HCO3)2 Lời giải chi tiết :
Sục khí CO2 vào dung dịch Ca(OH)2 thu được 1 g kết tủa thì có 2 trường hợp xảy ra. Trường hợp 1: Phản ứng chỉ tạo ra 1 g kết tủa: nCaCO3=1100=0,01(mol) CO2 + Ca(OH)2 → CaCO3 + H2O (1) 0,01 ← 0,01 (mol) Theo đề bài: nCa(OH)2 = 0,01.2 = 0,02 (mol). Vậy Ca(OH)2 dư. VCO2 = 22,4.0,01 = 0,224 (lít). Trường hợp 2: Phản ứng tạo ra nhiều hơn 1 g kết tủa, sau đó tan bớt trong CO2 dư còn lại 1 g. CO2 + Ca(OH)2 → CaCO3 + H2O 0,02 ← 0,02 → 0,02 (mol) Số mol CaCO3 bị tan: 0,02 - 0,01 = 0,01 mol CaCO3 + CO2 + H2O → Ca(HCO3)2 0,01 → 0,01 (mol) VCO2 = 22,4.(0,02 + 0,01) = 0,672 (lít).
Câu 24 :
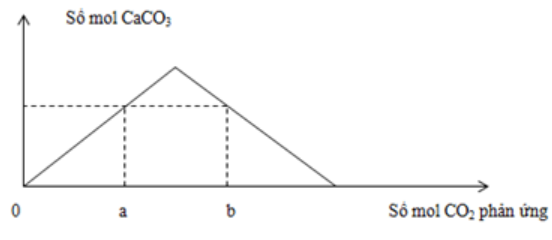
Thổi từ từ khí CO2 đến dư vào dung dịch chứa 0,12 mol Ca(OH)2 . Sự phụ thuộc của số mol kết tủa thu được vào số mol CO2 phản ứng được biểu điễn theo đồ thị sau:
Mối quan hệ của a và b là:
Đáp án : A Lời giải chi tiết :
Các phản ứng: Ca(OH)2 + CO2 → CaCO3 + H2O(1) CaCO3 + CO2 + H2O → Ca(HCO3)2(2) - Tại nCO2 = a (đồ thị đi lên) => Chỉ xảy ra phản ứng (1) => nCaCO3 = nCO2 = a - Tại nCO2 = b (đồ thị đi xuống): Kết tủa đã bị hòa tan một phần Sản phẩm lúc này gồm: CaCO3: a mol Ca(HCO3)2: 0,12 - a (BTNT "Ca") BTNT "C": nCO2 = nCaCO3 + 2nCa(HCO3)2 => b = a + 2(0,12 - a) => b = 0,24 - a
Câu 25 :
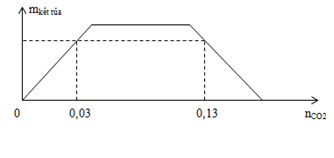
Sục khí CO2 vào V ml dung dịch hỗn hợp NaOH 0,2M và Ba(OH)2 0,1M. Đồ thị biểu diễn khối lượng kết tủa theo số mol CO2 phản ứng như sau:
Giá trị của V là:
Đáp án : C Phương pháp giải :
Thứ tự các phản ứng: CO2 + Ba(OH)2 → BaCO3 + H2O (1) CO2 + 2NaOH → Na2CO3 + H2O (2) CO2 + Na2CO3 + H2O → 2NaHCO3 (3) CO2 + BaCO3 + H2O → Ba(HCO3)2 (4) - Đoạn 1 đồ thị đi lên: chỉ xảy ra phản ứng (1) (kết tủa tăng) - Đoạn 2 đồ thị nằm ngang: chỉ xảy ra phản ứng (2) và (3) (kết tủa không đổi) - Đoạn 3 đồ thị đi xuống: chỉ xảy ra phản ứng (4) (kết tủa bị hòa tan) Lời giải chi tiết :
Thứ tự các phản ứng: CO2 + Ba(OH)2 → BaCO3 + H2O (1) CO2 + 2NaOH → Na2CO3 + H2O (2) CO2 + Na2CO3 + H2O → 2NaHCO3 (3) CO2 + BaCO3 + H2O → Ba(HCO3)2 (4) - Đoạn 1 đồ thị đi lên: chỉ xảy ra phản ứng (1) (kết tủa tăng): nBaCO3 = nCO2 = 0,03 mol - Đoạn 2 đồ thị nằm ngang: chỉ xảy ra phản ứng (2) và (3) (kết tủa không đổi) - Đoạn 3 đồ thị đi xuống: chỉ xảy ra phản ứng (4) (kết tủa bị hòa tan) Sản phẩm gồm: BaCO3 (0,03 mol) Ba(HCO3)2 (0,1V - 0,03 mol) NaHCO3 (0,2V mol) BTNT "C": nCO2 = nBaCO3 + 2nBa(HCO3)2 + nNaHCO3 => 0,13 = 0,03 + 2(0,1V - 0,03) + 0,2V => V = 0,4 lít = 400 ml
|

















 Giai đoạn 1: Đoạn đồ thị đi lên xảy ra phản ứng hình thành kết tủa:
Giai đoạn 1: Đoạn đồ thị đi lên xảy ra phản ứng hình thành kết tủa: