Trắc nghiệm Ôn tập chương 1 - Hóa 12Đề bài
Câu 1 :
Số đồng phân este ứng với công thức phân tử C4H8O2 là
Câu 2 :
Khi cho 0,15 mol este đơn chức X tác dụng với dung dịch NaOH (dư), sau khi phản ứng kết thúc thì lượng NaOH phản ứng là 12 gam và tổng khối lượng sản phẩm hữu cơ thu được là 29,7 gam. Số đồng phân cấu tạo của X thoả mãn các tính chất trên là
Câu 3 :
Este nào sau đây khi phản ứng với dung dịch NaOH dư, đun nóng không tạo ra hai muối?
Câu 4 :
Thủy phân chất X bằng dung dịch NaOH, thu được hai chất Y và Z đều có phản ứng tráng bạc, Z tác dụng được với Na sinh ra khí H2. Chất X là
Câu 5 :
Thực hiện phản ứng xà phòng hoá chất hữu cơ X đơn chức với dung dịch NaOH thu được một muối Y và ancol Z. Đốt cháy hoàn toàn 2,07 gam Z cần 3,024 lít O2 (đktc) thu được lượng CO2 nhiều hơn khối lượng nước là 1,53 gam. Nung Y với vôi tôi xút thu được khí T có tỉ khối so với không khí bằng 1,03. CTCT của X là:
Câu 6 :
Đun 20,4 gam một chất hữu cơ A đơn chức với 300 ml dung dịch NaOH 1M thu được muối B và hợp chất hữu cơ C. Cho C phản ứng với Na dư thu được 2,24 lít H2 (đktc). Nung B với NaOH rắn thu được khí D có tỉ khối đối với O2 bằng 0,5. Khi oxi hóa C bằng CuO được chất hữu cơ E không phản ứng với AgNO3/NH3. Xác định CTCT của A?
Câu 7 :
Hai este X, Y có cùng công thức phân tử C8H8O2 và chứa vòng benzen trong phân tử. Cho 6,8 gam hỗn hợp gồm X và Y tác dụng với dung dịch NaOH dư, đun nóng, lượng NaOH phản ứng tối đa là 0,06 mol, thu được dung dịch Z chứa 4,7 gam ba muối. Khối lượng muối của axit cacboxylic có phân tử khối lớn hơn trong Z là
Câu 8 :
Khi đốt cháy hoàn toàn một este no, đơn chức thì số mol CO2 sinh ra bằng số mol O2 đã phản ứng. Tên gọi của este là
Câu 9 :
Đốt cháy hoàn toàn 0,11 gam một este X (tạo nên từ một axit cacboxylic đơn chức và một ancol đơn chức) thu được 0,22 gam CO2 và 0,09 gam H2O. Số este đồng phân của X là
Câu 10 :
Hỗn hợp X gồm vinyl axetat, metyl axetat và etyl fomat. Đốt cháy hoàn toàn 3,08 gam X, thu được 2,16 gam H2O. Phần trăm số mol của vinyl axetat trong X là
Câu 11 :
Este X có các đặc điểm sau: - Đốt cháy hoàn toàn X tạo thành CO2 và H2O có số mol bằng nhau; - Thuỷ phân X trong môi trường kiềm được chất Y (tham gia phản ứng tráng gương) và chất Z (có số nguyên tử cacbon bằng một nửa số nguyên tử cacbon trong X). Phát biểu không đúng là:
Câu 12 :
Một hỗn hợp X gồm hai chất hữu cơ đơn chức. Cho X phản ứng vừa đủ với 500 ml dung dịch KOH 1M. Sau phản ứng, thu được hỗn hợp Y gồm hai muối của hai axit cacboxylic và một rượu (ancol). Cho toàn bộ lượng rượu thu được ở trên tác dụng với Na (dư), sinh ra 3,36 lít H2 (ở đktc). Hỗn hợp X gồm
Câu 13 :
Cho m gam hỗn hợp gồm hai chất hữu cơ đơn chức, mạch hở tác dụng vừa đủ với dung dịch chứa 11,2 gam KOH, thu được muối của một axit cacboxylic và một ancol X. Cho toàn bộ X tác dụng hết với Na thu được 3,36 lít khí H2 (ở đktc). Hai chất hữu cơ đó là
Câu 14 :
Đốt cháy hoàn toàn 3,42 gam hỗn hợp gồm axit acrylic, vinyl axetat, metyl acrylat và axit oleic, rồi hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 (dư). Sau phản ứng thu được 18 gam kết tủa và dung dịch X. Khối lượng X so với khối lượng dung dịch Ca(OH)2 ban đầu đã thay đổi như thế nào?
Câu 15 :
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY < MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a : b là
Câu 16 :
Cho glixerin trioleat (hay triolein) lần lượt vào mỗi ống nghiệm chứa riêng biệt: Na, Cu(OH)2, CH3OH, dd Br2, dd NaOH. Trong điều kiện thích hợp, số pư xảy ra là
Câu 17 :
Thuỷ phân hoàn toàn 444 gam một lipit thu được 46 gam glixerol (glixerin) và hai loại axit béo. Hai loại axit béo đó là
Câu 18 :
Xà phòng hoá hoàn toàn 17,24 gam chất béo cần vừa đủ 0,06 mol NaOH. Cô cạn dd sau pư thu được khối lượng xà phòng là
Câu 19 :
Cho 200 gam một loại chất béo có chỉ số axit bằng 7 tác dụng vừa đủ với một lượng NaOH, thu được 207,55 gam hỗn hợp muối khan. Khối lượng NaOH đã tham gia phản ứng là
Câu 20 :
Hỗn hợp X gồm 3 este đơn chức, tạo thành từ cùng một ancol Y với 3 axit cacboxylic (phân tử chỉ có nhóm -COOH); trong đó, có hai axit no là đồng đẳng kế tiếp nhau và một axit không no (có đồng phân hình học, chứa một liên kết đôi C=C trong phân tử). Thủy phân hoàn toàn 5,88 gam X bằng dung dịch NaOH, thu được hỗn hợp muối và m gam ancol Y. Cho m gam Y vào bình đựng Na dư, sau phản ứng thu được 896 ml khí (đktc) và khối lượng bình tăng 2,48 gam. Mặt khác, nếu đốt cháy hoàn toàn 5,88 gam X thì thu được CO2 và 3,96 gam H2O. Phần trăm khối lượng của este không no trong X là
Câu 21 :
Hỗn hợp X chứa ba este mạch hở, trong phân tử chỉ chứa một loại nhóm chức và được tạo bởi các axit cacboxylic có mạch không phân nhánh. Đốt cháy hết 0,2 mol X cần dùng 0,52 mol O2 thu được 0,48 mol H2O. Đun nóng 24,96 gam X cần dùng 560 ml dung dịch NaOH 0,75M thu được hỗn hợp Y chứa các ancol có tổng khối lượng là 13,38 gam và hỗn hợp Z gồm hai muối, trong đó có a gam muối A và b gam muối B (MA < MB). Tỉ lệ gần nhất a : b là
Câu 22 :
Đốt cháy hoàn toàn m gam triglixerit X được CO2 và 18,72 gam H2O. Xà phòng hóa cũng lượng triglixerit X trên bằng lượng vừa đủ dung dịch NaOH rồi cô cạn được rắn khan Y. Đốt cháy hoàn toàn Y thu được Na2CO3, 44,44 gam CO2 và 17,82 gam H2O. Mặt khác m gam triglixerit X trên làm mất màu vừa đủ x mol Br2 trong dung dịch brom. Giá trị x là
Câu 23 :
Chất béo X gồm các triglixerit và các axit béo tự do. Trung hòa lượng axit béo có trong 100 gam chất béo cần dùng 100 ml dung dịch KOH 0,1M. Mặt khác, thủy phân hoàn toàn 100 gam chất béo đó cần dùng 200 ml dung dịch NaOH 2M, đun nóng, sau phản ứng thu được m gam muối. Giá trị của m là
Câu 24 :
Hỗn hợp X gồm axit oleic và triglixerit Y (tỉ lệ mol tương ứng 2 : 3). Đốt cháy hoàn toàn một lượng hỗn hợp X cần vừa đủ 2,82 mol O2, thu được 2,01 mol CO2 và 1,84 mol H2O. Mặt khác, cho 46,98 gam X trên tác dụng tối đa với x mol Br2 trong dung dịch. Giá trị của x là
Câu 25 :
Đốt cháy hoàn toàn 0,08 mol một chất béo X cần dùng vừa đủ 6,36 mol O2. Mặt khác, cho lượng X trên vào dung dịch nước Br2 dư thấy có 0,32 mol Br2 tham gia phản ứng. Nếu cho lượng X trên tác dụng hết với NaOH thì khối lượng muối khan thu được là
Câu 26 :
Đốt cháy hoàn toàn m gam một triglixerit X cần vừa đủ x mol O2, sau phản ứng thu được CO2 và y mol H2O. Biết m = 78x - 103y. Nếu cho a mol X tác dụng với dung dịch Br2 dư thì lượng Br2 phản ứng tối đa là 0,45 mol. Giá trị của a là
Câu 27 :
Đốt cháy hoàn toàn 13,728 gam triglixerit X, thu được a mol hỗn hợp Y gồm CO2 và H2O. Cho toàn bộ hỗn hợp Y qua cacbon nung đỏ, thu được 2,364 mol hỗn hợp Z gồm CO, H2 và CO2. Cho hỗn hợp Z qua dung dịch Ba(OH)2 dư thu được 202,516 gam kết tủa. Cho 13,728 gam X tác dụng được tối đa với 0,032 mol Br2 trong dung dịch. Giá trị của m là
Câu 28 :
Hiđro hóa hoàn toàn 26,52 gam triolein cần vừa đủ V lít khí H2 (đktc). Giá trị của V là:
Câu 29 :
Đốt cháy hoàn toàn 4,03 gam triglixerit X bằng một lượng oxi vừa đủ, cho toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng nước vôi trong dư thu được 25,5 gam kết tủa và khối lượng dung dịch thu được giảm 9,87 gam so với khối lượng nước vôi trong ban đầu. Mặt khác khi thủy phân hoàn toàn 8,06 gam X trong dung dịch NaOH dư đun nóng thu được dung dịch chứa a gam muối. Giá trị của a là
Câu 30 :
Đốt cháy hoàn toàn 13,728 gam một triglixerit X cần vừa đủ 27,776 lít O2 (đktc) thu được số mol CO2 và số mol H2O hơn kém nhau 0,064. Mặt khác, hiđro hóa hoàn toàn một lượng X cần 0,096 mol H2 thu được m gam chất hữu cơ Y. Xà phòng hóa hoàn toàn m gam Y bằng dung dịch NaOH thu được dung dịch chứa a gam muối. Giá trị của a là
Câu 31 :
Cho m gam triolein tác dụng hoàn toàn với H2 dư thu được (m + 0,3) gam chất X. Nếu cho toàn bộ X tác dụng với dung dịch KOH dư, đun nóng thu được a gam muối. Giá trị của a là
Câu 32 :
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2 thu được 6,384 lít CO2 và 4,77 g H2O. Mặt khác m gam X phản ứng vừa đủ với x gam Brom (trong dung môi CCl4). Biết thể tích các khí đo ở đktc. Giá trị của x là:
Câu 33 :
X là trieste tạo bởi glixerol và các axit cacboxylic đơn chức. X có các đặc điểm: - Trong X số nguyên tử cacbon nhiều hơn số nguyên tử oxi là 3. - Đốt cháy hoàn toàn x mol X thu được y mol CO2 và z mol H2O với y - z = 3x. - X có đồng phân hình học cis - trans. Nhận xét nào sau đây là sai?
Câu 34 :
Hỗn hợp X gồm hai đieste (có tỉ lệ mol 1 : 1 và có cùng công thức phân tử C10H10O4) đều chứa vòng benzen. Khi xà phòng hoá hoàn toàn 38,8 gam X bằng dung dịch NaOH vừa đủ, thu được hỗn hợp Y gồm hai ancol có số nguyên tử cacbon bằng nhau và dung dịch Z. Cô cạn dung dịch Z thu được m gam chất rắn gồm các hợp chất hữu cơ. Giá trị của m là
Câu 35 :
Cho sơ đồ các phản ứng theo đúng tỉ lệ mol: X (C18H12O12) + 6NaOH → X1 + 3X2. X1 + 6HCl → X3 + 6NaCl. X3 + C2H5OH → X4 + H2O Biết khi đốt cháy hoàn toàn X1 chỉ tạo ra sản phẩm chứa Na2CO3 và CO2. Phân tử khối của X4 là
Câu 36 :
Phát biểu nào sau đây sai?
Câu 37 :
Thủy phân hoàn toàn triglixerit X trong dung dịch NaOH dư, đun nóng, sinh ra glixerol và hỗn hợp 2 muối gồm natri oleat và natri stearat. Đốt cháy hoàn toàn m gam X cần vừa đủ 1,61 mol O2, thu được H2O và 1,14 mol CO2. Phát biểu nào sau đây đúng?
Câu 38 :
Cho các sơ đồ phản ứng theo đúng tỉ lệ mol: (a) X + 3H2O H2SO4⟷to X1 + X2 + X3 + X4 (b) X1 + 2H2 Ni,to→ X2 Cho biết: X là triglixerit có số liên kết π nhỏ hơn 6 và có 55 nguyên tử cacbon trong phân tử; X1, X2, X3, X4 là những hợp chất hữu cơ khác nhau, X2 nhiều hơn X3 hai nhóm CH2. Nhận định nào sau đây không đúng?
Lời giải và đáp án
Câu 1 :
Số đồng phân este ứng với công thức phân tử C4H8O2 là
Đáp án : C Phương pháp giải :
B1: Tính độ không no k B2: viết các đồng phân thỏa mãn Lời giải chi tiết :
k=π+v=2.4+2−82=1 → Este no, đơn chức, mạch hở (1) HCOOCH2CH2CH3 (2) HCOOCH(CH3)2 (3) CH3COOCH2CH3 (4) CH3CH2COOCH3
Câu 2 :
Khi cho 0,15 mol este đơn chức X tác dụng với dung dịch NaOH (dư), sau khi phản ứng kết thúc thì lượng NaOH phản ứng là 12 gam và tổng khối lượng sản phẩm hữu cơ thu được là 29,7 gam. Số đồng phân cấu tạo của X thoả mãn các tính chất trên là
Đáp án : C Phương pháp giải :
+) So sánh nNaOH và neste => dạng của este +) BTKL: meste = msản phẩm hữu cơ + mH2O - mNaOH => Meste => Các CTCT thỏa mãn Lời giải chi tiết :
nNaOH=1240=0,3mol=2neste → este của phenol RCOOC6H4R’ RCOOC6H4R’ +2NaOH → RCOONa + R’C6H4ONa + H2O meste = msản phẩm hữu cơ + mH2O - mNaOH = 29,7 + 0,15.18 – 12 = 20,4 g Meste=20,40,15=136→ C8H8O2 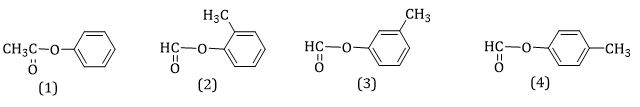
Câu 3 :
Este nào sau đây khi phản ứng với dung dịch NaOH dư, đun nóng không tạo ra hai muối?
Đáp án : C Lời giải chi tiết :
C6H5COOC6H5 + 2NaOH → C6H5COONa + C6H5ONa + H2O CH3COO-[CH2]2-OOCCH2CH3 + 2NaOH → CH3COONa + CH3CH2COONa + CH2OH-CH2OH CH3OOC-COOCH3 + 2NaOH → (COONa)2 + 2CH3OH CH3COOC6H5 + 2NaOH → CH3COONa + C6H5ONa + H2O
Câu 4 :
Thủy phân chất X bằng dung dịch NaOH, thu được hai chất Y và Z đều có phản ứng tráng bạc, Z tác dụng được với Na sinh ra khí H2. Chất X là
Đáp án : A Phương pháp giải :
Z vừa có phản ứng tráng bạc, vừa tác dụng được với Na => Z chứa gốc –CHO và –OH => chất X Lời giải chi tiết :
Z vừa có phản ứng tráng bạc, vừa tác dụng được với Na => Z chứa gốc –CHO và –OH => X có dạng HCOOCH=CH-R-OH hoặc HCOO-CH2-RCHO Từ 4 đáp án => X là HCOO-CH2CHO PTHH: HCOO-CH2CHO + NaOH → HCOONa + HO-CH2CHO
Câu 5 :
Thực hiện phản ứng xà phòng hoá chất hữu cơ X đơn chức với dung dịch NaOH thu được một muối Y và ancol Z. Đốt cháy hoàn toàn 2,07 gam Z cần 3,024 lít O2 (đktc) thu được lượng CO2 nhiều hơn khối lượng nước là 1,53 gam. Nung Y với vôi tôi xút thu được khí T có tỉ khối so với không khí bằng 1,03. CTCT của X là:
Đáp án : D Phương pháp giải :
+) mX+mO2=mCO2+mH2O => PT (1) +) theo gt, khối lượng CO2 nhiều hơn nước là 1,53 gam => PT (2) +) nH2O>nCO2=> CTTQ của Z +) Từ phản ứng đốt cháy Z => nH2OnCO2⇒n Lời giải chi tiết :
=> X là este đơn chức: RCOOR’.
Và 44.nCO2−18.nH2O=1,53 gam⇒nCO2=0,09 mol; nH2O=0,135 mol nH2O>nCO2 => Z là ancol no, đơn chức, mạch hở có công thức: CnH2n+1OH (n ≥ 1) Từ phản ứng đốt cháy Z => nH2OnCO2=n+1n=0,1350,09⇒n=2 Y có dạng CxHyCOONa => T: CxHy+1 => MT = 12x + y + 1 = 1,03.29 => x = 2 và y = 6 => CTPT este: C2H5COOC2H5
Câu 6 :
Đun 20,4 gam một chất hữu cơ A đơn chức với 300 ml dung dịch NaOH 1M thu được muối B và hợp chất hữu cơ C. Cho C phản ứng với Na dư thu được 2,24 lít H2 (đktc). Nung B với NaOH rắn thu được khí D có tỉ khối đối với O2 bằng 0,5. Khi oxi hóa C bằng CuO được chất hữu cơ E không phản ứng với AgNO3/NH3. Xác định CTCT của A?
Đáp án : B Phương pháp giải :
+) Biện luận chất C là ancol bậc 2 +) Dựa vào các đáp án cho A là este đơn chức => B là muối của Na +) Nung B với NaOH rắn tạo ra D => chất D +) nancol = 2.nH2 +) so sánh nNaOH và nancol => tính số mol este => Meste Lời giải chi tiết :
Chất C tác dụng với Na sinh ra khí H2 => C là ancol Oxi hóa C ra E không phản ứng với AgNO3 => C không là ancol bậc 1 Dựa vào các đáp án cho A là este đơn chức => B là muối của Na Nung B với NaOH rắn tạo ra D có MD = 32.0,5 = 16 => D là CH4 => Gốc R trong D là CH3- Đặt công thức của A là RCOOR’ CH3COOR’ + NaOH → CH3COONa + R’OH R’OH + Na → R’ONa + H2 Ta có: nH2 = 0,1 mol => nancol = 2.0,1 = 0,2 mol nNaOH = 0,3 mol > nancol => NaOH dư, este phản ứng hết => neste = nancol = 0,2 mol => Meste=20,40,2=102 => R’ = 102 – 59 = 43 => gốc R’ là C3H7- và ancol bậc 2
Câu 7 :
Hai este X, Y có cùng công thức phân tử C8H8O2 và chứa vòng benzen trong phân tử. Cho 6,8 gam hỗn hợp gồm X và Y tác dụng với dung dịch NaOH dư, đun nóng, lượng NaOH phản ứng tối đa là 0,06 mol, thu được dung dịch Z chứa 4,7 gam ba muối. Khối lượng muối của axit cacboxylic có phân tử khối lớn hơn trong Z là
Đáp án : A Phương pháp giải :
+) Tính độ không no k +) So sánh nhỗn hợp với nNaOH => các chất trong Z +) Gọi nX = x và nY = y +) Khối lượng hỗn hợp => PT (1) +) Số mol NaOh phản ứng => PT (2) (1), (2) => x, y +) Bảo toàn khối lượng: => mH2O + mancol →¯M => CTPT của ancol +) Kết hợp Z chứa 3 muối => X và Y Lời giải chi tiết :
k=π+v=8.2+2−82=4 nhỗn hợp = 6,8136=0,05mol→1<nNaOHnhh<2 mà Z chứa 2 muối → Z chứa 1 este của phenol và 1 este của ancol. Gọi X là este của phenol và Y là este của ancol Ta có: Este của phenol (X) + 2NaOH→ Muối của axit cacboxylic + muối phenolat + H2O Este của ancol (Y) + NaOH → Muối của axit cacboxylic + ancol →{nX=xmolnY=ymol→{x+y=0,052x+y=0,06→{x=0,01y=0,04→∑(nH2O+nancol)=0,01+0,04=0,05mol Bảo toàn khối lượng: ∑(mH2O+mancol)=6,8+0,06.40−4,7=4,5gam →¯M=4,50,05=90→{H2OC6H5CH2OH →{Y:HCOOCH2C6H5X:[HCOOC6H4CH3CH3COOC6H5 Kết hợp Z chứa 3 muối →{Y:HCOOCH2C6H5X:CH3COOC6H5 Thỏa mãn MCH3COONa>MHCOONa→ Khối lượng muối có phân tử khối lớn hơn: →nCH3COONa=nY=0,01mol→mCH3COONa=0,01.82=0,82gam
Câu 8 :
Khi đốt cháy hoàn toàn một este no, đơn chức thì số mol CO2 sinh ra bằng số mol O2 đã phản ứng. Tên gọi của este là
Đáp án : A Phương pháp giải :
+) Este no, đơn chức có CTPT CnH2nO2 +) Viết PT đốt cháy hoặc sử dụng bảo toàn oxi => n Lời giải chi tiết :
Gọi CTPT của este no, đơn chức, mạch hở là CnH2nO2(n⩾ {C_n}{H_{2n}}{O_2} + \dfrac{{3n - 2}}{2}{O_2}\xrightarrow{{{t^o}}}nC{O_2} + n{H_2}O {n_{C{O_2}}} = {n_{{O_2}}} \to n = \dfrac{{3n - 2}}{2} \to n = 2 \to {C_2}{H_4}{O_{2\,}}\,\,\, \Leftrightarrow \,\,\,HCOOC{H_3} (metyl fomiat)
Câu 9 :
Đốt cháy hoàn toàn 0,11 gam một este X (tạo nên từ một axit cacboxylic đơn chức và một ancol đơn chức) thu được 0,22 gam CO2 và 0,09 gam H2O. Số este đồng phân của X là
Đáp án : A Phương pháp giải :
+) Từ nCO2 và nH2O => mC và mH +) BTKL: {m_{este}} = {m_C} + {m_H} + {m_O}\, \Rightarrow {m_O} \Rightarrow {n_O} +) Este đơn chức {n_{este}} = \dfrac{1}{2}{n_O} => số nguyên tử C và số nguyên tử H Lời giải chi tiết :
{n_{C{O_2}}} = 0,005\,mol\, \to {n_C} = {n_{C{O_2}}} = 0,005\,mol \to {m_C} = 0,005.12 = 0,06\,g {n_{{H_2}O}} = 0,005\,mol\, \to {n_H} = 2{n_{{H_2}O}} = 0,005.2 = 0,01\,mol \to {m_H} = 0,01\,g Áp dụng định luật bảo toàn khối lượng ta có : {m_{este}} = {m_C} + {m_H} + {m_O}\, \to {m_O} = 0,11 - 0,06 - 0,01 = 0,04\,g \to {n_O} = \dfrac{{0,04}}{{16}} = 0,0025\,mol Este đơn chức {n_{este}} = \dfrac{1}{2}{n_O} = 0,00125\,\,mol\,\, Số nguyên tử C = \dfrac{{{n_{C{O_2}}}}}{{{n_{este}}}} = \dfrac{{0,005}}{{0,00125}} = 4 Số nguyên tử H = \dfrac{{2{n_{{H_2}O}}}}{{{n_{este}}}} = \dfrac{{0,005.2}}{{0,00125}} = 8 CTPT của X là : {C_4}{H_8}{O_2}→ este no, đơn chức, mạch hở Số đồng phân là : HCOOC{H_2}C{H_2}C{H_{3\,}};HCOOCH{(C{H_{3\,}})_2};C{H_3}COO{C_2}{H_5};{C_2}{H_5}COOC{H_3}
Câu 10 :
Hỗn hợp X gồm vinyl axetat, metyl axetat và etyl fomat. Đốt cháy hoàn toàn 3,08 gam X, thu được 2,16 gam H2O. Phần trăm số mol của vinyl axetat trong X là
Đáp án : D Phương pháp giải :
+) Quy đổi hỗn hợp thành : {C_4}{H_6}{O_2} và {C_3}{H_6}{O_2}, số mol lầ lượt là x và y +) BTNT H => PT (1) +) Từ khối lượng hỗn hợp X => PT (2) Lời giải chi tiết :
Vinyl axetat (C4H6O2): C{H_3}COOCH = C{H_2} Metyl axetat (C3H6O2): C{H_3}COOC{H_3}\, Etyl fomat (C3H6O2): HCOO{C_2}{H_5}\,\, Quy đổi hỗn hợp thành : {C_4}{H_6}{O_2} và {C_3}{H_6}{O_2} {n_{{H_2}O}} = \dfrac{{2,16}}{{18}} = 0,12\,\,mol Ta có : \left\{ \begin{gathered}{n_{{C_3}{H_6}{O_2}}} = x\,mol \hfill \\{n_{{C_4}{H_6}{O_2}}} = y\,mol \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}3x + 3y = {n_{{H_2}O}} = 0,12 \hfill \\74x + 86y = {m_{este}} = 3,08 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}x = 0,03\,mol \hfill \\y = 0,01\,mol \hfill \\ \end{gathered} \right. \to \% {n_{{C_4}{H_6}{O_2}}} = \dfrac{{0,01}}{{0,01 + 0,03}} \cdot 100 = 25\%
Câu 11 :
Este X có các đặc điểm sau: - Đốt cháy hoàn toàn X tạo thành CO2 và H2O có số mol bằng nhau; - Thuỷ phân X trong môi trường kiềm được chất Y (tham gia phản ứng tráng gương) và chất Z (có số nguyên tử cacbon bằng một nửa số nguyên tử cacbon trong X). Phát biểu không đúng là:
Đáp án : C Phương pháp giải :
+) Đốt cháy X thu được: {n_{C{O_2}}} = {n_{{H_2}O}} → este no, đơn chức, mạch hở +) Y có khả năng tham gia phản ứng tráng gương → CTPT của Y +) X có số nguyên tử C bằng 1 nửa số nguyên tử C trong X → CTPT của Z => CTPT của X Lời giải chi tiết :
Este X khi đốt cháy thu được {n_{C{O_2}}} = {n_{{H_2}O}}→ este no, đơn chức, mạch hở Thủy phân X trong NaOH thu được muối Y có khả năng tham gia phản ứng tráng gương → Y là HCOONa Mặt khác X có số nguyên tử C bằng 1 nửa số nguyên tử C trong X → trong Z có số nguyên tử C bằng trong muối. → Z là C{H_3}OH \to X:\,HCOOC{H_3} \Leftrightarrow {C_2}{H_4}{O_2} {C_2}{H_4}{O_2} + 2{O_2}\xrightarrow{{{t^o}}}2C{O_2} + 2{H_2}O 1 2 2 C{H_3}OH\xrightarrow{{{H_2}S{O_4}_{(đ)},\,{{170}^o}C}}C{H_3}OC{H_3} + {H_2}O
Câu 12 :
Một hỗn hợp X gồm hai chất hữu cơ đơn chức. Cho X phản ứng vừa đủ với 500 ml dung dịch KOH 1M. Sau phản ứng, thu được hỗn hợp Y gồm hai muối của hai axit cacboxylic và một rượu (ancol). Cho toàn bộ lượng rượu thu được ở trên tác dụng với Na (dư), sinh ra 3,36 lít H2 (ở đktc). Hỗn hợp X gồm
Đáp án : A Phương pháp giải :
+) từ nH2 => tính nancol +) So sánh nancol với nKOH => kết luận chất trong X Lời giải chi tiết :
{n_{K{\text{O}}H}} = 0,5.1 = 0,5\,mol;\,{n_{{H_2}}} = \dfrac{{3,36}}{{22,4}} = 0,15\,mol ROH + Na \xrightarrow{{}} RONa + \dfrac{1}{2}H2 ↑ \to {n_{ancol}} = 2{n_{{H_2}}} = 0,3\,mol \to X:\left\{ \begin{gathered}1{\text{ }}axit \hfill \\1{\text{ }}este \hfill \\ \end{gathered} \right. (Thỏa mãn) RCOOR’ + KOH \xrightarrow{{}} RCOOK + R’OH R”COOH + KOH \xrightarrow{{}} R”COOK + H2O
Câu 13 :
Cho m gam hỗn hợp gồm hai chất hữu cơ đơn chức, mạch hở tác dụng vừa đủ với dung dịch chứa 11,2 gam KOH, thu được muối của một axit cacboxylic và một ancol X. Cho toàn bộ X tác dụng hết với Na thu được 3,36 lít khí H2 (ở đktc). Hai chất hữu cơ đó là
Đáp án : D Phương pháp giải :
+) từ nH2 => tính nancol +) So sánh nancol với nKOH => kết luận chất trong hỗn hợp đầu Lời giải chi tiết :
{n_{K{\text{O}}H}} = \dfrac{{11,2}}{{56}} = 0,2\,mol\,\,\,;\,\,\,\,{n_{{H_2}}} = \dfrac{{3,36}}{{22,4}} = 0,15\,mol ROH + Na \xrightarrow{{}} RONa + \dfrac{1}{2}H2 ↑ \to {n_{ancol}} = 2{n_{{H_2}}} = 0,3\,mol {n_{ancol}} > {n_{K{\text{O}}H}} mà hỗn hợp đầu tác dụng vừa đủ với KOH 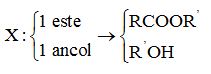 RCOOR’ + KOH \xrightarrow{{}} RCOOK + R’OH
Câu 14 :
Đốt cháy hoàn toàn 3,42 gam hỗn hợp gồm axit acrylic, vinyl axetat, metyl acrylat và axit oleic, rồi hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 (dư). Sau phản ứng thu được 18 gam kết tủa và dung dịch X. Khối lượng X so với khối lượng dung dịch Ca(OH)2 ban đầu đã thay đổi như thế nào?
Đáp án : B Phương pháp giải :
+) Các chất có công thức chung là CnH2n-2O2 +) viết PT đốt cháy => tính n +) \Delta m = {m_{C{O_2}}} + {m_{{H_2}O}}-{m_{CaC{O_3}}} Lời giải chi tiết :
Các chất có công thức chung là CnH2n-2O2 CnH2n-2O2 → nCO2 + (n – 1)H2O \dfrac{{3,42}}{{14n + 30}} 0,18 => n = 6 => nH2O = 0,15 mol \Delta m = {m_{C{O_2}}} + {m_{{H_2}O}}-{m_{CaC{O_3}}} = - 7,38 => giảm 7,38 gam
Câu 15 :
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY < MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a : b là
Đáp án : D Phương pháp giải :
+) nCO2 = nH2O => X no, đơn chức, mạch hở +) Bảo toàn O => nX +) Bảo toàn khối lượng => mX => MX +) Từ số mol X và khối lượng chất rắn => số mol mỗi muối Lời giải chi tiết :
{n_{{O_2}}} = 1,225\,mol;\,{n_{C{O_2}}} = 1,05\,mol;\,{n_{{H_2}O}} = 1,05\,mol => X no, đơn chức, mạch hở Bảo toàn O => nX = 0,35 mol Bảo toàn khối lượng => mX = 25,9 gam => MX = 74 => C3H6O2 => HCOOC2H5 (a mol) và CH3COOCH3 (b mol) nX = a + b = 0,35 mrắn = 68a + 82b + 0,05.40 = 27,9 => a = 0,2 và b = 0,15 => a : b = 4 : 3
Câu 16 :
Cho glixerin trioleat (hay triolein) lần lượt vào mỗi ống nghiệm chứa riêng biệt: Na, Cu(OH)2, CH3OH, dd Br2, dd NaOH. Trong điều kiện thích hợp, số pư xảy ra là
Đáp án : A Lời giải chi tiết :
{({C_{17}}{H_{33}}{\text{COO)}}_3}{C_3}{H_5} + B{r_2}\xrightarrow{{}}{({C_{17}}{H_{33}}B{r_2}COO)_3}{C_3}{H_5} {({C_{17}}{H_{33}}COO)_3}{C_3}{H_5} + 3NaOH\xrightarrow{{}}3{C_{17}}{H_{33}}COONa + {C_3}{H_5}{(OH)_3}
Câu 17 :
Thuỷ phân hoàn toàn 444 gam một lipit thu được 46 gam glixerol (glixerin) và hai loại axit béo. Hai loại axit béo đó là
Đáp án : C Phương pháp giải :
Phản ứng thủy phân tạo 2 axit béo → phương trình tổng quát dạng: {({R_1}COO)_2}{C_3}{H_5}{\text{(OOC}}{{\text{R}}_2}) + 3{H_2}O \to 2{R_1}COOH + {R_2}{\text{COOH}} + {C_3}{H_5}{(OH)_3} +) nlipit = nglixerol Lời giải chi tiết :
Phản ứng thủy phân tạo 2 axit béo → phương trình tổng quát dạng: {({R_1}COO)_2}{C_3}{H_5}{\text{(OOC}}{{\text{R}}_2}) + 3{H_2}O \to 2{R_1}COOH + {R_2}{\text{COOH}} + {C_3}{H_5}{(OH)_3} {n_{lipit}} = {n_{glixerol}} \to {n_{lipit}} = \dfrac{{46}}{{92}} = 0,5\,mol \to {M_{lipit}} = \dfrac{{444}}{{0,5}} = 888\,g/mol \to ({R_{^1}} + 44).2 + ({R_{^2}} + 44) + 41 = 888 \to 2{R_{^1}} + {R_{^2}} = 715 \to \left\{ \begin{gathered}{R_{^1}} = 239\,({C_{17}}{H_{35}}) \hfill \\{R_{^2}} = 237\,({C_{17}}{H_{33}}) \hfill \\ \end{gathered} \right. → C17H33COOH và C17H35COOH.
Câu 18 :
Xà phòng hoá hoàn toàn 17,24 gam chất béo cần vừa đủ 0,06 mol NaOH. Cô cạn dd sau pư thu được khối lượng xà phòng là
Đáp án : A Phương pháp giải :
Bảo toàn khối lượng: mxà phòng = mchất béo + mNaOH - mglixerol Lời giải chi tiết :
Ta có: {(RCOO)_3}{C_3}{H_5} + 3NaOH\xrightarrow{{}}3RCOONa + {C_3}{H_5}{(OH)_3} 0,02 ← 0,06 → 0,02 Bảo toàn khối lượng: mxà phòng = mchất béo + mNaOH - mglixerol = 17,24 + 0,06.40 - 0,02.92 = 17,8\,gam
Câu 19 :
Cho 200 gam một loại chất béo có chỉ số axit bằng 7 tác dụng vừa đủ với một lượng NaOH, thu được 207,55 gam hỗn hợp muối khan. Khối lượng NaOH đã tham gia phản ứng là
Đáp án : B Phương pháp giải :
+) Từ chỉ số axit => số mol NaOH phản ứng với axit béo RCOOH + NaOH\xrightarrow{{}}RCOONa + {H_2}O 0,025 0,025 {(RCOO)_3}{C_3}{H_5} + 3NaOH\xrightarrow{{}}3RCOONa + {C_3}{H_5}{(OH)_3} 3x x Bảo toàn khối lượng: mchất béo + maxit + mNaOH = mmuối + mglixrol => x => tổng số mol NaOH phản ứng Lời giải chi tiết :
Để trung hòa 200 gam chất béo có chỉ số axit bằng 7 {n_{NaOH}} = \,{n_{KOH}} = \dfrac{7}{{56}}.\dfrac{1}{{1000}}.200 = 0,025\,mol RCOOH + NaOH\xrightarrow{{}}RCOONa + {H_2}O 0,025 0,025 {(RCOO)_3}{C_3}{H_5} + 3NaOH\xrightarrow{{}}3RCOONa + {C_3}{H_5}{(OH)_3} 3x x Bảo toàn khối lượng: mchất béo + maxit + mNaOH = mmuối + mglixrol \to 200 + (0,025 + 3x).40 = 207,55 + 0,025.18 + x.92 \to x = 0,25 \to \sum {{n_{NaOH}}} = 0,025 + 3.0,25 = 0,775\,mol \to {m_{NaOH}} = 0,775.40 = 31\,gam
Câu 20 :
Hỗn hợp X gồm 3 este đơn chức, tạo thành từ cùng một ancol Y với 3 axit cacboxylic (phân tử chỉ có nhóm -COOH); trong đó, có hai axit no là đồng đẳng kế tiếp nhau và một axit không no (có đồng phân hình học, chứa một liên kết đôi C=C trong phân tử). Thủy phân hoàn toàn 5,88 gam X bằng dung dịch NaOH, thu được hỗn hợp muối và m gam ancol Y. Cho m gam Y vào bình đựng Na dư, sau phản ứng thu được 896 ml khí (đktc) và khối lượng bình tăng 2,48 gam. Mặt khác, nếu đốt cháy hoàn toàn 5,88 gam X thì thu được CO2 và 3,96 gam H2O. Phần trăm khối lượng của este không no trong X là
Đáp án : D Phương pháp giải :
+) nancol = 2.nH2 và mancol = mbình tăng + mH2 => Mancol => CTPT của ancol => CTTQ của các este trong X +) Đốt 5,88 gam X (ứng với 0,08 mol) + O2 \xrightarrow{{{t^o}}} ? mol CO2 + 0,22 mol H2O +) nO trong X = 2.nX và mX = mC + mH + mO => nC +) neste không no = \sum {n_{C{O_2}}} - \sum {n_{{H_2}O}} => n2 este no => \bar C => CTPT của 2 este no +) Vì este không no chứa ít nhất 4C, chặn khoảng giá trị số C của este không no +) Biện luận CTPT của este không no (dựa vào dữ kiện có đồng phân hình học) Lời giải chi tiết :
Ancol + Na dư → 0,04 mol H2 và mbình tăng = 2,48 gam => nancol = 2.nH2 = 0,08 mol và mancol = mbình tăng + mH2 = 2,56 gam => Mancol = 32 => ancol là CH3OH => X gồm 2 este no dạng CnH2n+1COOCH3 và 1 este không no dạng CmH2m-1COOCH3 (m ≥ 2) +) Đốt 5,88 gam X (ứng với 0,08 mol) + O2 \xrightarrow{{{t^o}}} ? mol CO2 + 0,22 mol H2O nO trong X = 2.nX = 0,16 mol và mX = mC + mH + mO => nC = 0,24 mol Tương quan đốt có neste không no = \sum {n_{C{O_2}}} - \sum {n_{{H_2}O}} = 0,02{\text{ }}mol => n2 este no = 0,06 mol \bar C = \dfrac{{0,24}}{{0,08}} = 3=> 2 este no là HCOOCH3 và CH3COOCH3 Vì este không no chứa ít nhất 4C, chặn khoảng giá trị số C của este không no: \(\dfrac{{0,24-0,06.3}}{{0,02}} = 3$ < số Ceste không no $ < 6 = \dfrac{{0,24-0,06.2}}{{0,02}}\) Tuy nhiên ứng với C4 có mỗi công thức CH2=CHCOOCH3 không có đồng phân hình học => loại => etse không no có 5C và cấu tạo có đồng phân hình học là: CH3CH=CHCOOCH3 =>\% {m_{{C_5}{H_8}{O_2}}}{\text{ = }}\dfrac{{0,02.100}}{{5,88}}{\text{.100% = }}34,01\%
Câu 21 :
Hỗn hợp X chứa ba este mạch hở, trong phân tử chỉ chứa một loại nhóm chức và được tạo bởi các axit cacboxylic có mạch không phân nhánh. Đốt cháy hết 0,2 mol X cần dùng 0,52 mol O2 thu được 0,48 mol H2O. Đun nóng 24,96 gam X cần dùng 560 ml dung dịch NaOH 0,75M thu được hỗn hợp Y chứa các ancol có tổng khối lượng là 13,38 gam và hỗn hợp Z gồm hai muối, trong đó có a gam muối A và b gam muối B (MA < MB). Tỉ lệ gần nhất a : b là
Đáp án : D Phương pháp giải :
+) Trong phản ứng xà phòng hóa: {n_X} = \dfrac{{24,96}}{{{M_X}}} mol và {n_{NaOH}} = 0,42 (mol) +) Tính tỉ lệ trong 0,2 mol X chứa ? mol O +) Bảo toàn O cho phản ứng cháy => {n_{C{O_2}}} +) Từ khối lượng este bị đốt cháy => lập PT tìm MX => số C trung bình trong X => 2 muối trong Z +) Gọi số mol mỗi muối trong Z là x, y +) Từ nNaOH => PT (1) +) Bảo toàn khối lượng => PT (2) Lời giải chi tiết :
Trong phản ứng xà phòng hóa: {n_X} = \dfrac{{24,96}}{{{M_X}}} mol và {n_{NaOH}} = 0,42 (mol) Ta có tỉ lệ: \dfrac{{24,96}}{{{M_X}}} mol X chứa nO = 2.nNaOH = 0,42.2 = 0,84 mol O => trong 0,2 mol X chứa nO = \dfrac{{7{M_X}}}{{1040}} mol O Bảo toàn O cho phản ứng cháy => {n_{C{O_2}}} = \dfrac{{7{M_X}}}{{2080}} + 0,28 Khối lượng este bị đốt cháy: 0,2{M_X} = 12.\left( {\dfrac{{7{M_X}}}{{2080}} + 0,28} \right) + 0,48.2 + \dfrac{{16.7{M_X}}}{{1040}} => MX = 83,2 => nCO2 = 0,56 => số C = 2,8 Vậy este X có số C = số O => 2 muối trong Z chỉ có thể là HCOONa (x mol) và (COONa)2 (y mol) nNaOH = x + 2y = 0,42 Bảo toàn khối lượng: mmuối = 68x + 134y = 0,09 => x = 0,24 và y = 0,09 => a : b = 1,353
Câu 22 :
Đốt cháy hoàn toàn m gam triglixerit X được CO2 và 18,72 gam H2O. Xà phòng hóa cũng lượng triglixerit X trên bằng lượng vừa đủ dung dịch NaOH rồi cô cạn được rắn khan Y. Đốt cháy hoàn toàn Y thu được Na2CO3, 44,44 gam CO2 và 17,82 gam H2O. Mặt khác m gam triglixerit X trên làm mất màu vừa đủ x mol Br2 trong dung dịch brom. Giá trị x là
Đáp án : C Phương pháp giải :
- Cần tính được số mol CO2, H2O khi đốt X và số mol của X - Xác định độ bất bão hòa của X dựa vào công thức: {n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} - Khi cho X phản ứng với Br2 thì: nBr2 = (k - 3).nX Lời giải chi tiết :
Bảo toàn H cho phản ứng đốt m (g) X → nH(X) = 2nH2O = 2,08 mol - Xét phản ứng thủy phân m gam X trong NaOH: Đặt nX = a mol \mathop X\limits_{a\left( {mol} \right)} + \mathop {NaOH}\limits_{3{\rm{a}}\left( {mol} \right)} \to \left\{ \begin{array}{l}Muối + {O_2} \to \left\{ \begin{array}{l}N{a_2}C{O_3}\\C{O_2}:1,01\\{H_2}O:0,99\end{array} \right.\\\mathop {{C_3}{H_5}{{\left( {OH} \right)}_3}}\limits_{a\left( {mol} \right)} \end{array} \right. Bảo toàn H → nH(X) + nNaOH = 2nH2O(đốt muối) + 8nC3H8O3 → 2,08 + 3a = 2.0,99 + 8a → a = 0,02 Bảo toàn Na → nNa2CO3 = 1/2.nNaOH = 0,03 mol Bảo toàn C → nC(X) = nNa2CO3(đốt muối) + nCO2(đốt muối) + 3nC3H5(OH)3 = 1,1 mol - Xét phản ứng đốt m (g) X: Bảo toàn C → nCO2(đốt X) = nC(X) = 1,1 mol Ta có: {n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} \Leftrightarrow 0,02 = \frac{{1,1 - 1,04}}{{k - 1}} \Leftrightarrow k = 4 ⟹ X có 1 π ở gốc hiđrocacbon (vì 3 nhóm COO chiếm 3 π) ⟹ nBr2 = nX = 0,02 mol
Câu 23 :
Chất béo X gồm các triglixerit và các axit béo tự do. Trung hòa lượng axit béo có trong 100 gam chất béo cần dùng 100 ml dung dịch KOH 0,1M. Mặt khác, thủy phân hoàn toàn 100 gam chất béo đó cần dùng 200 ml dung dịch NaOH 2M, đun nóng, sau phản ứng thu được m gam muối. Giá trị của m là
Đáp án : C Phương pháp giải :
Trung hòa axit trong 100 gam chất béo: naxit = nKOH Cho chất béo tác dụng với NaOH: RCOOH + NaOH → RCOONa + H2O (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3 ntriglixerit = (nNaOH - naxit)/3 nH2O = naxit nC3H5(OH)3 = ntriglixerit BTKL: mmuối = mchất béo + mNaOH - mH2O - mC3H5(OH)3 Lời giải chi tiết :
Trung hòa axit trong 100 gam chất béo: naxit = nKOH = 0,01 mol Cho chất béo tác dụng với NaOH: RCOOH + NaOH → RCOONa + H2O (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3 ntriglixerit = (nNaOH - naxit)/3 = (0,4 - 0,01)/3 = 0,13 mol nH2O = naxit = 0,01 mol nC3H5(OH)3 = ntriglixerit = 0,13 mol BTKL: mmuối = mchất béo + mNaOH - mH2O - mC3H5(OH)3 = 100 + 0,4.40 - 0,01.18 - 0,13.92 = 103,86 gam
Câu 24 :
Hỗn hợp X gồm axit oleic và triglixerit Y (tỉ lệ mol tương ứng 2 : 3). Đốt cháy hoàn toàn một lượng hỗn hợp X cần vừa đủ 2,82 mol O2, thu được 2,01 mol CO2 và 1,84 mol H2O. Mặt khác, cho 46,98 gam X trên tác dụng tối đa với x mol Br2 trong dung dịch. Giá trị của x là
Đáp án : A Phương pháp giải :
Khi đốt hợp chất hữu cơ bất kì (chứa C, H, O) có độ bất bão hòa k, ta luôn có: nCO2 - nH2O = nhchc.(k-1) Lời giải chi tiết :
BTKL → mX = mCO2 + mH2O - mO2 = 2,01.44 + 1,84.18 - 2,82.32 = 31,32 gam Đặt số mol của axit oleic và triglixerit lần lượt là 2a và 3a mol Bảo toàn O → 2.2a + 6.3a + 2.2,82 = 2.2,01 + 1,84 → a = 0,01 → naxit oleic = 0,02 mol; ntriglixerit = 0,03 mol *Khi đốt hợp chất hữu cơ bất kì (chứa C, H, O) có độ bất bão hòa k, ta luôn có: nCO2 - nH2O = nhchc.(k-1) - Đốt axit oleic (k = 2) thì: nCO2(do axit oleic) - nH2O(do axit oleic) = 0,02 (*) - Đốt triglixerit Y (k) thì: nCO2(do Y) - nH2O(do Y) = 0,03.(k - 1) (**) Cộng vế với vế của (*) và (**) được: ∑nCO2 - ∑nH2O = 0,02 + 0,03.(k - 1) → 2,01 - 1,84 = 0,02 + 0,03.(k - 1) → k = 6 *Khi cho hỗn hợp tác dụng với Br2 thì: nBr2 = naxit oleic + 3.ntriglixerit = 0,02 + 3.0,03 = 0,11 mol Tỷ lệ: 31,32 gam hỗn hợp X tác dụng với tối đa 0,11 mol Br2 → 46,98 gam ……………………………….0,165 mol Vậy x = 0,165
Câu 25 :
Đốt cháy hoàn toàn 0,08 mol một chất béo X cần dùng vừa đủ 6,36 mol O2. Mặt khác, cho lượng X trên vào dung dịch nước Br2 dư thấy có 0,32 mol Br2 tham gia phản ứng. Nếu cho lượng X trên tác dụng hết với NaOH thì khối lượng muối khan thu được là
Đáp án : A Phương pháp giải :
- Từ nBr2 : n chất béo => độ bất bão hòa k của chất béo -Áp dụng định luật bảo toàn nguyên tố và {n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} => Số mol CO2 và H2O - Bảo toàn khối lượng để tính khối lượng muối. Lời giải chi tiết :
Ta có nBr2 : nX = 0,32 : 0,08 = 4 nên các gốc hiđrocacbon của chất béo có tổng cộng 4π Mà mỗi gốc COO có 1π nên độ bất bão hòa của toàn phân tử X là k = 4 + 3 = 7 - Phản ứng đốt 0,08 mol X: Giả sử nCO2 = a và nH2O = b (mol) +) Bảo toàn O → 6nX + 2nO2 = 2nCO2 + nH2O → 2a + b = 6.0,08 + 2.6,36 (1) +) {n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} → \frac{{a - b}}{{7 - 1}} = 0,08 (2) Giải (1) (2) được a = 4,56 và b = 4,08 BTKL → mX = mCO2 + mH2O - mO2 = 4,56.44 + 4,08.18 - 6,36.32 = 70,56 gam Ta có X + 3NaOH → Muối + C3H5(OH)3 0,08 → 0,24 → 0,08 (mol) BTKL → mmuối = mX + mNaOH - mC3H5(OH)3 = 70,56 + 0,24.40 - 0,08.92 = 72,8 gam
Câu 26 :
Đốt cháy hoàn toàn m gam một triglixerit X cần vừa đủ x mol O2, sau phản ứng thu được CO2 và y mol H2O. Biết m = 78x - 103y. Nếu cho a mol X tác dụng với dung dịch Br2 dư thì lượng Br2 phản ứng tối đa là 0,45 mol. Giá trị của a là
Đáp án : B Phương pháp giải :
- Từ phản ứng cháy xác định độ bất bão hòa k của chất béo: + BTKL tính được CO2 (theo x, y) + Bảo toàn O tính được mol O trong X (theo x, y) → mol của X (theo x, y) + Lập biểu thức: {n_{hchc}} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} Loại bỏ x, y và tính được k. - Khi cho chất béo phản ứng với Br2 thì X + (k-3) Br2 → Sản phẩm Từ số mol của Br2 tính được số mol chất béo Lời giải chi tiết :
BTKL → mCO2 = mX + mO2 - mH2O = 110x - 121y (g) → nCO2 = 2,5x - 2,75y (mol) Bảo toàn O → nO(trong X) = 2nCO2 + nH2O - 2nO2 = 3x - 4,5y (mol) X có 6O → nX = 1/6.nO(trong X) = 0,5x - 0,75y (mol) Khi đốt hợp chất hữu cơ chứa C, H, O thì: {n_{hchc}} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} (với k là độ bất bão hòa của toàn phân tử) \begin{array}{l} \to 0,5{\rm{x}} - 0,75y = \frac{{\left( {2,5{\rm{x}} - 2,75y} \right) - y}}{{k - 1}}\\ \to \left( {0,5{\rm{x}} - 0,75y} \right) = \frac{{5\left( {0,5{\rm{x}} - 0,75y} \right)}}{{k - 1}}\\ \to 1 = \frac{5}{{k - 1}}\\ \to k = 6\end{array} => X có chứa 6 liên kết π, mà có 3 π trong 3 nhóm COO → còn lại 3 π ngoài gốc hiđrocacbon - Khi X phản ứng với Br2 thì X + 3Br2 → Sản phẩm cộng → nX = 1/3.nBr2 = 1/3.0,45 = 0,15 mol = a
Câu 27 :
Đốt cháy hoàn toàn 13,728 gam triglixerit X, thu được a mol hỗn hợp Y gồm CO2 và H2O. Cho toàn bộ hỗn hợp Y qua cacbon nung đỏ, thu được 2,364 mol hỗn hợp Z gồm CO, H2 và CO2. Cho hỗn hợp Z qua dung dịch Ba(OH)2 dư thu được 202,516 gam kết tủa. Cho 13,728 gam X tác dụng được tối đa với 0,032 mol Br2 trong dung dịch. Giá trị của m là
Đáp án : C Phương pháp giải :
- Tính số mol CO2 từ số mol kết tủa=> tổng số mol CO và H2 - Áp dụng bảo toàn electron =>nC => a. - Quy đổi hỗn hợp X thành (HCOO)3C3H5, CH2 và H2O - Lập phương trình khối lượng X (1) - Lập phương trình giá trị của a (2) - Từ (1) và (2) tìm ra số mol (HCOO)3C3H5 và CH2 - Tìm số mol NaOH và glixerol. - Bảo toàn khối lượng để tìm khối lượng muối Lời giải chi tiết :
Dẫn hỗn hợp Z qua dung dịch Ba(OH)2 dư thì {n_{C{O_2}}} = {n_{BaC{{\rm{O}}_3}}} = 1,028\,\,mol \to {n_{CO}} + {n_{{H_2}}} = 2,364 - 1,028 = 1,336 mol Xét quá trình trao đổi electron của phản ứng giữa C với CO2 và H2O C → C+4 + 4e C+4 + 2e → C+2 2H+ + 2e → H2 Áp dụng bảo toàn electron: 4{n_C} = 2{n_{CO}} + 2{n_{{H_2}}} \to {n_C} = \frac{{2.1,336}}{4} = 0,668\,\,mol → a = 2,364 – 0,668 = 1,696 mol Quy đổi hỗn hợp X thành (HCOO)3C3H5 (x mol), CH2 (y mol) và H2 (-0,032 mol) → mX = 176x + 14y – 0,032.2 = 13,728 (1) {n_{C{O_2}}} + {n_{{H_2}O}} = (6{\rm{x}} + y) + (4{\rm{x}} + y - 0,032) = 1,696(2) Từ (1) và (2) → x = 0,016 mol; y = 0,784 mol Ta có: nNaOH = 3x = 0,048 mol; {n_{{C_3}{H_5}{{(OH)}_3}}} = x = 0,016\,\,mol Áp dụng bảo toàn khối lượng cho phản ứng: mX + mNaOH = mmuối + mglixerol → mmuối = 13,728 + 0,048.40 – 92.0,016 = 14,176 gam
Câu 28 :
Hiđro hóa hoàn toàn 26,52 gam triolein cần vừa đủ V lít khí H2 (đktc). Giá trị của V là:
Đáp án : C Phương pháp giải :
Tính toán theo PTHH: (C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5 Lời giải chi tiết :
(C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5 → nH2 = 3ntriolein = 3.26,52 : 884 = 0,09 mol → VH2 = 0,09.22,4 = 2,016 lít
Câu 29 :
Đốt cháy hoàn toàn 4,03 gam triglixerit X bằng một lượng oxi vừa đủ, cho toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng nước vôi trong dư thu được 25,5 gam kết tủa và khối lượng dung dịch thu được giảm 9,87 gam so với khối lượng nước vôi trong ban đầu. Mặt khác khi thủy phân hoàn toàn 8,06 gam X trong dung dịch NaOH dư đun nóng thu được dung dịch chứa a gam muối. Giá trị của a là
Đáp án : D Phương pháp giải :
Bảo toàn nguyên tố C → nCO2 Lập phương trình mdd giảm → mH2O BTKL → mO2 → bảo toàn O → nO(X) → nX = 1/6 .nO(X) → số mol của 8,06 g X BTKL mmuối = mX + mNaOH – mC3H5(OH)3 Lời giải chi tiết :
Ta có nCaCO3 = nCO2 = 0,255 mol mdd giảm = - mCO2 - mH2O + mCaCO3 = - 0,255.44 – mH2O + 25,5 = 9,87 → mH2O = 4,41 gam → nH2O = 0,245 mol BTKL có mO2 = mCO2 + mH2O – mX = 0,255.44 + 4,41 – 4,03 = 11,6 g → nO2= 0,3625 mol Bảo toàn O có 2nO2 + nO(X) = 2nCO2 + nH2O → nO(X) = 0,03 mol Vì X là triglixerit nên nX = 1/6 .nO(X) = 0,005 mol → 8,06 g X có số mol là 0,005.8,06 : 4,03 = 0,01 mol 0,01 mol X + 0,03 mol NaOH → muối + 0,01 mol C3H5(OH)3 BTKL mmuối = mX + mNaOH – mC3H5(OH)3 = 8,06 + 0,03.40 – 0,01.92 = 8,34 gam
Câu 30 :
Đốt cháy hoàn toàn 13,728 gam một triglixerit X cần vừa đủ 27,776 lít O2 (đktc) thu được số mol CO2 và số mol H2O hơn kém nhau 0,064. Mặt khác, hiđro hóa hoàn toàn một lượng X cần 0,096 mol H2 thu được m gam chất hữu cơ Y. Xà phòng hóa hoàn toàn m gam Y bằng dung dịch NaOH thu được dung dịch chứa a gam muối. Giá trị của a là
Đáp án : B Phương pháp giải :
Đặt nCO2 = x (mol); nH2O = y (mol) => x, y Bảo toàn O → nX → MX Lập CTPT của X theo nCO2 và nH2O → số liên kết ∏ của X → tỉ lệ của X với H2 phản ứng X + 0,096 mol H2 → Y → nX =nY → mX →mY Y + 3NaOH → a gam muối + C3H5(OH)3 → BTKL : mmuối Lời giải chi tiết :
X + O2 → x mol CO2 + y mol H2O nO2 = 1,24 mol mX + mO2 = mCO2 + mH2O → 13,728 + 1,24.32 = 44x + 18y (1) Mà x – y = 0,064 mol => x = 0,88 mol và y = 0,816 mol Bảo toàn O có nO(X) + 2nO2 = 2nCO2 + nH2O → nO(X) = 2.0,88 + 0,816 – 2.1,24 =0,096 mol Vì X là triglixerit nên nO(X) = 6nX → nX = 0,016 mol Ta có nX = (nCO2 - nH2O)/(k -1) => k = 5 → X cộng tối đa với 2H2 → no X + 0,096 mol H2 → Y => nX = 0,048 mol → mX =41,184 gam →mY = 41,184 + 0,096.2 =41,376 gam nY =nX =0,048 mol Y + 3NaOH → a gam muối + C3H5(OH)3 nNaOH = 3nY = 0,048.3 =0,144 mol và nC3H5(OH)3 = 0,048 mol → BTKL : mmuối = mY + mNaOH – mC3H5(OH)3 = 41,376 + 0,144.40 – 0,048.92 = 42,72 gam
Câu 31 :
Cho m gam triolein tác dụng hoàn toàn với H2 dư thu được (m + 0,3) gam chất X. Nếu cho toàn bộ X tác dụng với dung dịch KOH dư, đun nóng thu được a gam muối. Giá trị của a là
Đáp án : C Phương pháp giải :
Tính toán theo phương trình phản ứng. Bảo toàn khối lượng. Lời giải chi tiết :
Triolein + H2 theo tỉ lệ 1:3 Bảo toàn khối lượng: mTriolein + mH2 pứ = mX => mH2 pứ = (m + 0,3) – m = 0,3g => nH2 = 0,3 : 2 = 0,15 mol => ntristearin = nH2 : 3 = 0,05 mol Khi X + NaOH: (C17H35COO)3C3H5 + 3KOH → 3C17H35COOK + C3H5(OH)3 Mol 0,05 → 0,15 mol => mmuối = 0,15.322 = 48,3g
Câu 32 :
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2 thu được 6,384 lít CO2 và 4,77 g H2O. Mặt khác m gam X phản ứng vừa đủ với x gam Brom (trong dung môi CCl4). Biết thể tích các khí đo ở đktc. Giá trị của x là:
Đáp án : A Phương pháp giải :
- Bảo toàn nguyên tố O: nO(X) + 2nO2 = 2nCO2 + nH2O => nO(X) => nX - Mặt khác: (k – 1).nX = (nCO2 – nH2O) => k => số mol Br2 => x Lời giải chi tiết :
- Gọi công thức của X là (RCOO)3C3H5 có k liên kết pi nO2 = 9,016 : 22,4 = 0,4025 mol ; nCO2 = 6,384 : 22,4 = 0,285 mol ; nH2O = 0,265 mol Bảo toàn nguyên tố O: nO(X) + 2nO2 = 2nCO2 + nH2O => nO(X) = 0,03 mol = 6n(X) => nX = 0,005 mol Mặt khác: (k – 1).nX = (nCO2 – nH2O) => k = 5 Có 3 pi trong 3 gốc COO => 2 pi còn lại sẽ nằm trong gốc hidrocacbon (Có thể phản ứng được với Br2/CCl4) => nBr2 = 2.nX = 2.0,005 = 0,01 mol => mBr2 = x = 0,01.160 = 1,6g
Câu 33 :
X là trieste tạo bởi glixerol và các axit cacboxylic đơn chức. X có các đặc điểm: - Trong X số nguyên tử cacbon nhiều hơn số nguyên tử oxi là 3. - Đốt cháy hoàn toàn x mol X thu được y mol CO2 và z mol H2O với y - z = 3x. - X có đồng phân hình học cis - trans. Nhận xét nào sau đây là sai?
Đáp án : B Phương pháp giải :
- X là trieste tạo bởi glixerol và các axit cacboxylic đơn chức nên có 6O - Số C nhiều hơn số O là 3 nên X có 9C - Khi đốt hợp chất hữu cơ (chứa C, H, O) có độ bất bão hòa k ta có: {n_{hchc}} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} \to k = 4 ⟹ X có 1 liên kết C=C Mà X có đồng phân hình học nên X là (HCOO)2(CH3-CH=CH-COO)C3H5 Lời giải chi tiết :
- X là trieste tạo bởi glixerol và các axit cacboxylic đơn chức nên có 6O - Số C nhiều hơn số O là 3 nên X có 9C - Khi đốt hợp chất hữu cơ (chứa C, H, O) có độ bất bão hòa k ta có: {n_{hchc}} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} \Leftrightarrow x = \frac{{y - z}}{{k - 1}} \Leftrightarrow x = \frac{{3{\rm{x}}}}{{k - 1}} \Leftrightarrow k = 4 ⟹ X có 1 liên kết C=C Mà X có đồng phân hình học nên X là (HCOO)2(CH3-CH=CH-COO)C3H5 A đúng, 2 CTCT đó là:
B sai, X có 12 nguyên tử H C đúng, nX = 16,2 / 216 = 0,075 = nglixerol ⟹ mglixerol = 0,075.92 = 6,9 gam D đúng, vì X có đầu HCOO- nên có khả năng tráng bạc
Câu 34 :
Hỗn hợp X gồm hai đieste (có tỉ lệ mol 1 : 1 và có cùng công thức phân tử C10H10O4) đều chứa vòng benzen. Khi xà phòng hoá hoàn toàn 38,8 gam X bằng dung dịch NaOH vừa đủ, thu được hỗn hợp Y gồm hai ancol có số nguyên tử cacbon bằng nhau và dung dịch Z. Cô cạn dung dịch Z thu được m gam chất rắn gồm các hợp chất hữu cơ. Giá trị của m là
Đáp án : B Phương pháp giải :
k = \frac{{2C + 2 - H}}{2} = 6 ⟹ 2 este đều no (vì có 2π trong 2 nhóm COO và vòng benzen có độ bất bão hòa 4) Do sau phản ứng thu được 2 ancol có cùng số nguyên tử C nên 2 ancol đó là C2H5OH và C2H4(OH)2 ⟹ CTCT của 2 este trong X Sau đó tính toán theo các PTHH Lời giải chi tiết :
k = \frac{{2C + 2 - H}}{2} = 6 ⟹ 2 este đều no (vì có 2π trong 2 nhóm COO và vòng benzen có độ bất bão hòa 4) Do sau phản ứng thu được 2 ancol có cùng số nguyên tử C nên 2 ancol đó là C2H5OH và C2H4(OH)2 ⟹ CTCT của 2 este trong X là:
Ta có nA = nB = ½.nhh X = ½.(38,8 : 194) = 0,1 mol C2H5OOC-COOC6H5 + 3NaOH → (COONa)2 + C6H5ONa + C2H5OH + H2O 0,1 → 0,1 → 0,1 C6H5COO-CH2-CH2-OOCH + 2NaOH → C6H5COONa + HCOONa + C2H4(OH)2 0,1 → 0,1 → 0,1 Chất rắn trong Z gồm: \left\{ {\begin{array}{*{20}{l}}{{{\left( {COONa} \right)}_2}:0,1}\\{{C_6}{H_5}ONa:0,1}\\{{C_6}{H_5}COONa:0,1}\\{HCOONa:0,1}\end{array}} \right. → m = mchất rắn = 0,1.134 + 0,1.116 + 0,1.144 + 0,1.68 = 46,2 gam
Câu 35 :
Cho sơ đồ các phản ứng theo đúng tỉ lệ mol: X (C18H12O12) + 6NaOH → X1 + 3X2. X1 + 6HCl → X3 + 6NaCl. X3 + C2H5OH → X4 + H2O Biết khi đốt cháy hoàn toàn X1 chỉ tạo ra sản phẩm chứa Na2CO3 và CO2. Phân tử khối của X4 là
Đáp án : D Phương pháp giải :
Đốt cháy X1 chỉ thu được Na2CO3 và CO2 nên X1 chứa C, O và Na trong phân tử X1 pư với HCl theo tỉ lệ 1:6 nên X1 có 6 trung tâm phản ứng với HCl → X là este 6 chức → CTCT của X Chú ý: este vòng Lời giải chi tiết :
Đốt cháy X1 chỉ thu được Na2CO3 và CO2 nên X1 chứa C, O và Na trong phân tử X1 pư với HCl theo tỉ lệ 1:6 nên X1 có 6 trung tâm phản ứng với HCl → X là este 6 chức → CTCT của X C6[(COO)2C2H4]3 Công thức cấu tạo của X1 là:
X3 là axit C6(COOH)6 (6 gốc –COOH gắn vào 6 đỉnh của vòng benzen) X2 là C2H4(OH)2 X4 là C6(COOH)5(COOC2H5) → Phân tử khối của X4 = 370
Câu 36 :
Phát biểu nào sau đây sai?
Đáp án : A Phương pháp giải :
Dựa vào tính chất vật lí, tính chất hóa học và công thức chung của chất béo, este để chọn phát biểu sai. Lời giải chi tiết :
Phát biểu A sai vì sản phẩm của phản ứng xà phòng hoá chất béo là muối của axit béo và glixerol. Phát biểu B đúng vì ancol có liên kết hidro nên có nhiệt độ sôi cao hơn rất nhiều este có cùng phân tử khối. Phát biểu C đúng vì trong công nghiệp có thể chuyển hoá chất béo lỏng thành chất béo rắn bằng phản ứng hiđro hóa. Phát biểu D đúng vì công thức chung của este là CnH2n+2-2kO2m nên số nguyên tử hiđro trong phân tử este đơn và đa chức luôn là một số chẵn.
Câu 37 :
Thủy phân hoàn toàn triglixerit X trong dung dịch NaOH dư, đun nóng, sinh ra glixerol và hỗn hợp 2 muối gồm natri oleat và natri stearat. Đốt cháy hoàn toàn m gam X cần vừa đủ 1,61 mol O2, thu được H2O và 1,14 mol CO2. Phát biểu nào sau đây đúng?
Đáp án : C Phương pháp giải :
Bảo toàn nguyên tố Lời giải chi tiết :
- Vì sản phẩm chứa 2 muối của axit có 18C => Số C của X = 18.3 + 3 = 57 => D sai - X là este của axit oleic và stearic => X tác dụng H2 (dư, Ni, t0) tạo ra tristearin, không phải là triolein => A sai - Do X chứa 57 nguyên tử C => nX = nCO2 : 57 = 1,14 : 57 = 0,02 mol BTNT "O": nH2O = 6nX + 2nO2 - 2nCO2 = 6.0,02 + 2.1,61 - 2.1,14 = 1,06 mol BTKL: mX = mCO2 + mH2O - mO2 = 1,14.44 + 1,06.18 - 1,61.32 = 17,72 gam => C đúng - Giả sử chất béo là: (C17H33COO)n(C17H35COO)3-nC3H5 => m chất béo = 0,02.[281n + 283(3-n) + 41] = 17,72 => n = 2 => X chứa 2 gốc oleat => X chứa 2 liên kết C=C => B sai
Câu 38 :
Cho các sơ đồ phản ứng theo đúng tỉ lệ mol: (a) X + 3H2O \underset{{{t^o}}}{\overset{{{H_2}S{O_4}}}{\longleftrightarrow}} X1 + X2 + X3 + X4 (b) X1 + 2H2 \xrightarrow{{Ni,{t^o}}} X2 Cho biết: X là triglixerit có số liên kết π nhỏ hơn 6 và có 55 nguyên tử cacbon trong phân tử; X1, X2, X3, X4 là những hợp chất hữu cơ khác nhau, X2 nhiều hơn X3 hai nhóm CH2. Nhận định nào sau đây không đúng?
Đáp án : D Lời giải chi tiết :
- X1, X2, X3 là axit. - Từ (b) suy ra X2 là axit no. X2 nhiều hơn X3 2 nhóm CH2 nên X3 cũng là axit no - X1 có thể cộng tối đa 2H2 nên phân tử X1 chứa 2 liên kết π ở ngoài mạch hidrocacbon Mà số liên kết π trong X nhỏ hơn 6 nên suy ra phân tử X chứa 3π trong 3 nhóm COO và 2π ngoài mạch hidrocacbon => Hệ số bất bão hòa k = 5 Đặt: Số C(X1) = Số C(X2) = n => Số C(X3) = n - 2 Số C(X) = Số C(X1) + Số C(X2) + Số C(X3) + 3 => n + n + (n - 2) + 3 = 55 => n = 18 Kết luận: X1 là C17H31COOH X2 là C17H35COOH X3 là C15H31COOH X là C55H102O6 X4 là C3H5(OH)3 Xét các phương án: A. %mH(X3) = 32/256.100% = 12,5% => A đúng B đúng C đúng D. %mC(X1) = (18.12/280).100% = 77,14% => D sai
|