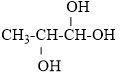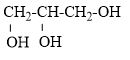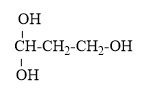Đề khảo sát chất lượng đầu năm Hóa 12 - Đề số 2Đề bài
Câu 1 :
Cho CH3CHO phản ứng với H2 (xt Ni, nung nóng) thu được
Câu 2 :
Theo A-rê-ni-ut, chất nào sau đây là axit ?
Câu 3 :
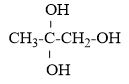
Chất X có CTCT như hình bên. X có tên gọi 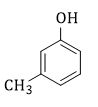
Câu 4 :
Oxit nào sau đây không tạo muối?
Câu 5 :
Dung dịch X có chứa a mol Na+, b mol Mg2+, c mol Cl- và d mol SO42-. Biểu thức nào sau đây đúng:
Câu 6 :
Những kim loại nào sau đây không tác dụng được với dung dịch HNO3 đặc, nguội
Câu 7 :
Cho phản ứng NaOH + HCl → NaCl + H2O. Phản ứng hóa học nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
Câu 8 :
Khi số nguyên tử C trong phân tử của các axit thuộc dãy đồng đẳng của axit fomic tăng lên thì tính axit của chúng
Câu 9 :
Trong các nhận xét dưới đây, nhận xét nào sai ?
Câu 10 :
Khi cho axetilen vào dung dịch AgNO3 trong NH3 dư, hiện tượng quan sát được là
Câu 11 :
Chọn định nghĩa đúng về axit no, đơn chức
Câu 12 :
Phản ứng nào sau đây dùng để điều chế CO trong phòng thí nghiệm
Câu 13 :
HNO3 chỉ thể hiện tính oxi hóa khi tác dụng với các chất thuộc dãy nào dưới đây?
Câu 14 :
Đốt cháy hoàn toàn một lượng ancol A thu được số mol nước gấp đôi số mol CO2. Tên gọi của A là
Câu 15 :
Cho propen, propin, đivinyl tác dụng với HCl (tỉ lệ 1 : 1), số sản phẩm thu được lần lượt là
Câu 16 :
Hợp chất hữu cơ X có công thức phân tử dạng CnH2n+2. X thuộc dãy đồng đẳng của
Câu 17 :
Chất nào sau đây ở thể khí ở nhiệt độ thường ?
Câu 18 :
Ancol no, mạch hở, đơn chức có công thức tổng quát là
Câu 19 :
Axit panmitic là axit nào sau đây ?
Câu 20 :
Từ 1 lít hỗn hợp CO và CO2 có thể điều chế tối đa bao nhiêu lít CO2? (H = 100%)
Câu 21 :
Tên gọi của anđehit có khối lượng phân tử nhỏ nhất là
Câu 22 :
Công thức đơn giản nhất của một axit no, đa chức là (C3H4O3)n. Công thức cấu tạo thu gọn của axit đó là
Câu 23 :
Anken X có công thức cấu tạo: CH3–CH2–C(CH3)=CH–CH3. Tên của X là
Câu 24 :
Nitơ có nhiều trong khoáng vật diêm tiêu, diêm tiêu có thành phần chính là
Câu 25 :
Hợp chất C5H10 mạch hở có bao nhiêu đồng phân cấu tạo ?
Câu 26 :
Hợp chất hữu cơ có CTTQ là CnH2n+2Om có thể thuộc loại hợp chất nào sau đây:
Câu 27 :
Cho sơ đồ phản ứng : FeS2 + HNO3 → Fe(NO3)3 + H2SO4 + NO + H2O Sau khi cân bằng, hệ số cân bằng của HNO3 trong phản ứng là :
Câu 28 :
Công thức cấu tạo của ancol C3H5(OH)3 là
Câu 29 :
Cho etin phản ứng với dung dịch brom dư thu được sản phẩm là
Câu 30 :
Tính pH của 300ml dung dịch (gồm 100 ml Ba(OH)2 0,1M và 200 ml NaOH 0,05M)
Câu 31 :
Đốt cháy a mol axit X đơn chức được x mol CO2 và y mol H2O. Biết rằng x – y = a. Công thức tổng quát của X là
Câu 32 :
Cho các chất có CTCT như sau: HOCH2-CH2OH (X); HOCH2-CH2-CH2-OH (Y); HOCH2-CH(OH)-CH2OH (Z); CH3-CH2-O-CH2-CH3 (R); CH3-CH(OH)-CH2OH (T). Những chất tác dụng được với Cu(OH)2 tạo thành dung dịch màu xanh lam là
Câu 33 :
Trong các cặp chất cho dưới đây, cặp nào không xảy ra phản ứng với nhau?
Câu 34 :
Cho N (Z = 7). Cấu hình electron của Nitơ là?
Câu 35 :
Axit HNO3 là một axit
Câu 36 :
Đem nung một lượng Cu(NO3)2 sau một thời gian thì dừng lại làm nguội rồi cân thấy khối lượng giảm 0,54 gam. Khối lượng muối đã bị nhiệt phân là
Câu 37 :
Dung dịch X chứa a mol NaHCO3 và b mol Na2CO3. Thực hiện các thí ngiệm sau TN1: cho (a + b) mol CaCl2 vào dd X TN2: cho (a + b) mol Ca(OH)2 vào dd X Khối lượng kết tủa thu được trong 2 TN là
Câu 38 :
Khi cho một hỗn hợp gồm 2 axit (A đơn chức, B hai chức đều no, mạch hở) có khối lượng là 16,4 gam tác dụng với Na vừa đủ, sau phản ứng thu được 3,36 lít khí H2. Lượng muối thu được là
Câu 39 :
Propan-1-ol có công thức cấu tạo là
Câu 40 :
Cho 11,2 lít CO2 (đktc) hấp thụ hết trong dung dịch chứa a mol Ca(OH)2 và 0,2 mol NaOH. Xác định giá trị của a để sau phản ứng thu được 10 gam kết tủa:
Câu 41 :
Cho các chất sau: 2-metylbut-1-en (1); 3,3-đimetylbut-1-en (2); 3-metylpent-1-en (3); 3-metylpent-2-en (4). Những chất nào là đồng phân của nhau ?
Câu 42 :
Thêm 25 ml dung dịch NaOH 2M vào 100 ml dung dịch H2SO4. Đem dung dịch thu được cho tác dụng với dung dịch NaHCO3 dư thu được 5,6 lít CO2 (đktc). Nồng độ mol/lít của dung dịch H2SO4 ban đầu là:
Câu 43 :
Cho 0,01 mol phenol tác dụng hoàn toàn với lượng dư dung dịch hỗn hợp HNO3 đặc và H2SO4 đặc. Phát biểu nào sau đây không đúng
Câu 44 :
Cho 0,001 mol NH4Cl vào 100 ml dung dịch NaOH có pH = 12 và đun sôi, sau đó làm nguội, thêm vào một ít phenolphtalein, dung dịch thu được có màu
Câu 45 :
Hỗn hợp X gồm 2 ankin có tỷ lệ mol 1: 3. Đốt cháy hoàn toàn hỗn hợp X sau đó cho toàn bộ sản phẩm cháy vào nước vôi trong dư thấy khối lượng bình nước vôi trong tăng 10,96 gam và trong bình có 20 gam kết tủa. Vậy công thức của 2 ankin là:
Câu 46 :
Ankan 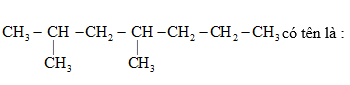
Câu 47 :
Cho 0,1 mol anđehit đơn chức, mạch hở X phản ứng đủ với 0,3 mol AgNO3 trong dung dịch NH3, thu được 43,6 gam kết tủa. Mặt khác, hiđro hóa hoàn toàn 4 gam X cần a mol H2. Giá trị của a là:
Câu 48 :
Dung dịch Y chứa 0,02 mol Mg2+; 0,03 mol Na+; 0,03 mol Cl- và y mol SO42-. Giá trị của y là
Câu 49 :
Tiến hành 2 thí nghiệm sau TN1: cho 6 gam ancol mạch hở, đơn chức A tác dụng với m gam Na thu được 0,075 gam H2 TN2: cho 6 gam A tác dụng với 2m gam Na thu được không tới 0,1 gam H2. A có công thức là
Câu 50 :
Nhiệt phân hoàn toàn hỗn hợp BaCO3, MgCO3, Al2O3 được rắn X và khí Y. Hoà tan rắn X vào nước thu được kết tủa E và dung dịch Z. Sục khí Y dư vào dung dịch Z thấy xuất hiện kết tủa F, hoà tan E vào dung dịch NaOH dư thấy tan một phần được dung dịch G. Các chất trong dung dịch G và kết tủa F là
Lời giải và đáp án
Câu 1 :
Cho CH3CHO phản ứng với H2 (xt Ni, nung nóng) thu được
Đáp án : C Phương pháp giải :
Xem lại lí thuyết phản ứng cộng của anđehit Lời giải chi tiết :
CH3CHO + H2 $\xrightarrow{Ni,{{t}^{o}}}$ CH3CH2OH
Câu 2 :
Theo A-rê-ni-ut, chất nào sau đây là axit ?
Đáp án : B Lời giải chi tiết :
Theo A-rê-ni-ut, axit là chất phân li ra H+ => HCl là axit
Câu 3 :
Chất X có CTCT như hình bên. X có tên gọi 
Đáp án : D Lời giải chi tiết :
Đánh số từ nhóm OH => tên gọi: 3-metylphenol
Câu 4 :
Oxit nào sau đây không tạo muối?
Đáp án : C Lời giải chi tiết :
CO là một oxit trung tính nên không có khả năng tạo muối.
Câu 5 :
Dung dịch X có chứa a mol Na+, b mol Mg2+, c mol Cl- và d mol SO42-. Biểu thức nào sau đây đúng:
Đáp án : B Phương pháp giải :
Áp dụng định luật bảo toàn điện tích: ∑n(+) = ∑n(-) Lời giải chi tiết :
Áp dụng định luật bảo toàn điện tích cho dung dịch X ta có:
=> a + 2b = c + 2d
Câu 6 :
Những kim loại nào sau đây không tác dụng được với dung dịch HNO3 đặc, nguội
Đáp án : A Phương pháp giải :
Ghi nhớ một số KL bị thụ động với HNO3 đặc nguội như Al, Fe, Cr Lời giải chi tiết :
Al, Fe là những kim loại bị thụ động với HNO3 đặc nguội
Câu 7 :
Cho phản ứng NaOH + HCl → NaCl + H2O. Phản ứng hóa học nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
Đáp án : C Phương pháp giải :
Nắm được cách chuyển đổi từ phương trình phân tử sang phương trình ion rút gọn Lời giải chi tiết :
Phương trình ion rút gọn của phản ứng NaOH + HCl → NaCl + H2O là: OH- + H+ → H2O A. 2OH- + Fe2+ → Fe(OH)2 B. OH- + NH4+ → NH3 + H2O C. OH- + H+ → H2O D. OH- + HCO3- → CO32- + H2O
Câu 8 :
Khi số nguyên tử C trong phân tử của các axit thuộc dãy đồng đẳng của axit fomic tăng lên thì tính axit của chúng
Đáp án : C Lời giải chi tiết :
Khi số nguyên tử C trong phân tử của các axit thuộc dãy đồng đẳng của axit fomic tăng lên thì tính axit của chúng giảm đi.
Câu 9 :
Trong các nhận xét dưới đây, nhận xét nào sai ?
Đáp án : D Lời giải chi tiết :
Nhận xét sai là: Tất cả các chất chỉ có liên kết đơn trong phân tử đều là ankan. Ví dụ như chất CH3 – O – CH3 đều chỉ có các liên kết đơn nhưng không phải là ankan.
Câu 10 :
Khi cho axetilen vào dung dịch AgNO3 trong NH3 dư, hiện tượng quan sát được là
Đáp án : D Lời giải chi tiết :
Cho axetilen vào dung dịch AgNO3 : CH≡CH + 2AgNO3 + 2NH3 → CAg≡CAg ↓vàng nhạt + 2NH4NO3 => phản ứng tạo kết tủa vàng nhạt
Câu 11 :
Chọn định nghĩa đúng về axit no, đơn chức
Đáp án : A Lời giải chi tiết :
Định nghĩa đúng về axit no, đơn chức là : Axit no, đơn chức là những hợp chất hữu cơ mà phân tử có một nhóm chức cacboxyl liên kết với gốc hiđrocacbon no.
Câu 12 :
Phản ứng nào sau đây dùng để điều chế CO trong phòng thí nghiệm
Đáp án : C Lời giải chi tiết :
Phản ứng dùng để điều chế CO trong phòng thí nghiệm là HCOOH$\xrightarrow{{{H}_{2}}S{{O}_{4}},{{t}^{0}}}$ CO + H2O
Câu 13 :
HNO3 chỉ thể hiện tính oxi hóa khi tác dụng với các chất thuộc dãy nào dưới đây?
Đáp án : A Phương pháp giải :
HNO3 thể hiện tính oxi hóa khi phản ứng với các chất khử (chất có khả năng tăng số oxi hóa) Lời giải chi tiết :
A đúng B loại CuO, CaCO3 C loại CaO D loại Fe2O3
Câu 14 :
Đốt cháy hoàn toàn một lượng ancol A thu được số mol nước gấp đôi số mol CO2. Tên gọi của A là
Đáp án : B Phương pháp giải :
Nếu đốt cháy ancol cho nH2O > 1,5.nCO2 thì ancol là CH3OH. Chỉ có CH4 và CH3OH có tính chất này (không kể amin) Lời giải chi tiết :
nH2O > 1,5.nCO2 => ancol đốt cháy là CH3OH
Câu 15 :
Cho propen, propin, đivinyl tác dụng với HCl (tỉ lệ 1 : 1), số sản phẩm thu được lần lượt là
Đáp án : B Phương pháp giải :
Xem lại lí thuyết phản ứng cộng ankin, cộng anken và ankađien Lời giải chi tiết :
Propen: CH2=CH-CH3 + HCl → CH3-CHCl-CH3 + CH2Cl-CH2-CH3 Propin: CH≡C-CH3 + HCl → CH2=CCl-CH3 + CHCl=CH-CH3 (có đphh) => propin thu được 3 sản phẩm Đivinyl: CH2=CH-CH=CH2 có 2 kiểu cộng 1,2 và cộng 1,4 (xem lại lí thuyết ankađien) CH2=CH-CH=CH2 + HCl → CH2=CH-CH2-CH2Cl + CH2=CH-CHCl-CH3 CH2=CH-CH=CH2 + HCl → CH3-CH=CH-CHCl (có đphh) => đivinyl thu được 4 sản phẩm
Câu 16 :
Hợp chất hữu cơ X có công thức phân tử dạng CnH2n+2. X thuộc dãy đồng đẳng của
Đáp án : B Lời giải chi tiết :
X thuộc dãy đồng đẳng của ankan.
Câu 17 :
Chất nào sau đây ở thể khí ở nhiệt độ thường ?
Đáp án : B Lời giải chi tiết :
- Ở điều kiện thường, các axit cacboxylic đều là những chất lỏng hoặc rắn. - HCHO là những chất khí tan tốt trong nước - CH3OH và C2H5HO là những chất lỏng
Câu 18 :
Ancol no, mạch hở, đơn chức có công thức tổng quát là
Đáp án : C Lời giải chi tiết :
Ancol no, mạch hở, đơn chức có công thức tổng quát là CnH2n+2O (n ≥ 1)
Câu 19 :
Axit panmitic là axit nào sau đây ?
Đáp án : A Lời giải chi tiết :
Axit panmitic có CTPT là C15H31COOH.
Câu 20 :
Từ 1 lít hỗn hợp CO và CO2 có thể điều chế tối đa bao nhiêu lít CO2? (H = 100%)
Đáp án : A Phương pháp giải :
Bảo toàn nguyên tố C. Lời giải chi tiết :
Bảo toàn nguyên tố C ta có: nCO2 thu được = nCO + nCO2 bđ Hay V CO2 thu được = VCO + VCO2 bđ = 1 lít
Câu 21 :
Tên gọi của anđehit có khối lượng phân tử nhỏ nhất là
Đáp án : B Lời giải chi tiết :
Anđehit có khối lượng phân tử nhỏ nhất là HCHO => tên gọi: metanal
Câu 22 :
Công thức đơn giản nhất của một axit no, đa chức là (C3H4O3)n. Công thức cấu tạo thu gọn của axit đó là
Đáp án : C Lời giải chi tiết :
CTPT: C3nH4nO3n Với n = 1 => C3H4O3 loại vì số O lẻ (axit cacboxylic không chứa tạp chức có số O chẵn) Với n = 2 => C6H8O6 => CTCT: C3H5(COOH)3 phù hợp đáp án C Với n = 3 => C9H12O9 loại vì số O lẻ và số C lớn không có đáp án phù hợp
Câu 23 :
Anken X có công thức cấu tạo: CH3–CH2–C(CH3)=CH–CH3. Tên của X là
Đáp án : C Lời giải chi tiết :
- Đánh số C từ vị trí gần nối đôi hơn $\mathop C\limits^5 {H_3}-\mathop C\limits^4 {H_2}-\mathop C\limits^3 \left( {C{H_3}} \right) = \mathop C\limits^2 H-\mathop C\limits^1 {H_3}$ - Gọi tên: 3-metylpent-2-en
Câu 24 :
Nitơ có nhiều trong khoáng vật diêm tiêu, diêm tiêu có thành phần chính là
Đáp án : C Lời giải chi tiết :
Nitơ có nhiều trong khoáng vật diêm tiêu, diêm tiêu có thành phần chính là: NaNO3
Câu 25 :
Hợp chất C5H10 mạch hở có bao nhiêu đồng phân cấu tạo ?
Đáp án : B Lời giải chi tiết :
Đề bài hỏi đồng phân cấu tạo => không đếm đồng phân hình học 1. CH2=CH-CH2-CH2-CH3 2. CH3-CH=CH-CH2-CH3 3. CH2=C(CH3)-CH2-CH3 4. (CH3)2C=CH-CH3 5. (CH3)2CH-CH=CH2
Câu 26 :
Hợp chất hữu cơ có CTTQ là CnH2n+2Om có thể thuộc loại hợp chất nào sau đây:
Đáp án : C Lời giải chi tiết :
Hợp chất hữu cơ có CTTQ là CnH2n+2Om có thể thuộc loại hợp chất ancol no, mạch hở, m chức và ete no, mạch hở, m chức.
Câu 27 :
Cho sơ đồ phản ứng : FeS2 + HNO3 → Fe(NO3)3 + H2SO4 + NO + H2O Sau khi cân bằng, hệ số cân bằng của HNO3 trong phản ứng là :
Đáp án : D Phương pháp giải :
+) Coi Fe và S trogn 1 chất có tổng số oxi hóa là 0 +) Xác định các nguyên tố có số oxi hóa thay đổi +) Viết quá trình cho - nhận e => xác định hệ số cân bằng Lời giải chi tiết :
Coi Fe và S ban đầu có trong chất có số oxi hóa là 0 $\begin{align}& {{\overset{0}{\mathop{FeS}}\,}_{2}}+\text{ }H\overset{+5}{\mathop{N}}\,{{O}_{3}}\xrightarrow{{}}\overset{+3}{\mathop{Fe}}\,{{\left( N{{O}_{3}} \right)}_{3}}+\text{ }{{H}_{2}}\overset{+6}{\mathop{S}}\,{{O}_{4}}+\text{ }\overset{+2}{\mathop{N}}\,O\text{ }+\text{ }{{H}_{2}}O \\ & \,\,1.|{{\overset{0}{\mathop{FeS}}\,}_{2}}\to \,\,\overset{+3}{\mathop{Fe}}\,\,\,+\,\,2\overset{+6}{\mathop{S}}\,\,\,+\,\,15e \\ & 5.|\overset{+5}{\mathop{N}}\,\,+\,\,3e\,\,\to \,\,\overset{+2}{\mathop{N}}\, \\ \end{align}$ => PTHH: FeS2 + 8HNO3 → Fe(NO3)3 + 2H2SO4 + 5NO + 2H2O => hệ số của HNO3 là 8
Câu 28 :
Công thức cấu tạo của ancol C3H5(OH)3 là
Đáp án : C Phương pháp giải :
Điều kiện bền của ancol: + nhóm -OH đính vào C no + chỉ có 1 nhóm -OH đính vào 1 cacbon Lời giải chi tiết :
Vì ancol có 3 nhóm OH mà mỗi nhóm OH chỉ đúng vào 1C => mỗi nguyên tử C có 1 nhóm OH
Câu 29 :
Cho etin phản ứng với dung dịch brom dư thu được sản phẩm là
Đáp án : B Lời giải chi tiết :
CH≡CH + 2Br2 → CHBr2 – CHBr2
Câu 30 :
Tính pH của 300ml dung dịch (gồm 100 ml Ba(OH)2 0,1M và 200 ml NaOH 0,05M)
Đáp án : B Phương pháp giải :
Từ số mol của Ba(OH)2 và NaOH \( \to {n_{O{H^ - }}} = 2{n_{Ba{{(OH)}_2}}} + {n_{NaOH}}\) \( \to {\text{[}}O{H^ - }{\text{] = }}\dfrac{{{n_{O{H^ - }}}}}{{0,3}}\) Mà [OH-].[H+] = 10-14 \( \to [{H^ + }] \to pH\) Lời giải chi tiết :
\({n_{Ba{{(OH)}_2}}} = 0,1.0,1 = 0,01\,\,mol;{n_{NaOH}} = 0,2.0,05 = 0,01\,\,mol\) \( \to {n_{OH - }} = 2{n_{Ba{{(OH)}_2}}} + {n_{NaOH}} = 2.0,01 + 0,01 = 0,03\,\,mol\) \( \to [O{H^ - }] = \dfrac{{0,03}}{{0,3}} = 0,1\,\,M\) Mà [OH-].[H+] = 10-14 \( \to [{H^ + }] = \dfrac{{{{10}^{ - 14}}}}{{0,1}} = {10^{ - 13}}\) \( \to pH = - \log {10^{ - 13}} = 13\)
Câu 31 :
Đốt cháy a mol axit X đơn chức được x mol CO2 và y mol H2O. Biết rằng x – y = a. Công thức tổng quát của X là
Đáp án : B Phương pháp giải :
Xem lại lí thuyết phản ứng đốt cháy axit cacboxylic Lời giải chi tiết :
Vì naxit = nCO2 – nH2O => trong CTPT của X có 2 liên kết pi => X no, 2 chức hoặc X có 1 nối đôi C=C và 1 chức –COOH
Câu 32 :
Cho các chất có CTCT như sau: HOCH2-CH2OH (X); HOCH2-CH2-CH2-OH (Y); HOCH2-CH(OH)-CH2OH (Z); CH3-CH2-O-CH2-CH3 (R); CH3-CH(OH)-CH2OH (T). Những chất tác dụng được với Cu(OH)2 tạo thành dung dịch màu xanh lam là
Đáp án : B Lời giải chi tiết :
Những chất tấc dụng với dd Cu(OH)2 tạo thành dung dịch màu xanh lam là những ancol có nhóm –OH liền kề HOCH2-CH2OH (X); HOCH2-CH(OH)-CH2OH (Z); CH3-CH(OH)-CH2OH (T)
Câu 33 :
Trong các cặp chất cho dưới đây, cặp nào không xảy ra phản ứng với nhau?
Đáp án : B Phương pháp giải :
Điều kiện xảy ra phản ứng trao đổi: Phản ứng trao đổi xảy ra khi thỏa mãn ít nhất 1 trong 3 điều kiện sau: 1. Tạo chất khí 2. Tạo kết tủa 3. Tạo chất điện li yếu Lời giải chi tiết :
A. Có phản ứng vì tạo chất điện li yếu (H2O). B. Không phản ứng vì không thỏa mãn 3 điều kiện của phản ứng trao đổi. C. Có phản ứng vì tạo kết tủa (AgCl). D. Có phản ứng vì tạo được kết tủa BaSO4.
Câu 34 :
Cho N (Z = 7). Cấu hình electron của Nitơ là?
Đáp án : C Lời giải chi tiết :
Nito có cấu hình e là: 1s22s22p3
Câu 35 :
Axit HNO3 là một axit
Đáp án : B Lời giải chi tiết :
Axit HNO3 là một axit mạnh
Câu 36 :
Đem nung một lượng Cu(NO3)2 sau một thời gian thì dừng lại làm nguội rồi cân thấy khối lượng giảm 0,54 gam. Khối lượng muối đã bị nhiệt phân là
Đáp án : D Phương pháp giải :
+) Gọi số mol Cu(NO3)2 là x => tính số mol các khí theo x +) mgiảm = mkhí sinh ra = mNO2 + mO2 => tính x Lời giải chi tiết :
2Cu(NO3)2 $\xrightarrow{{{t}^{o}}}$ 2CuO + 4NO2 + O2 x → x → 2x → 0,5x mgiảm = mkhí sinh ra = mNO2 + mO2 => 2x.46 + 0,5x.32 = 0,54 => x = 0,005 mol => mCu(NO3)2 = 0,94 gam
Câu 37 :
Dung dịch X chứa a mol NaHCO3 và b mol Na2CO3. Thực hiện các thí ngiệm sau TN1: cho (a + b) mol CaCl2 vào dd X TN2: cho (a + b) mol Ca(OH)2 vào dd X Khối lượng kết tủa thu được trong 2 TN là
Đáp án : B Phương pháp giải :
TN1: chỉ có Na2CO3 phản ứng: nCaCO3 = nNa2CO3 TN2: cả 2 chất đều phản ứng NaHCO3 + Ca(OH)2 → CaCO3 ↓ + NaOH + H2O Na2CO3 + Ca(OH)2 → CaCO3 ↓ + 2NaOH Lời giải chi tiết :
TN1: chỉ có Na2CO3 phản ứng: nCaCO3 = nNa2CO3 = b mol TN2: cả 2 chất đều phản ứng NaHCO3 + Ca(OH)2 → CaCO3 ↓ + NaOH + H2O a → a → a Na2CO3 + Ca(OH)2 → CaCO3 ↓ + 2NaOH b → b → b => ở TN2 thu được kết tủa nhiều hơn ở TN1
Câu 38 :
Khi cho một hỗn hợp gồm 2 axit (A đơn chức, B hai chức đều no, mạch hở) có khối lượng là 16,4 gam tác dụng với Na vừa đủ, sau phản ứng thu được 3,36 lít khí H2. Lượng muối thu được là
Đáp án : C Phương pháp giải :
+) nNa = 2.nH2 = 0,3 mol +) tăng giảm khối lượng: mmuối = maxit + 22.0,3 Lời giải chi tiết :
PTTQ: R(COOH)x + xNa → R(COONa)x + x/2 H2 => nNa = 2.nH2 = 0,3 mol Sử dụng tăng giảm khối lượng: mmuối = maxit + 22.0,3 = 23 gam
Câu 39 :
Propan-1-ol có công thức cấu tạo là
Đáp án : C Lời giải chi tiết :
Propan-1-ol có công thức cấu tạo là CH3-CH2-CH2OH
Câu 40 :
Cho 11,2 lít CO2 (đktc) hấp thụ hết trong dung dịch chứa a mol Ca(OH)2 và 0,2 mol NaOH. Xác định giá trị của a để sau phản ứng thu được 10 gam kết tủa:
Đáp án : C Phương pháp giải :
TH1: thu được 1 muối CO32- => nCa2+ = nCaCO3 Kiểm tra lại: nOH- = 2.nCa(OH)2 + nNaOH Mà thu được muối CO32- thì nOH- \( \ge \) 2.nCO2 => 0,4\( \ge \) 2.0,5 (vô lí) => loại trường hợp này TH2: thu được 2 muối HCO3- và CO32- +) Sử dụng công thức tính nhanh: \({n_{CO_3^{2 - }}} = {n_{O{H^ - }}} - {n_{C{O_2}}}\) Lời giải chi tiết :
nCO2 = 0,5 mol; nCaCO3 = 0,1 mol TH1: thu được 1 muối CO32- => nCa2+ = nCaCO3 = 0,1 mol => a = 0,1 Kiểm tra lại: nOH- = 2.nCa(OH)2 + nNaOH = 2.0,1 + 0,2 = 0,4 mol Mà thu được muối CO32- thì nOH- \( \ge \) 2.nCO2 => 0,4\( \ge \) 2.0,5 (vô lí) => loại trường hợp này TH2: thu được 2 muối HCO3- và CO32- Sử dụng công thức tính nhanh: \({n_{CO_3^{2 - }}} = {n_{O{H^ - }}} - {n_{C{O_2}}}\)=> 2a + 0,2 – 0,5 = 0,1 => a = 0,2 mol
Câu 41 :
Cho các chất sau: 2-metylbut-1-en (1); 3,3-đimetylbut-1-en (2); 3-metylpent-1-en (3); 3-metylpent-2-en (4). Những chất nào là đồng phân của nhau ?
Đáp án : D Lời giải chi tiết :
2-metylbut-1-en (1) => có 5C và 1 nối đôi => CTPT: C5H10 3,3-đimetylbut-1-en (2) => có 6C và 1 nối đôi => CTPT: C6H12 3-metylpent-1-en (3) => có 6C và 1 nối đôi => CTPT: C6H12 3-metylpent-2-en (4) => có 6C và 1 nối đôi => CTPT: C6H12 => những chất là đồng phân của nhau là: (2), (3) và (4)
Câu 42 :
Thêm 25 ml dung dịch NaOH 2M vào 100 ml dung dịch H2SO4. Đem dung dịch thu được cho tác dụng với dung dịch NaHCO3 dư thu được 5,6 lít CO2 (đktc). Nồng độ mol/lít của dung dịch H2SO4 ban đầu là:
Đáp án : A Phương pháp giải :
+) Dung dịch thu được tác dụng với NaHCO3 sinh khí CO2 => H+ dư sau phản ứng +) nH2SO4 ban đầu = nH2SO4 phản ứng với NaOH + nH2SO4 dư Lời giải chi tiết :
nNaOH = 0,05 mol Dung dịch thu được tác dụng với NaHCO3 sinh khí CO2 => H+ dư sau phản ứng 2NaHCO3 + H2SO4 → Na2SO4 + 2H2O + 2CO2 0,125 ← 0,25 2NaOH + H2SO4 → Na2SO4 + 2H2O 0,05 → 0,025 => nH2SO4 ban đầu = nH2SO4 phản ứng với NaOH + nH2SO4 dư = 0,025 + 0,125 = 0,15 mol => CM = 0,15 / 0,1 = 1,5M
Câu 43 :
Cho 0,01 mol phenol tác dụng hoàn toàn với lượng dư dung dịch hỗn hợp HNO3 đặc và H2SO4 đặc. Phát biểu nào sau đây không đúng
Đáp án : A Phương pháp giải :
Tính theo PTHH Lời giải chi tiết :
C6H5OH + 3HNO3 → C6H2(O2N)3OH + 3H2O 0,01 → 0,03 → 0,01 → maxit picric = 2,29 gam → A sai
Câu 44 :
Cho 0,001 mol NH4Cl vào 100 ml dung dịch NaOH có pH = 12 và đun sôi, sau đó làm nguội, thêm vào một ít phenolphtalein, dung dịch thu được có màu
Đáp án : D Phương pháp giải :
Tính toán theo PTHH: NH4Cl + NaOH → NaCl + NH3 + H2O + Dung dịch sau phản ứng có môi trường kiềm thì phenolphtalein chuyển màu hồng + Dung dịch sau phản ứng có môi trường axit hoặc trung tính thì phenolphtalein không đổi màu Lời giải chi tiết :
pOH = 14 – pH = 2 => CM NaOH = (OH-) = 0,01M nNaOH = 0,1.0,01 = 0,001 mol PTHH: NH4Cl + NaOH → NaCl + NH3 + H2O Pư: 0,001 0,001 Do phản ứng vừa đủ nên sau khi đun sôi thì NH3 bay hơi hết, dung dịch thu được chỉ còn lại NaCl có môi trường trung tính nên không làm đổi màu dung dịch phenolphtalein
Câu 45 :
Hỗn hợp X gồm 2 ankin có tỷ lệ mol 1: 3. Đốt cháy hoàn toàn hỗn hợp X sau đó cho toàn bộ sản phẩm cháy vào nước vôi trong dư thấy khối lượng bình nước vôi trong tăng 10,96 gam và trong bình có 20 gam kết tủa. Vậy công thức của 2 ankin là:
Đáp án : C Phương pháp giải :
+) mbình tăng = mCO2 + mH2O +) nankin = nCO2 – nH2O +) số C trung bình = nCO2 / nankin => trong X có C2H2 Vì hỗn hợp X gồm 2 ankin có tỉ lệ 1 : 3 => xét 2 TH TH1: nC2H2 = 0,02 mol => nCnH2n-2 = 0,06 mol TH2: nC2H2 = 0,06 mol; nCnH2n-2 = 0,02 mol Lời giải chi tiết :
nCaCO3 = 0,2 mol => nCO2 = nCaCO3 = 0,2 mol mbình tăng = mCO2 + mH2O = 10,96 gam => mH2O = 10,96 – 0,2.44 = 2,16 gam => nH2O = 0,12 mol => nankin = nCO2 – nH2O = 0,2 – 0,12 = 0,08 mol => số C trung bình = nCO2 / nankin = 0,2 / 0,08 = 2,5 => trong X có C2H2. Gọi ankin còn lại là CnH2n-2 Hỗn hợp X gồm 2 ankin có tỷ lệ mol 1: 3 TH1: nC2H2 = 0,02 mol => nCnH2n-2 = 0,06 mol => Bảo toàn C: 0,02.2 + 0,06n = 0,2 => n = 2,67 (loại) TH2: nC2H2 = 0,06 mol; nCnH2n-2 = 0,02 mol => Bảo toàn C: 0,06.2 + 0,02n = 0,2 => n = 4 => ankin còn lại là C4H6
Câu 46 :
Ankan 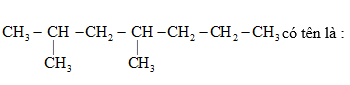
Đáp án : B Phương pháp giải :
Xem lại lí thuyết ankan Lời giải chi tiết :
- Đánh số vị trí C sao cho tổng số mạch nhánh là nhỏ nhất: 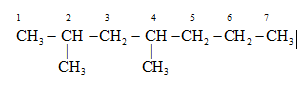 => tên của X là: 2,4-đimetylheptan
Câu 47 :
Cho 0,1 mol anđehit đơn chức, mạch hở X phản ứng đủ với 0,3 mol AgNO3 trong dung dịch NH3, thu được 43,6 gam kết tủa. Mặt khác, hiđro hóa hoàn toàn 4 gam X cần a mol H2. Giá trị của a là:
Đáp án : C Phương pháp giải :
X đơn chức nhưng nAg = 3nX => X có nhóm CH≡C – đầu mạch +) Kết tủa gồm : CAg≡C-RCOONH4 : 0,1 mol và 0,2 mol Ag => X là CH≡C – CH = CH – CHO (có tổng là 4π) +) nH2 = 4nX = 0,2 mol Lời giải chi tiết :
X đơn chức nhưng nAg = 3nX => X có nhóm CH≡C – đầu mạch => Kết tủa gồm : CAg≡C-RCOONH4 : 0,1 mol và 0,2 mol Ag => mkết tủa = 0,1.(R + 194) + 0,2.108 = 43,6 => R = 26 (C2H2) => X là CH≡C – CH = CH – CHO (có tổng là 4π) =>Thí nghiệm 2 : nX= 0,05 mol => nH2 = 4nX = 0,2 mol
Câu 48 :
Dung dịch Y chứa 0,02 mol Mg2+; 0,03 mol Na+; 0,03 mol Cl- và y mol SO42-. Giá trị của y là
Đáp án : D Phương pháp giải :
Bảo toàn điện tích. Lời giải chi tiết :
Áp dụng định luật bảo toàn điện tích ta có: 2nMg2+ + nNa+ = nCl- + 2nSO42- => 0,02.2 + 0,03.1 = 0,03.1 + 2y => y = 0,02
Câu 49 :
Tiến hành 2 thí nghiệm sau TN1: cho 6 gam ancol mạch hở, đơn chức A tác dụng với m gam Na thu được 0,075 gam H2 TN2: cho 6 gam A tác dụng với 2m gam Na thu được không tới 0,1 gam H2. A có công thức là
Đáp án : D Phương pháp giải :
X tác dụng với m gam Na tạo 0,075 gam H2 mà 2m gam Na tạo không tới 0,1 gam H2 → TN1 Na hết, ancol dư, TN2 ancol hết, Na dư Lời giải chi tiết :
X tác dụng với m gam Na tạo 0,075 gam H2 mà 2m gam Na tạo không tới 0,1 gam H2 → TN1 Na hết, ancol dư, TN2 ancol hết, Na dư TN2: ${n_{{H_2}}}$<$\frac{{0,1}}{2}$ = 0,05 mol → nancol < 0,05.2 = 0,1 mol → M >$\frac{6}{{0,1}}$ = 60 TN1: ${n_{{H_2}}}$> $\frac{{0,075}}{2}$= 0,0375 → nancol > 0,075 → M < 80 → 60 < 14n + 2 < 80 → 3 < n < 4,43 → n = 4 → ancol là C4H9OH
Câu 50 :
Nhiệt phân hoàn toàn hỗn hợp BaCO3, MgCO3, Al2O3 được rắn X và khí Y. Hoà tan rắn X vào nước thu được kết tủa E và dung dịch Z. Sục khí Y dư vào dung dịch Z thấy xuất hiện kết tủa F, hoà tan E vào dung dịch NaOH dư thấy tan một phần được dung dịch G. Các chất trong dung dịch G và kết tủa F là
Đáp án : B Phương pháp giải :
Dựa vào các phản ứng hóa học => xác định sản phẩm sau phản ứng Lời giải chi tiết :
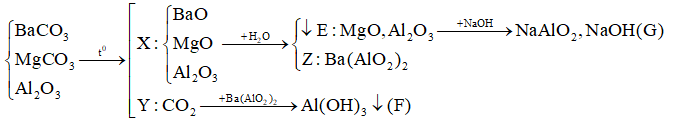 (Vì E tan 1 phần trong kiềm => trong E chứa Al2O3 còn dư => dung dịch Z không còn Ba(OH)2 |