Đề số 2 - Đề kiểm tra giữa học kì II - Hóa học 12 có đáp án và lời giải chi tiếtĐề số 2 - Đề kiểm tra giữa học kì II - Hóa học 12 có đáp án và lời giải chi tiết Đề bài Câu 1 : Tripeptit là hợp chất A. mà mỗi phân tử có 3 liên kết peptit. B. có liên kết peptit mà phân tử có 3 gốc amino axit giống nhau. C. có liên kết peptit mà phân tử có 3 gốc amino axit khác nhau. D. có 2 liên kết peptit mà phân tử có 3 gốc α-amino axit. Câu 2 : Loại dầu nào sau đây không phải là este của axit béo và glixerol? A. Dầu luyn. B. Dầu lạc (đậu phộng). C. Dầu dừa. D. Dầu vừng (mè). Câu 3 : Tên gọi amin nào sau đây là không đúng? A. C6H5NH2 là alanin. B. CH3CH2CH2NH2 là n-propylamin. C. CH3CH(CH3)NH2 là isopropylamin. D. CH3NHCH3 là đimetylamin. Câu 4 : Phát biểu nào sau đây về tính chất vật lí của amin là không đúng? A. Độ tan trong nước của amin giảm dần khi số nguyên tử cacbon trong phân tử tăng. B. Anilin là chất lỏng khó tan trong nước, màu đen. C. Các amin khí có mùi tương tự amoniac, độc. D. Metylamin, đimetylamin, etylamin là chất khí, dễ tan trong nước. Câu 5 : Glucozo không có tính chất nào dưới đây? A. Tính chất của poliancol. B. Lên men tạo ancol etylic. C. Tính chất của nhóm andehit. D. Tham gia phản ứng thủy phân. Câu 6 : Khi thủy phân trilinolein trong môi trường axit ta thu được sản phẩm là A. C17H31COOH và glixerol. B. C15H31COOH và glixerol. C. C17H35COOH. D. C15H31COOH và etanol. Câu 7 : Tính chất của chất béo được liệt kê như sau: (1) chất lỏng; (2) chất rắn; (3) nhẹ hơn nước; (4) tan trong nước; (5) tan trong xăng; (6) dễ bị thủy phân trong môi trường kiềm hoặc axit; (7) tác dụng với kim loại kiềm giải phóng; (8) dễ cộng vào gốc axit. Số tính chất đúng với mọi loại chất béo là A. 4. B. 3. C. 1. D. 2. Câu 8 : Nhỏ dung dịch iot lên miếng chuối xanh thấy xuất hiện màu xanh tím là do chuối xanh có chứa A. glucozo. B. saccarozo. C. tinh bột. D. xenlulozo. Câu 9 : Chất nào sau đây có phản ứng tráng gương? A. Tinh bột. B. Saccarozo. C. Xenlulozo. D. Glucozo. Câu 10 : Este etyl fomat có công thức là A. HCOOC2H5. B. HCOOCH3. C. HCOOCH=CH2. D. CH3COOCH3. Câu 11 : Amino axit nào sau đây có hai nhóm amino? A. Lysin. B. Valin. C. Axit glutamic. D. Alanin. Câu 12 : Cho các chất: Glucozo (X); Saccarozo (Y); Tinh bột (Z); Glixerol (T); Xenlulozo (H). Những chất có phản ứng thủy phân là A. Y, Z, H. B. X, Y, Z. C. X, Z, H. D. Y, T, H. Câu 13 : Cho chất hữu cơ X có công thức phân tử C2H8O3N2 tác dụng với dung dịch NaOH, thu được chất hữu cơ đơn chức Y và các chất vô cơ. Khối lượng phân tử (theo đvC) của Y là A. 68. B. 46. C. 45. D. 85. Câu 14 : Phân tích este X người ta thu được kết quả: %mC = 40% và %mH = 6,66%. Ngoài ra, từ thực nghiệm người ta xác định được X là este đơn chức. Este X là A. metyl axetat. B. etyl propionat. C. metyl fomat. D. metyl acrylat. Câu 15 : Nguyên nhân amin có tính bazo là A. có khả năng nhường proton. B. phản ứng được với dung dịch axit. C. trên nguyên tử N còn một đôi electron tự do có khả năng nhận H+. D. xuất phát từ amoniac. Câu 16 : Cặp chất nào sau đây không phải là đồng phân của nhau? A. Tinh bột và xenlulozo B. Fructozo và glucozo C. Metyl fomat và axit axetic D. Mantozo và saccarozo Câu 17 : Chọn phát biểu đúng trong các phát biểu dưới đây? A. Xenlulozơ có cấu trúc mạch phân nhánh. B. Glucozơ bị khử bởi dung dịch AgNO3/NH3 đun nóng. C. Amilozơ có cấu trúc mạch không phân nhánh. D. Saccarozơ có phản ứng tráng gương. Câu 18 : Khi nói về peptit và protein, phát biểu nào sau đây là sai? A. Protein có phản ứng màu biure với Cu(OH)2. B. Thủy phân hoàn toàn protein đơn giản thu được các α-amino axit. C. Liên kết của nhóm CO với nhóm NH giữa hai đơn vị α-amino axit được gọi là liên kết peptit. D. Tất cả các protein đều tan trong nước tạo thành dung dịch keo. Câu 19 : Số đồng phân của hợp chất este đơn chức có công thức phân tử C4H8O2 tác dụng với dung dịch AgNO3/NH3 sinh ra Ag là A. 4. B. 1. C. 2. D. 3. Câu 20 : Cho dãy chuyển hóa: \(C{{H}_{4}}\xrightarrow{{{1500}^{o}}C}X\xrightarrow{{{H}_{2}}O}Y\xrightarrow{{{H}_{2}}}Z\xrightarrow{{{O}_{2}}}T\xrightarrow{{{C}_{2}}{{H}_{{}}}_{2}}M\). Công thức của M là A. CH3COOCH3. B. CH2=CHCOOCH3. C. CH3COOC2H5. D. CH3COOCH=CH2. Câu 21 : Thuốc thử được dùng để phân biệt Gly-Ala-Gly với Gly-Ala là A. Cu(OH)2. B. Dung dịch HCl. C. Dung dịch NaOH. D. Dung dịch NaCl. Câu 22 : Axit X + 2H2 \(\xrightarrow{Ni,{{t}^{o}}}\) Axit Y. Tên gọi của axit X và Y lần lượt là A. Axit oleic và axit stearic. B. Axit linoleic và axit stearic. C. Axit panmitic; axit oleic. D. Axit linoleic và axit oleic. Câu 23 : Cacbohidrat Z tham gia chuyển hóa: Z \(\xrightarrow{Cu{{(OH)}_{2}}/O{{H}^{-}}}\)dung dịch xanh lam \(\xrightarrow{{{t}^{o}}}\) kết tủa đỏ gạch. Vậy Z không thể là chất nào trong các chất cho dưới đây? A. Saccarozo. B. Glucozo. C. Mantozo. D. Fructozo. Câu 24 : Cho các chất sau: X1: C6H5NH2; X2: CH3NH2; X3: H2NCH2COOH; X4: HOOCCH2CH2CH(NH2)COOH; X5: H2NCH2CH2CH2CH(NH2)COOH. Các dung dịch làm quỳ tím hóa xanh là A. X2, X3, X4. B. X2, X5. C. X1, X3, X5. D. X1, X2, X5. Câu 25 : Chất X có công thức phân tử C3H6O2, là este của axit axetic. Công thức cấu tạo thu gọn của X là: A. HCOOC2H5. B. HOC2H4CHO. C. C2H5COOH. D. CH3COOCH3. Câu 26 : Đốt cháy m gam hỗn hợp gồm 2 amin no đơn chức mạch hở thu được 28,6 gam CO2 và 18,45 gam H2O. Giá trị của m là A. 12,65 gam. B. 11,95 gam. C. 13 gam. D. 13,35 gam. Câu 27 : Tính thể tích dung dịch HNO3 96% (D = 1,52 g/ml) cần dùng để tác dụng với lượng dư xenlulozo tạo 29,7 kg xenlulozo trinitrat. A. 15,00 lít. B. 1,439 lít. C. 24,39 lít. D. 12,952 lít. Câu 28 : Để đốt cháy hết 1,62 gam hỗn hợp hai este no, đơn chức, mạch hở, đồng đẳng kế tiếp cần vừa đủ 1,904 lít oxi (đktc). Công thức phân tử của 2 este là A. C4H8O2 và C5H10O2. B. C2H4O2 và C3H6O2. C. C4H8O2 và C3H6O2. D. C2H4O2 và C5H10O2. Câu 29 : Hợp chất hữu cơ X có công thức C2H8N2O4. Khi cho 12,4 gam X tác dụng với 200 ml dung dịch NaOH 1,5M thu được 4,48 lít (đktc) khí Y làm xanh quỳ tím ẩm. Cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan. Giá trị của m là A. 13,4. B. 17,4. C. 17,2. D. 16,2. Câu 30 : Lấy 14,6 gam một đipeptit X tạo ra từ glyxin và alanin cho tác dụng vừa đủ với dung dịch HCl 1M. Thể tích dung dịch HCl tham gia phản ứng là A. 0,23 lít. B. 0,2 lít. C. 0,4 lít. D. 0,1 lít. Câu 31 : Khi thủy phân 486 kg bột gạo có 80% tinh bột (còn lại là tạp chất trơ). Nếu hiệu suất của quá trình sản xuất là 75%, khối lượng glucozơ tạo thành là A. 432 kg. B. 324 kg. C. 405 kg. D. 648 kg. Câu 32 : Chất hữu cơ X có công thức phân tử tác dụng với dung dịch NaOH (đun nóng) theo phương trình phản ứng: C4H6O4 + 2NaOH → 2Z + Y Để oxi hóa hết a mol Y thì cần vừa đủ 2a mol CuO (đung nóng), sau phản ứng tạo thành a mol chất T (biết Y, Z, T là các hợp chất hữu cơ). Khối lượng phân tử của T là: A. 118 đvC. B. 44 đvC. C. 58 đvC. D. 82 đvC. Câu 33 : Lên men m gam tinh bột thành ancol etylic với hiệu suất của cả quá trình là 60%. Lượng CO2 sinh ra được hấp thụ hoàn toàn vào dung dịch Ca(OH)2, thu được 30 gam kết tủa và dung dịch X. Thêm dung dịch KOH 1M vào X, thu được kết tủa. Để lượng kết tủa thu được là lớn nhất thì cần tối thiểu 100 ml dung dịch KOH. Giá trị của m là A. 54,0. B. 40,5. C. 67,5. D. 47,25. Câu 34 : Cho 23 gam C2H5OH tác dụng với 24 gam CH3COOH (xúc tác H2SO4 với hiệu suất phản ứng 60%. Khối lượng este thu được là: A. 23,76 gam. B. 26,4 gam. C. 21,12 gam. D. 22 gam. Câu 35 : Đốt cháy hoàn toàn 14,8 gam este X thu được 13,44 lít CO2 (đktc) và 10,8 gam H2O. CTPT của X là: A. C2H4O2. B. C4H8O2. C. C5H10O2. D. C3H6O2. Câu 36 : Cho hỗn hợp X gồm 0,2 mol H2NC3H5(COOH)2 (axit glutamic) và 0,1 mol H2NCH2COOH (glyxin) tác dụng với 300 ml dung dịch KOH 2M thu được dung dịch X. Cô cạn dung dịch X thu được m gam chất rắn khan. Giá trị của m là A. 43,5. B. 48,3. C. 61,5. D. 51,9. Câu 37 : Cho 1 mol chất X (C9H8O4, chứa vòng benzen) tác dụng tối đa với 3 mol NaOH trong dung dịch, thu được ba chất hữu cơ Y, Z, T (MY < MT < MZ). Đốt cháy hoàn toàn Z, thu được sản phẩm chỉ gồm CO2, Na2CO3. Phát biểu nào sau đây đúng? A. Đun nóng Z với hỗn hợp rắn NaOH và CaO, thu được ankan. B. Nhiệt độ sôi của Y cao hơn nhiệt độ sôi của Z và T. C. Đun nóng Y với dung dịch H2SO4 đặc 170oC, thu được anken. D. Từ Y có thể điều chế trực tiếp axit axetic bằng một phản ứng hóa học. Câu 38 : Hỗn hợp E gồm 3 este X, Y, Z đều no, mạch cacbon hở và không phân nhánh (MX < MY < MZ). Đốt cháy hoàn toàn 18,26 gam E cần 13,104 lít O2 (đktc), thu được 8,82 gam H2O. Mặt khác, đun nóng 18,26 gam E với dung dịch NaOH (lấy dư 40% so với lượng phản ứng), cô cạn dung dịch sau phản ứng thu được chất rắn T và hỗn hợp hai ancol no (kế tiếp trong dãy đồng đẳng). Đốt cháy hoàn toàn T, thu được Na2CO3, CO2 và 1,08 gam H2O. Phân tử khối của Z là A. 88. B. 118. C. 132. D. 146. Câu 39 : Chất X (CnH2n+4O4N2) là muối amoni của axit cacboxylic đa chức, chất Y (CmH2m+4O2N2) là muối amoni của một amino axit. Cho m gam E gồm X và Y (có tỉ lệ mol tương ứng là 7 : 3) tác dụng hết với lượng dư dung dịch NaOH đun nóng, thu được 0,17 mol etylamin và 15,09 gam hỗn hợp muối. Phần trăm khối lượng của X trong E có giá trị gần nhất với giá trị nào sau đây? A. 71. B. 52. C. 68. D. 77. Câu 40 : Hỗn hợp T gồm ba peptit mạch hở X, Y, Z có tỉ lệ mol tương ứng là 2 : 3 : 4. Thủy phân hoàn toàn 35,97 gam T thu được hỗn hợp sản phẩm gồm 0,29 mol A và 0,18 mol B. Biết tổng số liên kết peptit trong ba phân tử X, Y, Z bằng 16; A và B đều là amino axit no, có 1 nhóm -NH2 và 1 nhóm -COOH trong phân tử. Đốt cháy hoàn toàn m gam hỗn hợp T thu được N2, 0,74 mol CO2 và a mol H2O. Giá trị a gần nhất là A. 0,72. B. 0,69. C. 0,65. D. 0,67. Lời giải chi tiết ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI 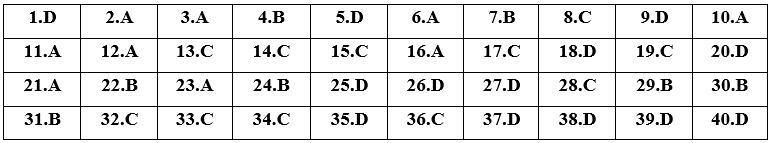 Câu 1 Tripeptit là hợp chất có 2 liên kết peptit mà phân tử có 3 gốc α-amino axit. Đáp án D Câu 2 Dầu luyn là hidrocacbon. Đáp án A Câu 3 C6H5NH2 có tên gọi là anilin. Đáp án A Câu 4 B sai vì anilin khó tan trong nước, không màu. Đáp án B Câu 5 Glucozo là monosaccarit nên không có phản ứng thủy phân. Đáp án D Câu 6 Trilinolein có công thức là (C17H31COO)3C3H5. PTHH: (C17H31COO)3C3H5 + H2O \(\overset{{{H}^{+}},{{t}^{o}}}{\mathop{\leftrightarrows }}\,\) 3C17H31COOH + C3H5(OH)3 Đáp án A Câu 7 Các tính chất đúng với mọi loại chất béo là: (3) nhẹ hơn nước; (5) tan trong xăng; (6) dễ bị thủy phân trong môi trường kiềm hoặc axit. Đáp án B Câu 8 Nhỏ dung dịch iot vào tinh bột sẽ xuất hiện màu xanh tím. Đáp án C Câu 9 Những chất có phản ứng tráng gương là những chất có chứa nhóm -CHO trong phân tử. Đáp án D Câu 10 Este etyl fomat có công thức là HCOOC2H5. Đáp án A Câu 11 Lysin có CTCT: H2N-CH2-CH2-CH2-CH2-CH(NH2)-COOH ⟹ có chứa 2 nhóm -NH2 trong phân tử. Đáp án A Câu 12 Các chất có phản ứng thủy phân là: Saccarozo (Y); Tinh bột (Z); Xenlulozo (H). Đáp án A Câu 13 Phương pháp: X + NaOH tạo 1 chất hữu cơ đơn chức và các chất vô cơ ⟹ X là C2H5NH3NO3 ⟹ Y ⟹ MY Hướng dẫn giải: X + NaOH tạo 1 chất hữu cơ đơn chức và các chất vô cơ ⟹ X là C2H5NH3NO3 PTHH: C2H5NH3NO3 + NaOH → C2H5NH2 + NaNO3 + H2O Vậy chất hữu cơ Y là C2H5NH2 có MY = 45 đvC. Đáp án C Câu 14 %mO = 100% - 40% - 6,66% = 53,34% Đặt CTPT của este là CxHyOz Ta có: ⟹ CTPT este có dạng (CH2O)n Mà X là este đơn chức nên có 2 nguyên tử O ⟹ n = 2 ⟹ CTPT của este là C2H4O2 ⟹ CTCT duy nhất là HCOOCH3 (metyl fomat). Đáp án C Câu 15 Nguyên nhân amin có tính bazo là trên nguyên tử N còn một đôi electron tự do có khả năng nhận H+. Đáp án C Câu 16 Tinh bột và xenlulozo đều có dạng (C6H10O5)n nhưng xenlulozo có giá trị n lớn hơn rất nhiều so với tinh bột ⟹ Khác về CTPT nên không phải là đồng phân của nhau. Đáp án A Câu 17 Phát biểu A sai vì xenlulozo có cấu trúc mạch không phân nhánh. Phát biểu B sai vì glucozơ bị oxi hóa bởi dung dịch AgNO3/NH3 đun nóng. Phát biểu C đúng. Phát biểu D sai vì saccarozo không có nhóm -CHO nên không có phản ứng tráng gương. Đáp án C Câu 18 D sai vì chỉ có protein dạng cầu tan được trong nước, còn protein dạng sợi (lông, móng, tóc, ...) không tan trong nước. Đáp án D Câu 19 Este có phản ứng tráng gương là este có đầu HCOO-. Vậy các este có CTPT C4H8O2 thỏa mãn là: HCOOCH2CH2CH3 HCOOCH(CH3)CH3 Đáp án C Câu 20 \(C{{H}_{4}}\xrightarrow{{{1500}^{o}}C}{{C}_{2}}{{H}_{2}}\xrightarrow{{{H}_{2}}O}C{{H}_{3}}CHO\xrightarrow{{{H}_{2}}}C{{H}_{3}}C{{H}_{2}}OH\xrightarrow{{{O}_{2}}}C{{H}_{3}}COOH\xrightarrow{{{C}_{2}}{{H}_{2}}}C{{H}_{3}}COOCH=C{{H}_{2}}\left( M \right)\) Các PTHH: 2CH4 \(\xrightarrow{{{1500}^{o}}C,lam.lanh.nhanh}\) C2H2 +3H2 C2H2 + H2O \(\xrightarrow{H{{g}^{2+}},{{t}^{o}}}\) CH3CHO CH3CHO+O2 \(\xrightarrow{{{t}^{o}}}\) CH3COOH CH3COOH + C2H2 \(\xrightarrow{{{t}^{o}},xt}\) CH3COOCH=CH2 Đáp án D Câu 21 Thuốc thử được dùng để phân biệt Gly-Ala-Gly với Gly-Ala là Cu(OH)2: + Tạo hợp chất màu tím ⟹ Gly-Ala-Gly + Không hiện tượng ⟹ Gly-Ala Đáp án A Câu 22 C17H31COOH + 2H2 \(\xrightarrow{Ni,{{t}^{o}}}\) C17H35COOH (axit linoleic) (axit stearic) Đáp án B Câu 23 Saccarozo phản ứng với Cu(OH)2/OH- tạo dung dịch xanh lam nhưng khi đun nóng thì không thu được kết tủa đỏ gạch vì không có nhóm -CHO. Đáp án A Câu 24 Phương pháp: Sự đổi màu của quỳ tím khi gặp amin, amino axit: *Amin: - Amin có nguyên tử N gắn trực tiếp với vòng benzen có tính bazo rất yếu, không làm đổi màu quỳ tím. - Các amin khác làm quỳ tím chuyển xanh. *Amino axit: - Số nhóm NH2 = số nhóm COOH ⟹ Không làm đổi màu quỳ tím - Số nhóm NH2 > số nhóm COOH ⟹ Làm quỳ tím hóa xanh (VD: Lysin) - Số nhóm NH2 < số nhóm COOH ⟹ Làm quỳ tím hóa đỏ (VD: Axit glutamic) Hướng dẫn giải: Các chất làm đổi màu quỳ tím thành xanh là: X2: CH3NH2; X5: H2NCH2CH2CH2CH(NH2)COOH. Đáp án B Câu 25 Công thức cấu tạo thu gọn của X là: CH3COOCH3. Đáp án D Câu 26 Phương pháp: Gọi công thức trung bình của 2 amin là Viết PTHH: \({{C}_{{\bar{n}}}}{{H}_{2\bar{n}+3}}N+\left( 1,5\bar{n}+0,75 \right){{O}_{2}}\xrightarrow{{{t}^{o}}}\bar{n}C{{O}_{2}}+\left( \bar{n}+1,5 \right){{H}_{2}}O+0,5{{N}_{2}}\) Từ tỉ lệ về số mol của CO2 và H2O tính được giá trị Suy ra công thức chung của hỗn hợp và số mol của hỗn hợp Tính khối lượng của hỗn hợp Hướng dẫn giải: nCO2 = 0,65 mol; nH2O = 1,025 mol Gọi công thức trung bình của 2 amin là \({{C}_{{\bar{n}}}}{{H}_{2\bar{n}+3}}N+\left( 1,5\bar{n}+0,75 \right){{O}_{2}}\xrightarrow{{{t}^{o}}}\bar{n}C{{O}_{2}}+\left( \bar{n}+1,5 \right){{H}_{2}}O+0,5{{N}_{2}}\) Ta có: \(\frac{{{n}_{C{{O}_{2}}}}}{{{n}_{{{H}_{2}}O}}}=\frac{{\bar{n}}}{\bar{n}+1,5}=\frac{0,65}{1,025}\to \bar{n}=2,6\) ⟹ Hỗn hợp có CTTC là C2,6H8,2N và nhỗn hợp = 0,65 : 2,6 = 0,25 mol ⟹ m = 0,25.53,4 = 13,35 gam Đáp án D Câu 27 Để cho việc tính toán đơn giản ta coi công thức của xenlulozo là C6H7O2(OH)3 C6H7O2(OH)3 + 3HO-NO2 → C6H7O2(ONO2)3 + 3H2O PT: 3.63 = 189 (g) 297 (g) ĐB: 18,9 (kg) ← 29,7 (kg) ⟹ mdd HNO3 = 18,9.(100/96) = 19,8675 (kg) ⟹ Vdd HNO3 = m : D = 19,8675 : 1,52 = 12,952 lít Đáp án D Câu 28 nO2 = 1,904/22,4 = 0,085 mol Gọi công thức chung của 2 este là \({{C}_{{\bar{n}}}}{{H}_{2\bar{n}}}{{O}_{2}}+\left( 1,5\bar{n}-1 \right){{O}_{2}}\xrightarrow{{{t}^{o}}}\bar{n}C{{O}_{2}}+\bar{n}{{H}_{2}}O\) \(\frac{0,085}{1,5\bar{n}-1}\leftarrow 0,085\left( mol \right)\) Ta có: \({{m}_{este}}=\frac{0,085}{1,5\bar{n}-1}.\left( 14\bar{n}+32 \right)=1,62\to \bar{n}=3,5\) Do 2 este là đồng đẳng kế tiếp nên là C3H6O2 và C4H8O2. Đáp án C Câu 29 nX = 0,1 mol; nNaOH = 0,3 mol - Xác định công thức cấu tạo của X và khí Y: X + NaOH ⟶ Khí Y làm xanh quỳ tím ẩm ⟹ X là (COONH4)2 ⟹ Y là NH3 - Xác định các chất trong chất rắn khan và tính m: (COONH4)2 + 2NaOH → (COONa)2 + 2NH3 + 2H2O 0,1 0,2 0,1 0,2 mol Chất rắn gồm: 0,1 mol (COONa)2 và 0,1 mol NaOH dư ⟹ mrắn = 17,4 gam Đáp án B Câu 30 Các amino axit đều có 1 nhóm NH2 ⟹ đipeptit X có chứa 2 nguyên tử N MX = 75 + 89 - 18 = 146 g/mol ⟹ nX = 14,6/146 = 0,1 mol ⟹ nHCl = nN = 2nX = 0,2 mol ⟹ Vdd HCl = 0,2 lít Đáp án B Câu 31 mtinh bột = 486.(80/100) = 388,8 kg (C6H10O5)n + nH2O → nC6H12O6 PT: 162n 180n (kg) ĐB: 388,8 → 432 (kg) Do hiệu suất đạt 75% nên khối lượng glucozo thực tế thu được là: 432.(75/100) = 324 kg Bấm máy nhanh: mglucozo(thực tế) = 486 . 0,8 : 162 . 180 . 0,75 = 324 kg Đáp án B Câu 32 X + NaOH tạo 2Z và Y (đều là 2 chất hữu cơ) ⟹ X là este Oxi hóa 1 mol Y cần 2 mol CuO ⟹ Y có 2 nhóm OH ⟹ Y có ít nhất 2 cacbon Vậy X: (HCOO)2C2H4 ⟹ Y: C2H4(OH)2 ⟹ T: (CHO)2 có MT = 58 Đáp án C Câu 33 Phương pháp: - X phản ứng với KOH thu được kết tủa → X có chứa Ca(HCO3)2 Để kết tủa đạt cực đại với lượng KOH tối thiểu thì xảy ra phản ứng: Ca(HCO3)2 + KOH → CaCO3 + KHCO3 + H2O Từ số mol của KOH tính được số mol Ca(HCO3)2 - Bảo toàn nguyên tố C tính được số mol CO2: nCO2 = nCaCO3 + 2nCa(HCO3)2 - Tính khối lượng tinh bột cần dùng theo sơ đồ: C6H10O5 → C6H12O6 → 2CO2 Lưu ý: Quá trình sản xuất có hiệu suất. Hướng dẫn giải: X phản ứng với KOH thu được kết tủa → X có chứa Ca(HCO3)2 Phản ứng của X với KOH có thể xảy ra theo 2 PTHH sau: (1) Ca(HCO3)2 + KOH → CaCO3 + KHCO3 + H2O (2) Ca(HCO3)2 + 2KOH → CaCO3 + K2CO3 + 2H2O Ở cả 2 PTHH trên lượng CaCO3 đều đạt lớn nhất, nhưng dùng KOH tối thiểu thì xảy ra phản ứng (1): Ca(HCO3)2 + KOH → CaCO3 + KHCO3 + H2O 0,1 ← 0,1 (mol) Vậy hấp thụ CO2 vào Ca(OH)2 thu được CaCO3 (0,3 mol) và Ca(HCO3)2 (0,1 mol) Bảo toàn C → nCO2 = nCaCO3 + 2nCa(HCO3)2 = 0,5 mol Sơ đồ: C6H10O5 → C6H12O6 → 2CO2 0,25 ← 0,5 (mol) → mtinh bột (LT) = 0,25.162 = 40,5 gam Do hiệu suất cả quá trình là 60% nên lượng tinh bột thực tế cần dùng phải lớn hơn lượng lý thuyết: → m = mtinh bột (TT) = 40,5.(100/60) = 67,5 gam Đáp án C Câu 34 Phương pháp: Cách xác định hiệu suất tính theo chất nào? Tương tự như cách xác định chất phản ứng hết. PTHH: aA + bB → cC + dD Đề bài cho biết nA và nB. Để biết được hiệu suất tính theo chất nào ta so sánh tỉ số \(\frac{{{n}_{A}}}{a}\) và \(\frac{{{n}_{B}}}{b}\) Tỉ số nào nhỏ hơn thì hiệu suất tính theo chất đó. Hướng dẫn giải: CH3COOH + C2H5OH \(\overset{{{H}_{2}}S{{O}_{4}}dac,{{t}^{o}}}{\mathop{\leftrightarrows }}\,\) CH3COOC2H5 + H2O \({{n}_{{{C}_{2}}{{H}_{5}}OH}}=0,5mol<{{n}_{C{{H}_{3}}COOH}}=0,4mol\) và tỉ lệ mol các chất phản ứng là 1 : 1 ⟹ Tính hiệu suất theo chất có ít số mol hơn là C2H5OH \(\to {{n}_{este}}=0,4.60%=0,24mol\to {{m}_{este}}=21,12g\) Đáp án C Câu 35 nCO2 = 0,6 mol; nH2O = 0,6 mol ⟹ X là este no, đơn chức, mạch hở CnH2nO2 → nCO2 PT: 14n + 32 (g) n (mol) ĐB: 14,8 (g) 0,6 (mol) ⟹ 0,6.(14n + 32) = 14,8n ⟹ n = 3 ⟹ CTPT của X là C3H6O2 Đáp án D Câu 36 nKOH = 0,3.2 = 0,6 mol H2NC3H5(COOH)2 + 2 KOH → H2NC3H5(COOK)2 + 2H2O 0,2 → 0,4 → 0,2 (mol) H2NCH2COOH + KOH → H2NCH2COOK + H2O 0,1 → 0,1 → 0,1 (mol) Vậy chất rắn thu được gồm: H2NC3H5(COOK)2: 0,2 mol H2NCH2COOK: 0,1 mol KOH dư: 0,6 - 0,4 - 0,1 = 0,1 mol → mchất rắn = 0,2.223 + 0,1.113 + 0,1.56 = 61,5 gam Đáp án C Câu 37 Phương pháp: X có 4O và phản ứng với NaOH theo tỉ lệ mol 1 : 3 ⟹ X là este 2 chức trong đó có 1 nhóm COO gắn trực tiếp với vòng benzen ⟹ Sản phẩm gồm có 1 muối cacboxylat 2 chức, 1 muối của phenol, ancol Đốt Z chỉ thu được CO2, Na2CO3 mà không thu được H2O nên Z là (COONa)2 CTCT của X là CH3OOC-COOC6H5 Viết PTHH giữa X và NaOH. Dựa vào MY < MT < MZ suy ra các chất Y và T Xét các nhận định và xác định tính đúng/sai của chúng Hướng dẫn giải: X có 4O và phản ứng với NaOH theo tỉ lệ mol 1 : 3 ⟹ X là este 2 chức trong đó có 1 nhóm COO gắn trực tiếp với vòng benzen ⟹ Sản phẩm gồm có 1 muối cacboxylat 2 chức, 1 muối của phenol, ancol Đốt Z chỉ thu được CO2, Na2CO3 mà không thu được H2O nên Z là (COONa)2 CTCT của X là CH3OOC-COOC6H5 CH3OOC-COOC6H5 + 3NaOH → (COONa)2 (Z) + C6H5ONa (T) + CH3OH (Y) + H2O - A sai vì (COONa)2 thực hiện phản ứng vôi tôi xút sẽ thu được H2, không thu được ankan \({{\left( COONa \right)}_{2}}+2NaOH\xrightarrow{CaO,{{t}^{o}}}2N{{a}_{2}}C{{O}_{3}}+{{H}_{2}}\) - B sai, nhiệt độ sôi của CH3OH (Y) thấp hơn nhiều so với (COONa)2 (Z) và C6H5ONa (T) - C sai, vì CH3OH (Y) không có phản ứng tách nước tạo anken - D đúng, vì \(C{{H}_{3}}OH+CO\xrightarrow{{{t}^{o}},xt}C{{H}_{3}}COOH\) Đáp án D Câu 38 *Đốt E: E + O2 → CO2 + H2O 18,26 (g) 0,585 (mol) 0,49 (mol) BTKL ⟹ mCO2 = mE + mO2 - mH2O = 28,16 (g) → nCO2 = 0,64 (mol) BTNT: O ⟹ nO(E) = 2nCO2 + nH2O - 2nO2 = 0,6 (mol) → nCOO = ½ nO(E) = 0,3 (mol) Ta thấy nCO2 > nH2O mà các este đều no → hỗn hợp có chứa este 2 chức (do mạch hở, không phân nhánh) → neste hai chức = nCO2 - nH2O = 0,64 - 0,49 = 0,15 mol Lại thấy nCOO = 2neste hai chức ⟹ X, Y, Z đều là este hai chức Thủy phân E thu dược các ancol no, đơn chức, đồng đẳng kế tiếp nên X, Y, Z đều được tạo bởi axit 2 chức và ancol đơn chức Ctb = 0,64 : 0,15 = 4,267 nên có 1 este có số C < 4,267 → X là (COOCH3)2 → 2 ancol là CH3OH và C2H5OH *Thủy phân E: nNaOH pư = nCOO = 0,3 mol → nNaOH dư = 0,3.40% = 0,12 mol (1) mhh E = 0,15.90 + 14x + 32y + 46z + 18.(-0,3) = 18,26 (2) nCO2 = 2.0,15 + x + y + 2z = 0,64 (3) nH2O(đốt muối) = nCH2 + 0,5nNaOH dư → x + 0,5.0,12 = 0,06 Giải hệ trên được x = 0; y = 0,26; z = 0,04 Do x = 0 ⟹ không cần trả CH2 cho gốc axit ⟹ X, Y, Z đều được tạo từ (COOH)2 Vì MX < MY < MZ nên các chất X, Y, Z là: (X) (COOCH3)2 (Y) CH3OOC-COOC2H5 (Z) (COOC2H5)2 ⟹ MZ = 146 Đáp án D Câu 39 Ta có: X + 2NaOH → Muối + 2C2H5NH2 + 2H2O Y + NaOH → Muối + C2H5NH2 + H2O Ta có nX : nY = 7 : 3 và nC2H5NH2 = 2nX + nY = 0,17 mol Suy ra nX = 0,07 mol và nY = 0,03 mol Bảo toàn khối lượng: mE + mNaOH = mmuối + mC2H5NH2 + mH2O → mE = 15,09 + 0,17.45 + 0,17.18 – 0,17.40 = 19 → mE = 0,07(14n + 96) + 0,03(14m + 64) = 19 → n = \(\frac{0,74-0,03m}{0,07}\) Vì m là số C của muối axit cacboxylic với C2H5NH2 nên m ≥ 6 n là số C của aa với C2H5NH2 nên n ≥ 4 Thỏa mãn với m = 6 và n = 8 thì mX = 0,07(14.8 + 96) =14,56 gam → %mX = 76,63% gần nhất với 77% Đáp án D Câu 40 Phương pháp: - Sử dụng phương pháp trùng ngưng hóa để tìm số mol các peptit - Sử dụng phương pháp quy đổi T thành CONH; CH2; H2O (với số mol H2O bằng số mol peptit) cho phản ứng đốt cháy Hướng dẫn giải: Gọi số mắt xích của X, Y, Z lần lượt là x, y, z. Tổng số liên kết peptit trong X, Y, Z là (x - 1) + (y - 1) + (z - 1) = 16 → x + y + z = 19 Sử dụng phương pháp trùng ngưng hóa: 2X + 3Y + 4Z → (A29B18)k (T') + 8H2O Số mắt xích của T': (2.15 + 3.2 + 4.2) ≤ 47k ≤ (2.2 + 3.2 + 4.15) → 44 ≤ 47k ≤ 70 → 1,07 ≤ k ≤ 1,49 → k = 1 → T' có dạng A29B18 → nA29B18 = nA/29 = 0,01 mol 2X + 3Y + 4Z → A29B18 + 8H2O 0,02 ← 0,03 ← 0,04 ← 0,01 → nT = 0,02 + 0,03 + 0,04 = 0,09 mol Quy đổi 35,97 gam T thành: CONH (0,47); CH2 (a); H2O (0,09) → 0,47.43 + 14a + 0,09.18 = 35,97 → a = 1,01 Đốt 35,97 gam T: Bảo toàn C → nCO2 = nCONH + nCO2 = 1,48 mol Bảo toàn H → nH2O = 0,5.nCONH + nCH2 + nH2O = 1,335 mol Tỷ lệ: 34,97g T tạo thành 1,48 mol CO2 và 1,335 mol H2O m g ……………0,74 mol → 0,6675 mol (gần nhất với 0,67) Đáp án D HocTot.Nam.Name.Vn
|















Danh sách bình luận