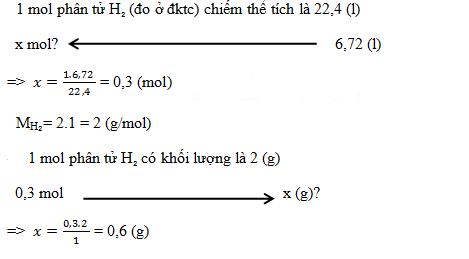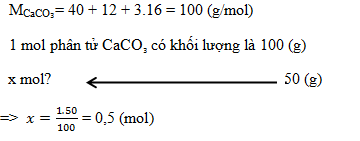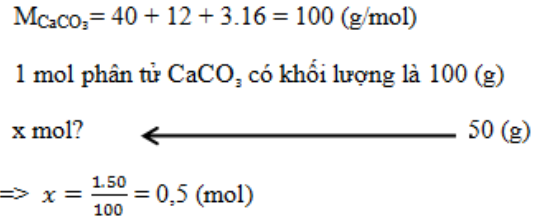Trắc nghiệm Bài 19. Chuyển đổi giữa khối lượng, thể tích và lượng chất - Hóa học 8Đề bài
Câu 1 :
Số mol phân tử N2 có trong 280 gam khí Nitơ là
Câu 2 :
Trong 24 gam MgO có bao nhiêu phân tử MgO?
Câu 3 :
Tính khối lượng nước biết trong đó có số phân tử bằng số phân tử có trong 20 gam NaOH?
Câu 4 :
Số mol nguyên tử hiđro có trong 36 gam nước là:
Câu 5 :
Phải lấy bao nhiêu gam sắt để có số nguyên tử nhiều gấp 2 lần số nguyên tử có trong 8 gam lưu huỳnh?
Câu 6 :
Thể tích của 280 gam khí nitơ ở đktc là: +) Khí nitơ có công thức hóa học là N2 +) Tính khối lượng mol N2 +) nN2=mM +) VN2=n∗22,4
Câu 7 :
Phải lấy bao nhiêu lít khí CO2 ở đktc để có 3,01.1023 phân tử CO2?
Câu 8 :
Lấy 1 mol mỗi mẫu chất sau: H2O, HCl, Fe2O3, C6H12O6. Mẫu chất có khối lượng lớn nhất là
Câu 9 :
Tìm dãy kết quả tất cả đúng về lượng chất (mol) của những khối lượng chất (gam) sau: 4 gam C; 62 gam P; 11,5 gam Na; 42 gam Fe
Câu 10 :
Tìm dãy tất cả kết quả đúng về số mol của những khối lượng chất sau: 15 gam CaCO3; 9,125 gam HCl; 100 gam CuO
Câu 11 :
Công thức đúng chuyển đổi giữa thể tích chất khí (đktc) và lượng chất là:
Câu 12 :
Thể tích của hỗn hợp khí gồm 0,5 mol CO2, và 0,2 mol O2 ở điều kiện tiêu chuẩn là
Câu 13 :
Số mol chứa trong 3.10 23 phân tử nước là:
Câu 14 :
Dãy kết quả tất cả đúng về khối lượng (g) của những chất sau là: 0,1 mol CH4; 0,15 mol CH3CHO; 0,3 mol HCOOC2H5.
Câu 15 :
Hỗn hợp X gồm 4 gam metan (CH4) và 7 gam etilen (C2H4) có thể tích là
Câu 16 :
3,36 lít khí axetilen (C2H2) ở điều kiện tiêu chuẩn có khối lượng là
Câu 17 :
0,2 mol C2H5CHO có khối lượng là
Câu 18 :
4,48 lít khí X ở điều kiện tiêu chuẩn chiếm số mol là
Câu 19 :
Biết 0,125 mol X có khối lượng 20 gam. Khối lượng mol phân tử của chất X là
Câu 20 :
Ở cùng điều kiện nhiệt độ và áp suất, so sánh thể tích của 4 gam CH4 và 1 gam H2 ta có:
Câu 21 :
1 mol khí SO2 ở điều kiện tiêu chuẩn có thể tích là:
Câu 22 :
Trong 16g CuSO4 có chứa bao nhiêu gam đồng?
Câu 23 :
Tính khối lượng khí H2 có trong 6,72 lít khí H₂(đo ở đktc)?
Câu 24 :
Tính số mol phân tử có trong 50 gam CaCO₃?
Câu 25 :
0,75 mol phân tử hyđro(đo ở đktc) chiếm thể tích bao nhiêu lít?
Lời giải và đáp án
Câu 1 :
Số mol phân tử N2 có trong 280 gam khí Nitơ là
Đáp án : B Phương pháp giải :
+) Khí Nitơ có công thức phân tử là N2 +) Tính khối lượng mol phân tử N2 => số mol N2 : n=mM Lời giải chi tiết :
Khối lượng mol phân tử N2 là: 14.2 = 28 g/mol => số mol N2 là : n=mM=28028=10(mol)
Câu 2 :
Trong 24 gam MgO có bao nhiêu phân tử MgO?
Đáp án : B Phương pháp giải :
+) Tính khối lượng mol của MgO=> số mol MgO là: n=mM => số phân tử MgO là: n.6,02.1023 Lời giải chi tiết :
Khối lượng của MgO là: m = 24 g/mol Khối lượng mol của MgO là: M = 24 + 16 = 40 gam => số mol MgO là: n=mM=2440=0,6(mol) => số phân tử MgO là: 0,6.6,02.1023 = 3,612.1023 (phân tử)
Câu 3 :
Tính khối lượng nước biết trong đó có số phân tử bằng số phân tử có trong 20 gam NaOH?
Đáp án : B Phương pháp giải :
+) Tính khối lượng mol của NaOH => số mol NaOH là: n=mM => số mol của H2O +) Tính Khối lượng mol của H2O => khối lượng nước là: m = n . M Lời giải chi tiết :
Khối lượng mol của NaOH là: M = 23 + 16 + 1 = 40 g/mol => số mol NaOH là: n=mM=2040=0,5(mol) => số mol của H2O là 0,5 mol Khối lượng mol của H2O là: M = 2 + 16 = 18 g/mol => khối lượng nước là: m = n . M = 0,5.18 = 9 gam
Câu 4 :
Số mol nguyên tử hiđro có trong 36 gam nước là:
Đáp án : D Lời giải chi tiết :
Khối lượng của H2O là: 36 gam Khối lượng mol của H2O : M = 2.1 + 16 = 18 g/mol => số mol của H2O là: n=mM=3618=2(mol) Trong 1 phân tử H2O có 2 nguyên tử H => trong 2 mol phân tử H2O có: 2.2 = 4 mol nguyên tử H
Câu 5 :
Phải lấy bao nhiêu gam sắt để có số nguyên tử nhiều gấp 2 lần số nguyên tử có trong 8 gam lưu huỳnh?
Đáp án : C Lời giải chi tiết :
Khối lượng của S là: m = 8 gam Khối lượng mol của S là: M = 32 g/mol => số mol của S là: n=mM=832=0,25(mol) Vì số nguyên tử của sắt nhiều gấp 2 lần số nguyên tử S => số mol sắt nhiều gấp 2 lần số mol S => số mol sắt là: 0,25.2 = 0,5 mol Khối lượng mol của sắt là M = 56 g/mol => khối lượng sắt cần lấy là: m = n. M = 0,5.56 = 28 gam
Câu 6 :
Thể tích của 280 gam khí nitơ ở đktc là: +) Khí nitơ có công thức hóa học là N2 +) Tính khối lượng mol N2 +) nN2=mM +) VN2=n∗22,4
Đáp án : D Lời giải chi tiết :
Khối lượng mol của khí N2 là: M = 2.14 = 28 g/mol => số mol khí N2 là: n=mM=28028=10(mol) => thể tích cảu 280 gam khí nitơ là: V = n.22,4 = 10.22,4 = 224 lít
Câu 7 :
Phải lấy bao nhiêu lít khí CO2 ở đktc để có 3,01.1023 phân tử CO2?
Đáp án : A Lời giải chi tiết :
1 mol CO2 chứa 6,02.1023 phân tử => 3,01.10236,02.1023=0,5 mol CO2 chứa 3,01.1023 phân tử => thể tích khí CO2 là: V = n.22,4 = 0,5.22,4 = 11,2 lít
Câu 8 :
Lấy 1 mol mỗi mẫu chất sau: H2O, HCl, Fe2O3, C6H12O6. Mẫu chất có khối lượng lớn nhất là
Đáp án : D Lời giải chi tiết :
Vì cùng lấy 1 mol chất => chất có khối lượng lớn nhất cũng là chất có khối lượng mol lớn nhất Khối lượng mol của H2O là: M = 2.1 + 16 = 18 g/mol Khối lượng mol của HCl là: M = 1 + 35,5 = 36,5 g/mol Khối lượng mol của Fe2O3 là M = 56.2 + 16.3 = 160 g/mol Khối lượng mol của C6H12O6 là: M = 12.6 + 12 + 16.6 = 180 g/mol => chất có khối lượng lớn nhất là C6H12O6
Câu 9 :
Tìm dãy kết quả tất cả đúng về lượng chất (mol) của những khối lượng chất (gam) sau: 4 gam C; 62 gam P; 11,5 gam Na; 42 gam Fe
Đáp án : A Lời giải chi tiết :
Số mol của 4 gam C là: n=mM=412=0,33mol Số mol của 62 gam P là: n=mM=6231=2mol Số mol của 11,5 gam Na là: n=mM=11,523=0,5mol Số mol của 42 gam Fe là: n=mM=4256=0,75mol
Câu 10 :
Tìm dãy tất cả kết quả đúng về số mol của những khối lượng chất sau: 15 gam CaCO3; 9,125 gam HCl; 100 gam CuO
Đáp án : C Phương pháp giải :
Chuyển đổi giữa lượng chất và khối lượng chất Lời giải chi tiết :
Khối lượng mol của CaCO3 là: M = 40 + 12 + 16.3 = 100 g/mol => số mol của CaCO3 là: n=mM=15100=0,15mol Khối lượng mol của HCl là: M = 1 + 35,5 = 36,5 g/mol => số mol của HCl là: n=mM=9,12536,5=0,25mol Khối lượng mol của CuO là: M = 64 + 16 = 80 g/mol => số mol của CuO là: n=mM=10080=1,25mol
Câu 11 :
Công thức đúng chuyển đổi giữa thể tích chất khí (đktc) và lượng chất là:
Đáp án : B Lời giải chi tiết :
Công thức chuyển đổi giữa thể tích chất khí(đktc) và chất lượng là: V= n. 22,4
Câu 12 :
Thể tích của hỗn hợp khí gồm 0,5 mol CO2, và 0,2 mol O2 ở điều kiện tiêu chuẩn là
Đáp án : D Phương pháp giải :
V =22,4 n Lời giải chi tiết :
Thể tích của hỗn hợp khí gồm 0,5 mol CO2, và 0,2 mol O2 ở điều kiện tiêu chuẩn là V = (0,5 +0,2).22,4 =15,68 lít
Câu 13 :
Số mol chứa trong 3.10 23 phân tử nước là:
Đáp án : D Phương pháp giải :
N = 6.1023 .n Lời giải chi tiết :
Số mol chứa trong 3.10 23 phân tử nước là: 3.1023 : (6.1023) = 0,5 mol
Câu 14 :
Dãy kết quả tất cả đúng về khối lượng (g) của những chất sau là: 0,1 mol CH4; 0,15 mol CH3CHO; 0,3 mol HCOOC2H5.
Đáp án : C Phương pháp giải :
Tính phân tử khối của các chất sau đó áp dụng công thức: m = n×M (g) Lời giải chi tiết :
MCH4 = MC + 4MH = 12 + 4.1 = 16 (g/mol) ⟹ mCH4 = nCH4×MCH4 = 0,1×16 = 1,6 (g) MCH3CHO = 2MC + 4MH + MO = 2.12 + 4.1 + 16 = 44 (g/mol) ⟹ mCH3CHO = nCH3CHO×MCH3CHO = 0,15×44=6,6 (g) MHCOOC2H5 = 3MC + 6MH + 2MO = 3,12 + 6.1 + 2.16 = 74 (g/mol) ⟹ mHCOOC2H5 = nHCOOC2H5×MHCOOC2H5 = 0,3×74 = 22,2 (g)
Câu 15 :
Hỗn hợp X gồm 4 gam metan (CH4) và 7 gam etilen (C2H4) có thể tích là
Đáp án : C Phương pháp giải :
Bước 1: Tính MCH4 = MC + 4MH ⟹ nCH4 = mCH4/MCH4 Bước 2: Tính MC2H4 = 2MC + 4MH ⟹ nC2H4 = mC2H4/MC2H4 Bước 3: Tính ∑nCH4+C2H4 =nCH4 + nC2H4. Từ đó tính được Vhh = ∑nCH4+C2H4 ×2,24 Lời giải chi tiết :
MCH4 = MC + 4MH = 12 + 4.1 = 16 (g/mol) ⇒nCH4=mCH4MCH4=416=0,25(mol) MC2H4 = 2MC + 4MH = 2.12 + 4.1 = 28 (g/mol) ⇒nC2H4=mC2H4MC2H4=728=0,25(mol) ⟹ ∑nCH4+C2H4 = 0,25 + 0,25 = 0,5 (mol) Thể tích của hỗn hợp X là: Vx (đktc) = ∑nCH4+C2H4 ×2,24 = 0,5×2,24 =11,2 (lít)
Câu 16 :
3,36 lít khí axetilen (C2H2) ở điều kiện tiêu chuẩn có khối lượng là
Đáp án : A Phương pháp giải :
Bước 1: Đổi số mol C2H2 theo công thức: n = V/22,4 Bước 2: Tính phân tử khối của C2H2 = 2MC + 2MH Bước 3: Tính mC2H2 = nC2H2×MC2H2 = ? Lời giải chi tiết :
Bước 1: Tính số mol: n=V22,4=3,3622,4=0,15(mol) Bước 2: Tính phân tử khối C2H2: MC2H2 = 2MC + 6M2= 2.12 + 2.1 = 26 (g/mol) Bước 3: Tính: mC2H2 = nC2H2×MC2H2 = 0,15×26 = 3,9 (g)
Câu 17 :
0,2 mol C2H5CHO có khối lượng là
Đáp án : B Phương pháp giải :
Bước 1: Tính MC2H5CHO = 3MC + 6MH + MO = ? Bước 2: Tính mC2H5OH = nC2H5OH×MC2H5CHO = ? Lời giải chi tiết :
Xét C2H5CHO = 3C + 6H + 1O = 3.12 + 6.1 + 1.16 = 58 (g/mol) ⟹ mC2H5CHO = n×M = 0,2×58 = 11,6 (g).
Câu 18 :
4,48 lít khí X ở điều kiện tiêu chuẩn chiếm số mol là
Đáp án : A Phương pháp giải :
áp dụng công thức: n=V22,4=? Lời giải chi tiết :
áp dụng công thức: n=V22,4=4,4822,4=0,2(mol)
Câu 19 :
Biết 0,125 mol X có khối lượng 20 gam. Khối lượng mol phân tử của chất X là
Đáp án : C Phương pháp giải :
áp dụng công thức: M=mn=?(g/mol) Lời giải chi tiết :
áp dụng công thức: M=mn=200,125=160(g/mol)
Câu 20 :
Ở cùng điều kiện nhiệt độ và áp suất, so sánh thể tích của 4 gam CH4 và 1 gam H2 ta có:
Đáp án : B Phương pháp giải :
Cùng điều kiện nhiệt độ áp suất tỉ lệ số mol bằng tỉ lệ thể tích Lời giải chi tiết :
nCH4 = 4 : 16 =0,25 mol nH2 =0,5 mol Vì nH2 > nCH4 nên VH2 > VCH4
Câu 21 :
1 mol khí SO2 ở điều kiện tiêu chuẩn có thể tích là:
Đáp án : A Phương pháp giải :
Công thức tính thể tích của 1 chất ở đktc là: V = n ×22,4 = ? (lít) Lời giải chi tiết :
Ở điều kiện tiêu chuẩn 1 mol khí bất kì có thể tích là 22,4 lít
Câu 22 :
Trong 16g CuSO4 có chứa bao nhiêu gam đồng?
Đáp án : A Lời giải chi tiết :
nCuSO4 = mCuSO4 : MCuSO4 = 16 : 160 = 0,1 mol Trong 1mol CuSO4 có 1 mol Cu => 0,1 mol CuSO4 có 0,1 mol Cu => mCu = nCu . MCu = 0,1 . 64 = 6,4g
Câu 23 :
Tính khối lượng khí H2 có trong 6,72 lít khí H₂(đo ở đktc)?
Đáp án : A Lời giải chi tiết :
Câu 24 :
Tính số mol phân tử có trong 50 gam CaCO₃?
Đáp án : B Lời giải chi tiết :
Câu 25 :
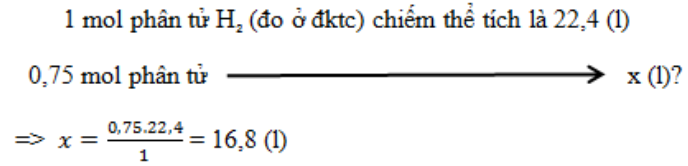
0,75 mol phân tử hyđro(đo ở đktc) chiếm thể tích bao nhiêu lít?
Đáp án : D Lời giải chi tiết :
|