Trắc nghiệm Bài 41. Phenol - Hóa 11Đề bài
Câu 1 :
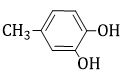
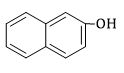
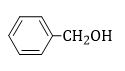
Chất nào sau đây không phải là phenol ?
Câu 2 :
Chất X có CTCT như hình bên. X có tên gọi 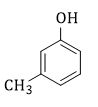
Câu 3 :
Có 2 lọ dung dịch mất nhãn là etanol và phenol. Dùng hóa chất nào sau đây để nhận biết 2 lọ trên ?
Câu 4 :
Hợp chất thơm X có CTPT C7H8O. X có thể tác dụng với Na và NaOH. Số đồng phân X thỏa mãn là:
Câu 5 :
Phenol có khả năng dễ tham gia phản ứng thế với dung dịch Br2 vì
Câu 6 :
Phenol phản ứng được với dung dịch nào sau đây ?
Câu 7 :
X và Y là 2 hợp chất hữu cơ thơm có công thức là C7H8O, đều không làm mất màu dung dịch brom. X chỉ tác dụng với Na, không tác dụng với dung dịch NaOH, Y không tác dụng với Na và NaOH. Vậy X và Y lần lượt là
Câu 8 :
Nếu cho cùng một lượng chất tác dụng với Na hoặc với NaOH thì số mol X phản ứng bằng số mol NaOH và bằng số mol H2 sinh ra. X là
Câu 9 :
Phát biểu nào sau đây về phenol là sai?
Câu 10 :
Cho các phát biểu sau về phenol: (a) phenol tan nhiều trong nước lạnh; (b) phenol có tính axit nhưng phenol không làm đổi màu quỳ tím; (c) phenol được dùng để sản xuất phẩm nhuộm, chất diệt nấm mốc; (d) nguyên tử H trong benzen dễ bị thế hơn nguyên tử H trong vòng benzen của phenol; (e) cho nước brom vào phenol thấy xuất hiện kết tủa. Số phát biểu đúng là
Câu 11 :
Cho 6,04 gam hỗn hợp X gồm phenol và ancol etylic tác dụng với Na dư thu được 1,12 lít H2 (đktc). Khi cho hỗn hợp X vào dung dịch Br2 dư thì thu được bao nhiêu gam kết tủa?
Câu 12 :
Cho 15,8 gam hỗn hợp gồm CH3OH, C6H5OH tác dụng với dung dịch brom dư, thì làm mất màu vừa hết 48 gam Br2. Nếu đốt cháy hoàn toàn hỗn hợp trên thì thể tích CO2 thu được ở điều kiện tiêu chuẩn là
Câu 13 :
Đốt cháy hoàn toàn hỗn hợp X gồm phenol và etanol (tỉ lệ mol là 1:3) rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch nước vôi trong thì thu được 15 gam kết tủa. Lọc bỏ kết tủa, lấy dung dịch thu được tác dụng với dung dịch NaOH dư thì thấy xuất hiện 7,5 gam kết tủa nữa. Khối lượng hỗn hợp X là
Câu 14 :
Cho m gam hỗn hợp X gồm phenol và etanol phản ứng hoàn toàn với Na dư thu được 2,24 lít khí H2 (đktc). Mặt khác, m gam hỗn hợp X phản ứng vừa đủ với 100 ml dung dịch NaOH 1M. Giá trị của m là
Câu 15 :
Cho dung dịch chứa m gam hỗn hợp gồm phenol (C6H5OH) và axit clohiđric (HCl) tác dụng vừa đủ với nước brom, thu được dung dịch X và 33,1 gam kết tủa. Trung hòa hoàn toàn X cần vừa đủ 500ml dung dịch NaOH 1M. Giá trị của m là
Câu 16 :
Đốt cháy 21 gam chất X là dẫn xuất benzen (CTPT trùng với CTĐGN), thu được 23,52 lit CO2 (đktc) và 10,8 gam H2O. Mặt khác, 21 gam X tác dụng vừa đủ với dung dịch NaOH thu được 27,6 gam muối. Số CTCT của X là:
Câu 17 :
Cho 0,01 mol phenol tác dụng hoàn toàn với lượng dư dung dịch hỗn hợp HNO3 đặc và H2SO4 đặc. Phát biểu nào sau đây không đúng
Câu 18 :
Cho etanol, phenol lần lượt tác dụng với Na, dung dịch NaOH, dung dịch Br2. Số phản ứng xảy ra là
Câu 19 :
Phản ứng giữa CO2 với dung dịch C6H5ONa xảy ra theo phương trình hóa học sau: CO2 + H2O + C6H5ONa → C6H5OH + NaHCO3. Phản ứng xảy ra được là do phenol có:
Câu 20 :
Cho 11,28 gam phenol tác dụng với lượng dư dung dịch Br2, sau phản ứng kết thúc thu được m gam kết tủa trắng. Giá trị của m là:
Câu 21 :
0,5 mol phenol có khối lượng là:
Câu 22 :
Để thu được 22,9 gam axit picric cần m gam phenol. Giá trị của m là ? Biết hiệu suất phản ứng đạt 94%.
Câu 23 :
Cho các chất : C6H5OH (X) ; C6H5CH2OH (Y) ; HOC6H4OH (Z) ; C6H5CH2CH2OH (T). Các chất đồng đẳng của nhau là :
Câu 24 :
Một dung dịch chứa 6,1 g chất X là đồng đẳng của phenol đơn chức. Cho dung dịch trên tác dụng với nước brom dư thu được 17,95 g hợp chất Y chứa 3 nguyên tử Br trong phân tử. Biết hợp chất này có nhiều hơn 3 đồng phân cấu tạo. CTPT chất đồng đẳng của phenol là
Câu 25 :
Phenol (công thức hóa học C6H5OH) là một hợp chất phổ biến trong bộ môn Hóa học. Đây là chất rắn ở dạng tinh thể, không màu, có mùi đặc trưng và nóng chảy ở nhiệt độ 43oC. Khi để bên ngoài không khí, phenol sẽ bị oxi hóa một phần chuyển sang màu hồng, và bị chảy rữa do hút ẩm. Phenol trước đây được chiết xuất từ nhựa than đá. Nhưng sau này, để đáp ứng nhu cầu lớn (khoảng 7 triệu tấn/năm), phenol được điều chế chủ yếu bằng cách oxi hóa các chế phẩm dầu mỏ. Trong công nghiệp, phenol được sử dụng rộng rãi để chế tạo nhựa, tơ sợi hóa học, thuốc diệt cỏ, thuốc nhuộm, thuốc nổ, thuốc sát trùng, thuốc chữa cúm, ... Khi tiếp xúc với phenol, cần tuyệt đối tránh để phenol chạm trực tiếp vào da, mắt và các cơ quan thuộc hệ hô hấp. Phenol là một chất rất độc, khi rơi vào da sẽ gây bỏng hóa học rất nặng. Ngoài ra, phần da chạm vào phenol rất dễ nổi mụn nước lâu ngày không khỏi. Bên cạnh đó, phenol cũng được chứng minh gây nhiều tác hại cho cơ thể người như rối loạn nhịp tim, tai biến, đau thận, đau gan, hôn mê. Trong Thế chiến thứ hai, phenol được sử dụng để làm chất độc giết người cho lò hơi ngạt trong các trại tập trung của Đức Quốc xã hoặc tiêm trực tiếp vào các nạn nhân khiến họ tử vong.
Câu 25.1
Hãy chọn các câu phát biểu đúng về phenol? (1) Hợp chất thuộc loại phenol là hợp chất có vòng benzen và có nhóm -OH. (2) Phenol là hợp chất chứa một hoặc nhiều nhóm hiđroxyl (-OH) liên kết trực tiếp với vòng benzen. (3) Phenol có tính axit nhưng nó là axit yếu hơn axit cacbonic. (4) Phenol tan trong nước lạnh vô hạn. (5) Phenol tan trong dung dịch NaOH tạo thành natri phenolat.
Câu 25.2
Để rửa sạch chai lọ đựng phenol, nên dùng cách nào sau đây?
Câu 25.3
Trong một lần làm thí nghiệm chẳng may do sơ ý, bạn An đã làm phenol đổ ra tay và bị bỏng. Cô giáo thấy vậy liền cấp cứu sơ bộ cho An như sau: “Rửa nhiều lần bằng glixerol cho tới khi màu da trở lại bình thường rồi rửa lại bằng nước, sau đó băng chỗ bỏng bằng bông tẩm glixerol”. Em hãy giải thích tại sao cô giáo lại làm như vậy?
Lời giải và đáp án
Câu 1 :
Chất nào sau đây không phải là phenol ?
Đáp án : D Lời giải chi tiết :
D không phải là phenol mà là ancol thơm vì trong phân tử có nhóm –OH liên kết với nguyên tử C no thuộc mạch nhánh của vòng benzen
Câu 2 :
Chất X có CTCT như hình bên. X có tên gọi 
Đáp án : D Lời giải chi tiết :
Đánh số từ nhóm OH => tên gọi: 3-metylphenol
Câu 3 :
Có 2 lọ dung dịch mất nhãn là etanol và phenol. Dùng hóa chất nào sau đây để nhận biết 2 lọ trên ?
Đáp án : B Lời giải chi tiết :
Để nhận biết etanol và phenol ta dùng dung dịch brom. Etanol không phản ứng, phenol làm mất màu dung dịch, tạo kết tủa trắng.
Câu 4 :
Hợp chất thơm X có CTPT C7H8O. X có thể tác dụng với Na và NaOH. Số đồng phân X thỏa mãn là:
Đáp án : A Lời giải chi tiết :
X có thể tác dụng với Na và NaOH nên X là phenol. Vậy X có 3 đồng phân là: 2-metylphenol; 3-metylphenol; 4-metylphenol
Câu 5 :
Phenol có khả năng dễ tham gia phản ứng thế với dung dịch Br2 vì
Đáp án : D Lời giải chi tiết :
Phenol có khả năng dễ tham gia phản ứng thế với dung dịch Br2 vì có nhóm OH đẩy điện tử vào vòng benzen làm H trong vòng dễ bị thế.
Câu 6 :
Phenol phản ứng được với dung dịch nào sau đây ?
Đáp án : D Lời giải chi tiết :
Phenol phản ứng được với dung dịch KOH
Câu 7 :
X và Y là 2 hợp chất hữu cơ thơm có công thức là C7H8O, đều không làm mất màu dung dịch brom. X chỉ tác dụng với Na, không tác dụng với dung dịch NaOH, Y không tác dụng với Na và NaOH. Vậy X và Y lần lượt là
Đáp án : D Lời giải chi tiết :
X chỉ tác dụng với Na, không tác dụng với dung dịch NaOH => X không phải là phenol => X là ancol C6H5CH2OH Y không tác dụng với Na và NaOH => Y là ete C6H5OCH3
Câu 8 :
Nếu cho cùng một lượng chất tác dụng với Na hoặc với NaOH thì số mol X phản ứng bằng số mol NaOH và bằng số mol H2 sinh ra. X là
Đáp án : B Phương pháp giải :
1 nhóm OH $\xrightarrow{+Na}$ $\frac{1}{2}$ H2 Lời giải chi tiết :
Số mol X bằng số mol NaOH phản ứng => X chứa 1 nhóm –OH phenol Số mol X bằng số mol H2 sinh ra => X chứa 2 nhóm –OH trong phân tử => X chứa 1 nhóm –OH phenol và 1 nhóm –OH ancol
Câu 9 :
Phát biểu nào sau đây về phenol là sai?
Đáp án : A Lời giải chi tiết :
Phát biểu sai là: Phenol thuộc loại ancol thơm, đơn chức vì phenol không phải ancol thơm.
Câu 10 :
Cho các phát biểu sau về phenol: (a) phenol tan nhiều trong nước lạnh; (b) phenol có tính axit nhưng phenol không làm đổi màu quỳ tím; (c) phenol được dùng để sản xuất phẩm nhuộm, chất diệt nấm mốc; (d) nguyên tử H trong benzen dễ bị thế hơn nguyên tử H trong vòng benzen của phenol; (e) cho nước brom vào phenol thấy xuất hiện kết tủa. Số phát biểu đúng là
Đáp án : B Lời giải chi tiết :
Các phát biểu đúng là: (b) phenol có tính axit nhưng phenol không làm đổi màu quỳ tím; (c) phenol được dùng để sản xuất phẩm nhuộm, chất diệt nấm mốc; (e) cho nước brom vào phenol thấy xuất hiện kết tủa.
Câu 11 :
Cho 6,04 gam hỗn hợp X gồm phenol và ancol etylic tác dụng với Na dư thu được 1,12 lít H2 (đktc). Khi cho hỗn hợp X vào dung dịch Br2 dư thì thu được bao nhiêu gam kết tủa?
Đáp án : C Phương pháp giải :
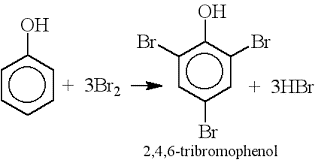
Gọi ${n_{{C_6}{H_5}OH}} = \,x\,\,mol;\,{n_{{C_2}{H_5}OH}} = \,y\,mol$ → mhỗn hợp X = PT (1) → ${n_{{H_2}}} = \,0,05\,mol$ → PT (2) C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr Lời giải chi tiết :
Gọi ${n_{{C_6}{H_5}OH}} = \,x\,\,mol;\,\,\,{n_{{C_2}{H_5}OH}}\, = \,y\,\,mol$ → mhỗn hợp X = 94x + 46y = 6,04 (1) C6H5OH + Na $\xrightarrow{{}}$ C6H5ONa + $\frac{1}{2}$ H2↑ x mol → 0,5x mol C2H5OH + Na $\xrightarrow{{}}$ C2H5ONa + $\frac{1}{2}$ H2↑ y mol → 0,5y mol → ${n_{{H_2}}} = \,\,\,\frac{{1,12}}{{22,4}}\,\, = \,\,0,05\,mol$ → 0,5x + 0,5y = 0,05 (2) Từ (1) và (2) → $\left\{ \begin{gathered}0,5x + 0,5y\, = 0,05 \hfill \\94x + 46y = 6,04 \hfill \\ \end{gathered} \right.\,\,\, \to \,\,\,\left\{ \begin{gathered}x = 0,03 \hfill \\ y = 0,07 \hfill \\ \end{gathered} \right.$ Hỗn hợp X + dung dịch Br2 dư : C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr 0,03 → 0,03 → ${m_ \downarrow } = {m_{{C_6}{H_3}B{r_3}O}} = 0,03.331 = 9,93\,\,gam$
Câu 12 :
Cho 15,8 gam hỗn hợp gồm CH3OH, C6H5OH tác dụng với dung dịch brom dư, thì làm mất màu vừa hết 48 gam Br2. Nếu đốt cháy hoàn toàn hỗn hợp trên thì thể tích CO2 thu được ở điều kiện tiêu chuẩn là
Đáp án : D Phương pháp giải :
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr Từ số mol Br2 tính số mol C6H5OH => số mol CH3OH +) Bảo toàn nguyên tố C: ${n_{C{O_2}}} = {n_{C{H_3}OH}} + \,6.{n_{{C_6}{H_5}OH}}$ Lời giải chi tiết :
${n_{B{r_2}}} = \,\frac{{48}}{{160}}\, = 0,3\,mol$ C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr 0,1 mol ← 0,3 mol → ${m_{{C_6}{H_5}OH}} = \,0,1.94 = 9,4\,gam$→ ${m_{C{H_3}OH}} = \,15,8 - 9,4 = 6,4\,gam$ → ${n_{C{H_3}OH}} = \frac{{6,4}}{{32}} = 0,2\,mol$ Bảo toàn nguyên tố C: → ${n_{C{O_2}}} = {n_{C{H_3}OH}} + \,6.{n_{{C_6}{H_5}OH}} = 0,2 + 6.0,1 = 0,8\,mol$ → ${V_{C{O_2}(\,ktc)}} = 0,8.22,4 = 17,92\,$ lít
Câu 13 :
Đốt cháy hoàn toàn hỗn hợp X gồm phenol và etanol (tỉ lệ mol là 1:3) rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch nước vôi trong thì thu được 15 gam kết tủa. Lọc bỏ kết tủa, lấy dung dịch thu được tác dụng với dung dịch NaOH dư thì thấy xuất hiện 7,5 gam kết tủa nữa. Khối lượng hỗn hợp X là
Đáp án : A Phương pháp giải :
Áp dụng đinh luật bảo toàn nguyên tử: ${n_{C{O_2}}} = \,\,2{n_{{C_2}{H_5}OH}}\,\, + \,\,6{n_{{C_6}{H_5}OH}}\,$; ${n_{{H_2}O}} = \,\,3{n_{{C_2}{H_5}OH}} + \,\,3{n_{{C_6}{H_5}OH}}$ $ + ){n_{Ca{{(HC{O_3})}_2}(2)}} = {n_{CaC{O_3}(3)}}$ +) $\sum {n_{C{O_2}}} = {n_{C{O_2}(1)}} + {n_{C{O_2}(2)}} = {n_{CaC{O_3}}} + 2{n_{Ca{{(HC{O_3})}_2}}}$ Lời giải chi tiết :
Gọi ${n_{{C_6}{H_5}OH}} = \,x\,\,mol\, \to \,{n_{{C_2}{H_5}OH}} = 3x\,\,mol$ (vì tỉ lệ mol là 1:3) Áp dụng đinh luật bảo toàn nguyên tử: ${n_{C{O_2}}} = \,\,2{n_{{C_2}{H_5}OH}}\,\, + \,\,6{n_{{C_6}{H_5}OH}}\, = \,\,2.3x\, + \,6x\,\, = \,\,12x$ mol ${n_{{H_2}O}} = \,\,3{n_{{C_2}{H_5}OH}} + \,\,3{n_{{C_6}{H_5}OH}} = 3.3x\, + \,3x\,\, = \,\,12x$ mol Khi cho sản phẩm cháy vào bình đựng dung dịch nước vôi trong xảy ra các phản ứng: CO2 + Ca(OH)2 $ \to $ CaCO3 ↓ + H2O (1) 2CO2 + Ca(OH)2 $ \to $ Ca(HCO3)2 (2) Ta có:${n_{CaC{O_3}(1)}} = \frac{{15}}{{100}} = 0,15\,\,mol$ Dung dịch sau phản ứng tác dụng với NaOH dư xảy ra phương trình hóa học sau: $Ca{(HC{O_3})_2}\, + \,2NaOH \to \,Ca\,C{O_3} \downarrow \, + \,N{a_2}C{O_3} + {H_2}O\,\,\,(3)$ → ${n_{Ca{{(HC{O_3})}_2}(2)}} = {n_{CaC{O_3}(3)}} = \frac{{7,5}}{{100}} = 0,075\,mol$ → $\sum {n_{C{O_2}}} = {n_{C{O_2}(1)}} + {n_{C{O_2}(2)}} = {n_{CaC{O_3}(1)}} + 2{n_{Ca{{(HC{O_3})}_2}(2)}} = 0,15 + \,\,2.0,075$= 0,3 mol Mà ${n_{C{O_2}}}$= 12x → 12x = 0,3 → x = 0,025 mol → mhỗn hợp X =${m_{{C_6}{H_5}OH}} + {m_{{C_2}{H_5}OH}}$ = 94.0,025 + 46.3.0,025 = 5,8 gam.
Câu 14 :
Cho m gam hỗn hợp X gồm phenol và etanol phản ứng hoàn toàn với Na dư thu được 2,24 lít khí H2 (đktc). Mặt khác, m gam hỗn hợp X phản ứng vừa đủ với 100 ml dung dịch NaOH 1M. Giá trị của m là
Đáp án : C Phương pháp giải :
${n_{{C_6}{H_5}OH}}\, + \,{n_{{C_2}{H_5}OH}}\, = \,2{n_{{H_2}}}$ C6H5OH + NaOH $ \to $ C6H5ONa + H2O Từ số mol NaOH => số mol C6H5OH Lời giải chi tiết :
${n_{{H_2}}} = \frac{{2,24}}{{22,4}} = 0,1\,mol$, nNaOH = 1.0,1 = 0,1 mol C6H5OH + Na $ \to $ C6H5ONa + $\frac{1}{2}$ H2 C2H5OH + Na $ \to $ C2H5ONa + $\frac{1}{2}$ H2 → ${n_{{C_6}{H_5}OH}}\, + \,{n_{{C_2}{H_5}OH}}\, = \,2{n_{{H_2}}} = \,2.0,1 = 0,2\,mol$ C6H5OH + NaOH $ \to $ C6H5ONa + H2O 0,1 mol ← 0,1 mol → ${n_{{C_2}{H_5}OH}} = \,0,2 - {n_{{C_6}{H_5}OH}}\, = \,0,2 - 0,1 = 0,1\,mol$ → $m = {m_{{C_6}{H_5}OH}} + {m_{{C_2}{H_5}OH}} = 0,1.94 + 0,1.46 = 14\,\,gam$
Câu 15 :
Cho dung dịch chứa m gam hỗn hợp gồm phenol (C6H5OH) và axit clohiđric (HCl) tác dụng vừa đủ với nước brom, thu được dung dịch X và 33,1 gam kết tủa. Trung hòa hoàn toàn X cần vừa đủ 500ml dung dịch NaOH 1M. Giá trị của m là
Đáp án : A Phương pháp giải :
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr 0,1 ← 0,1 → 0,3 → Dung dịch X: HCl; HBr (0,3 mol) +) ${n_{{\text{HCl}}}}\, + {n_{HBr}} = {n_{NaOH}}$ Lời giải chi tiết :
${n_{{C_6}{H_3}B{r_3}O}} = \frac{{33,1}}{{331}} = 0,1\,mol$ Khi cho hỗn hợp C6H5OH và HCl tác dụng với nước brom thì chỉ có phenol phản ứng theo phương trình: C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr 0,1 ← 0,1 → 0,3 → Dung dịch X: HCl; HBr (0,3 mol) Khi trung hòa hỗn hợp X bằng dung dịch NaOH: ${n_{{\text{HCl}}}}\, + {n_{HBr}} = {n_{NaOH}} = 1.0,5 = 0,5\,mol$ → ${n_{{\text{HCl}}}} = \,0,5 - {n_{HBr}} = 0,5 - 0,3 = 0,2\,\,mol$ → $m = {m_{{C_6}{H_5}OH}} + {m_{HCl}} = O,1.94 + 0,2.36,5 = 16,7$ gam
Câu 16 :
Đốt cháy 21 gam chất X là dẫn xuất benzen (CTPT trùng với CTĐGN), thu được 23,52 lit CO2 (đktc) và 10,8 gam H2O. Mặt khác, 21 gam X tác dụng vừa đủ với dung dịch NaOH thu được 27,6 gam muối. Số CTCT của X là:
Đáp án : D Phương pháp giải :
Áp dụng định luật bảo toàn khối lượng: ${m_X}\, + \,\,{m_{{O_2}}}\, = \,\,{m_{C{O_2}}} + \,{m_{{H_2}O}}$ Nhận thấy: 2$2.{n_{{O_2}}} < 2.{n_{C{O_2}}} + {n_{{H_2}O}}$→ trong X chứa O Áp dụng định luật bảo toàn nguyên tử: nO trong X = 2$2.{n_{C{O_2}}} + {n_{{H_2}O}} - 2.{n_{{O_2}}}$ nC trong X = ${n_{C{O_2}}}$ nH trong X = 2${n_{{H_2}O}}$ → nC : nH : nO +) Tính số mol NaOH phản ứng => các nhóm -OH trong X Lời giải chi tiết :
Vì đốt cháy X thu được CO2 và H2O → trong X chứa C, H và có thể có O ${n_{C{O_2}}} = \frac{{23,52}}{{22,4}}= 1,05\,mol;\,{n_{{H_2}O}} = \frac{{10,8}}{{18}} = 0,6\,\,mol$ Áp dụng định luật bảo toàn khối lượng: ${m_X} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}}$ → ${m_{{O_2}}}$ = 1,05.44 + 0,6.18 – 21 = 36 gam → ${n_{{O_2}}}$ = 1,125 mol Nhận thấy: $2.{n_{{O_2}}} < 2.{n_{C{O_2}}} + {n_{{H_2}O}}$→ trong X chứa O Áp dụng định luật bảo toàn nguyên tử: nO trong X = $2.{n_{C{O_2}}} + {n_{{H_2}O}} - 2.{n_{{O_2}}}$= 2.1,05 + 0,6 – 2.1,125 = 0,45 mol nC trong X = ${n_{C{O_2}}}$= 1,05 mol nH trong X = 2.${n_{{H_2}O}}$= 1,2 mol → nC : nH : nO = 1,05 : 1,2 : 0,45 = 7 : 8 : 3 → CTĐGN của X là C7H8O3 Vì CTPT của X trùng với CTĐGN → CTPT của X là C7H8O3 ${n_{{C_7}{H_8}{O_3}}} = \,\,\frac{{21}}{{140}}\,\, = \,\,0,15\,\,mol$ X tác dụng với dung dịch NaOH: Cứ thay thế 1 nguyên tử H bằng 1 nguyên tử Na thì khối lượng tăng: 23 – 1 = 22 Mà theo bài, khối lượng tăng 27,6 – 21 = 6,6 gam +)số mol NaOH phản ứng là: nNaOH = $\frac{{6,6}}{{22}}$ = 0,3 mol → ${n_{{C_7}{H_8}{O_3}}} = 2{n_{NaOH}}$ → trong X có 2 nhóm -OH tác dụng với NaOH → X có 2 nhóm -OH phenol và 1 nhóm -OH ancol hoặc X có 2 nhóm -OH phenol và 1 nhóm ete Các CTCT của X là TH1 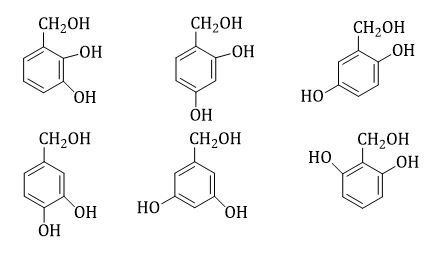 TH2: Thay -CH2OH bằng -OCH3 (6 công thức)
Câu 17 :
Cho 0,01 mol phenol tác dụng hoàn toàn với lượng dư dung dịch hỗn hợp HNO3 đặc và H2SO4 đặc. Phát biểu nào sau đây không đúng
Đáp án : A Phương pháp giải :
Tính theo PTHH Lời giải chi tiết :
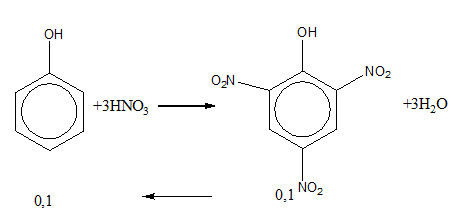
C6H5OH + 3HNO3 → C6H2(O2N)3OH + 3H2O 0,01 → 0,03 → 0,01 → maxit picric = 2,29 gam → A sai
Câu 18 :
Cho etanol, phenol lần lượt tác dụng với Na, dung dịch NaOH, dung dịch Br2. Số phản ứng xảy ra là
Đáp án : B Phương pháp giải :
Dựa vào tính chất hóa học của ancol – phenol trong sgk hóa 11 Lời giải chi tiết :
PTHH: C2H5OH + Na → C2H5ONa + 1/2 H2 C6H5OH + Na → C6H5ONa + 1/2H2↑ C6H5OH + NaOH → C6H5ONa + H2O
→ có 4 phản ứng xảy ra
Câu 19 :
Phản ứng giữa CO2 với dung dịch C6H5ONa xảy ra theo phương trình hóa học sau: CO2 + H2O + C6H5ONa → C6H5OH + NaHCO3. Phản ứng xảy ra được là do phenol có:
Đáp án : D Phương pháp giải :
Dựa vào tính chất: axit mạnh hơn đẩy axit yếu hơn ra khỏi muối tạo thành muối mới và axit mới yếu hơn axit ban đầu. Lời giải chi tiết :
Dựa vào tính chất: axit mạnh hơn đẩy axit yếu hơn ra khỏi muối tạo thành muối mới và axit mới yếu hơn axit ban đầu. Do đó axit cacbonic có tính axit mạnh hơn phenol.
Câu 20 :
Cho 11,28 gam phenol tác dụng với lượng dư dung dịch Br2, sau phản ứng kết thúc thu được m gam kết tủa trắng. Giá trị của m là:
Đáp án : D Phương pháp giải :
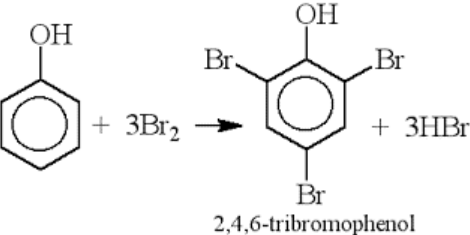
Tính toán theo phương trình hóa học: C6H5OH + 3Br2 → C6H2Br3OH + 3HBr Lời giải chi tiết :
C6H5OH + 3Br2 →C6H2Br3OH + 3HBr Ta có: nC6H2Br3OH = nphenol = 11,28 : 94 = 0,12 mol → mC6H2Br3OH = 0,12. 331 = 39,72 gam
Câu 21 :
0,5 mol phenol có khối lượng là:
Đáp án : B Phương pháp giải :
Từ công thức của phenol, áp dụng công thức m = n.M để tính khối lượng của phenol. Lời giải chi tiết :
Công thức của phenol là C6H5OH Khối lượng của phenol là mphenol = 0,5. 94 = 47 g
Câu 22 :
Để thu được 22,9 gam axit picric cần m gam phenol. Giá trị của m là ? Biết hiệu suất phản ứng đạt 94%.
Đáp án : D Phương pháp giải :
nphenol = nax picric = ? Lời giải chi tiết :
nax picric = 22,9 : 229 = 0,1 (mol)
Vì %H = 94% => mC6H5OH thực tế = mC6H5OH lí thuyết . 100% : %H = 9,4.100% : 94% = 10 (g)
Câu 23 :
Cho các chất : C6H5OH (X) ; C6H5CH2OH (Y) ; HOC6H4OH (Z) ; C6H5CH2CH2OH (T). Các chất đồng đẳng của nhau là :
Đáp án : B Phương pháp giải :
Ghi nhớ: Đồng đẳng là các chất hơn kém nhau 1 hay nhiều nhóm –CH2 trong phân tử và có tính chất hóa học tương tự nhau. Lời giải chi tiết :
C6H5CH2OH (Y); C6H5CH2CH2OH (T) cùng thuộc dãy đồng đẳng của ancol thơm
Câu 24 :
Một dung dịch chứa 6,1 g chất X là đồng đẳng của phenol đơn chức. Cho dung dịch trên tác dụng với nước brom dư thu được 17,95 g hợp chất Y chứa 3 nguyên tử Br trong phân tử. Biết hợp chất này có nhiều hơn 3 đồng phân cấu tạo. CTPT chất đồng đẳng của phenol là
Đáp án : C Phương pháp giải :
X+ 3Br2 → Y+ 3HBr x 3x 3x nBr2 = nHBr=x ĐLBTKL => mX + mBr2 = mhợp chất + mHBr 6,1 + 160.3x = 17,95 + 81.3x => x= 0,05 mol => MX Lời giải chi tiết :
X+ 3Br2 → Y+ 3HBr x 3x 3x nBr2 = nHBr=x ĐLBTKL => mX + mBr2 = mhợp chất + mHBr 6,1 + 160.3x = 17,95 + 81.3x => x= 0,05 mol => MX = 6,1 : 0,05=122 => X có thể là C2H5C6H4OH hoặc (CH3)2C6H3OH Biết hợp chất này có nhiều hơn 3 đồng phân cấu tạo =>
X chỉ có thể là (CH3)2C6H3OH
Câu 25 :
Phenol (công thức hóa học C6H5OH) là một hợp chất phổ biến trong bộ môn Hóa học. Đây là chất rắn ở dạng tinh thể, không màu, có mùi đặc trưng và nóng chảy ở nhiệt độ 43oC. Khi để bên ngoài không khí, phenol sẽ bị oxi hóa một phần chuyển sang màu hồng, và bị chảy rữa do hút ẩm. Phenol trước đây được chiết xuất từ nhựa than đá. Nhưng sau này, để đáp ứng nhu cầu lớn (khoảng 7 triệu tấn/năm), phenol được điều chế chủ yếu bằng cách oxi hóa các chế phẩm dầu mỏ. Trong công nghiệp, phenol được sử dụng rộng rãi để chế tạo nhựa, tơ sợi hóa học, thuốc diệt cỏ, thuốc nhuộm, thuốc nổ, thuốc sát trùng, thuốc chữa cúm, ... Khi tiếp xúc với phenol, cần tuyệt đối tránh để phenol chạm trực tiếp vào da, mắt và các cơ quan thuộc hệ hô hấp. Phenol là một chất rất độc, khi rơi vào da sẽ gây bỏng hóa học rất nặng. Ngoài ra, phần da chạm vào phenol rất dễ nổi mụn nước lâu ngày không khỏi. Bên cạnh đó, phenol cũng được chứng minh gây nhiều tác hại cho cơ thể người như rối loạn nhịp tim, tai biến, đau thận, đau gan, hôn mê. Trong Thế chiến thứ hai, phenol được sử dụng để làm chất độc giết người cho lò hơi ngạt trong các trại tập trung của Đức Quốc xã hoặc tiêm trực tiếp vào các nạn nhân khiến họ tử vong.
Câu 25.1
Hãy chọn các câu phát biểu đúng về phenol? (1) Hợp chất thuộc loại phenol là hợp chất có vòng benzen và có nhóm -OH. (2) Phenol là hợp chất chứa một hoặc nhiều nhóm hiđroxyl (-OH) liên kết trực tiếp với vòng benzen. (3) Phenol có tính axit nhưng nó là axit yếu hơn axit cacbonic. (4) Phenol tan trong nước lạnh vô hạn. (5) Phenol tan trong dung dịch NaOH tạo thành natri phenolat.
Đáp án : C Phương pháp giải :
Lý thuyết về phenol. Lời giải chi tiết :
(1) sai, loại hợp chất phenol là hợp chất có nhóm OH đính trực tiếp với vòng benzen. (2) đúng. (3) đúng, phản ứng chứng minh: C6H5ONa + H2O + CO2 → C6H5OH + NaHCO3. (4) sai, phenol ít tan trong nước lạnh. (5) đúng, PTHH: C6H5OH + NaOH → C6H5ONa + H2O. Vậy các phát biểu đúng là (2), (3), (5). Câu 25.2
Để rửa sạch chai lọ đựng phenol, nên dùng cách nào sau đây?
Đáp án : D Phương pháp giải :
Dựa vào tính chất hóa học của phenol. Lời giải chi tiết :
Để rửa sạch chai lọ đựng phenol ta nên dùng dung dịch NaOH sau đó rửa lại bằng nước vì phenol phản ứng với NaOH sinh ra C6H5ONa là chất tan nhiều trong nước, dễ dàng bị rửa trôi bằng nước. PTHH: C6H5OH + NaOH → C6H5ONa + H2O. Câu 25.3
Trong một lần làm thí nghiệm chẳng may do sơ ý, bạn An đã làm phenol đổ ra tay và bị bỏng. Cô giáo thấy vậy liền cấp cứu sơ bộ cho An như sau: “Rửa nhiều lần bằng glixerol cho tới khi màu da trở lại bình thường rồi rửa lại bằng nước, sau đó băng chỗ bỏng bằng bông tẩm glixerol”. Em hãy giải thích tại sao cô giáo lại làm như vậy?
Đáp án : B Phương pháp giải :
Dựa vào tính chất của phenol. Lời giải chi tiết :
Do sự tan của phenol trong glixerol lớn hơn rất nhiều trong da nên glixerol sẽ kéo/chiết dần phenol ra.
|













 => mC6H5OH lí thuyết = 0,1. 94 = 9,4 (g)
=> mC6H5OH lí thuyết = 0,1. 94 = 9,4 (g)