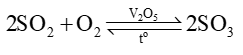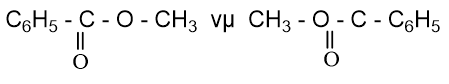Đề thi học kì 1 Hóa 11 Kết nối tri thức - Đề số 1Tổng hợp đề thi học kì 1 lớp 11 tất cả các môn - Kết nối tri thức Toán - Văn - Anh - Lí - Hóa - Sinh Câu 1: Cấu hình electron của nguyên tố sulfur (Z=16) là A. [Ne] 3s23p5 B. [Ne]3s23p4 C. [Ne]3s23p3 D. [Ne]3s23p5Đề bài
I. Trắc nghiệm
Chọn đáp án đúng
Câu 1 :
Cấu hình electron của nguyên tố sulfur (Z=16) là
Câu 2 :
Sulfur có các mức oxi hóa là:
Câu 3 :
Khi SO2 sinh ra từ việc đốt các nhiên liệu hóa thạch, các quặng sulfide là một trong các hợp chất gây ô nhiễm môi trường, do SO2 góp phần gây ra
Câu 5 :
Dãy chất nào sau đây là hợp chất hữu cơ
Câu 6 :
Nhận định nào sau đây không đúng?
Câu 7 :
Phản ứng hoá học của các hợp chất hữu cơ thường xảy ra
Câu 8 :
Quan sát phổ hồng ngoại (IR) của hợp chất X có công thức C2H5OH dưới đây, hãy chỉ ra peak nào giúp dự đoán X có nhóm –OH?
Câu 9 :
Khi tách và tinh chế chất lỏng dựa trên sự khác nhau về nhiệt độ sôi của các chất trong hỗn hợp ở áp suất nhất định, người ta thường sử dụng phương pháp nào sau đây?
Câu 10 :
Phương pháp kết tinh dùng để tách các chất
Câu 11 :
Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36 °C), heptane (sôi ở 98 °C), octane (sôi ở 126 °C) và nonane (sôi ở 151°C). Có thể tách riêng các chất đó bằng cách nào sau đây?
Câu 12 :
Acetylene là một hydrocarbon được dùng làm nhiên liệu trong đèn xì oxy-acetylene (khi tác dụng với oxygen) để hàn hay cắt kim loại. Kết quả phân tích nguyên tố của acetylene có 7,69% H về khối lượng. Phân tử khối của acetylene gấp 13 lần phân tử khối của hydrogen. Công thức phân tử của acetylene
Câu 13 :
Trong ruộng lúa, ao, hồ, ... thường chứa các vật thể hữu cơ. Khi các vật thể hữu cơ đó bị phân huỷ trong điều kiện không có oxygen sinh ra hydrocarbon (X) ở thể khí. Người ta đã lợi dụng hiện tượng này để làm các hầm biogas trong chăn nuôi gia súc, tạo khí (X) sử dụng đun nấu hoặc chạy máy, ... Công thức phân tử của (X) là, biết kết quả phân tích nguyên tố của (X) có 25% H về khối lượng. Phân tử khối của hợp chất này được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất.
Câu 14 :
Công thức phân tử của methyl formate và glucose lần lượt là C2H4O2 và C6H12O6. Công thức đơn giản nhất của hai chất này là
Câu 15 :
Từ phổ MS của ethanol, người ta xác định được ion phân tử [C2H6O+] có giá trị m/z bằng 46. Vậy, phân tử khối của ethanol là:
Câu 16 :
Thành phần phần trăm về khối lượng C, H, O tron phân tử methanol CH3OH lần lượt là
Câu 17 :
Có 4 loại cấu tạo mạch phân tử: (a) mạch hở không phân nhánh; (b) mạch hở phân nhánh; (c) mạch vòng không phân nhánh và (d) mạch vòng phân nhánh. Trong phân tử hợp chất hữu cơ, các nguyên tử carbon có thể liên kết với chính nó hình thành bao nhiêu loại mạch?
Câu 18 :
Chọn phát biểu là đúng theo thuyết cấu tạo hóa học?
Câu 19 :
Trong các dãy chất sau đây, dẫy nào gồm các chất là đồng đẳng của nhau
II. Tự luận
Lời giải và đáp án
I. Trắc nghiệm
Chọn đáp án đúng
Câu 1 :
Cấu hình electron của nguyên tố sulfur (Z=16) là
Đáp án : B Phương pháp giải :
Dựa vào Z = 16 để viết cấu hình của nguyên tố sulfur Lời giải chi tiết :
S (Z=16): 1s22s22p63s23p4 Đáp án B
Câu 2 :
Sulfur có các mức oxi hóa là:
Đáp án : B Phương pháp giải :
Dựa vào hóa trị của sulfur trong các hợp chất Lời giải chi tiết :
S có số oxi hóa lớn nhất là +6, thấp nhất là -2 Đáp án B
Câu 3 :
Khi SO2 sinh ra từ việc đốt các nhiên liệu hóa thạch, các quặng sulfide là một trong các hợp chất gây ô nhiễm môi trường, do SO2 góp phần gây ra
Đáp án : A Phương pháp giải :
SO2 là khí độc gây ra ô nhiễm môi trường góp phần gây ra hiện tượng mưa acid do \(S{O_2} + {O_2} + {H_2}O \to {H_2}S{O_4}\) Lời giải chi tiết :
Đáp án A
Đáp án : B Phương pháp giải :
\({\Delta _r}H_{298}^0 = \sum {\Delta _f}H_{298}^0(sp) - \sum {\Delta _f}H_{298}^0(cd)\) Nhiệt tạo thành của đơn chất bằng 0. Lời giải chi tiết :
\(\begin{array}{l}{\Delta _{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}} = 2{\Delta _{\rm{f}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}{\rm{(S}}{{\rm{O}}_3}) - 2{\Delta _{\rm{f}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}{\rm{(S}}{{\rm{O}}_2})\\{\rm{ = 2}} \times {\rm{(}} - 395,7) - 2 \times ( - 296,8)\\{\rm{ = }} - {\rm{197,8 (kJ)}}\end{array}\) Chọn B.
Câu 5 :
Dãy chất nào sau đây là hợp chất hữu cơ
Đáp án : C Phương pháp giải :
Hợp chất hữu cơ là các hợp chất của carbon, trừ một số hợp chất vô cơ như CO, CO2, muối carbonate, các cyanide, các carbide Lời giải chi tiết :
Đáp án C chứa các hợp chất hữu cơ
Câu 6 :
Nhận định nào sau đây không đúng?
Đáp án : D Phương pháp giải :
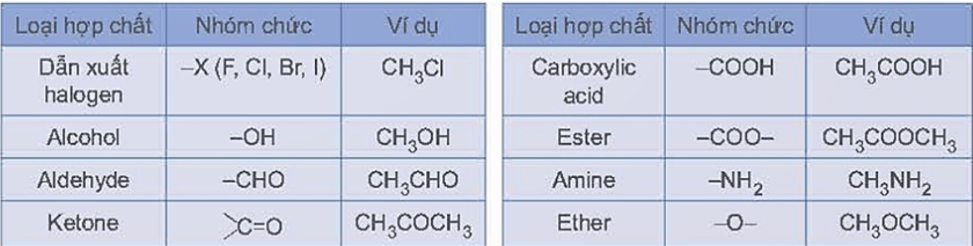
Một số loại nhóm chức cơ bản được thể hiện trong bảng sau:
Lời giải chi tiết :
Nhận định D không đúng vì: + CH3CH = O là aldehyde. + CH3COCH3 là ketone. → Chọn D
Câu 7 :
Phản ứng hoá học của các hợp chất hữu cơ thường xảy ra
Đáp án : D Phương pháp giải :
Dựa vào đăc điểm tính chất hóa học của hợp chất hữu cơ Lời giải chi tiết :
Phản ứng hóa học của hợp chất hữu cơ chậm, không hoàn toàn và không theo một hướng nhất định.
Câu 8 :
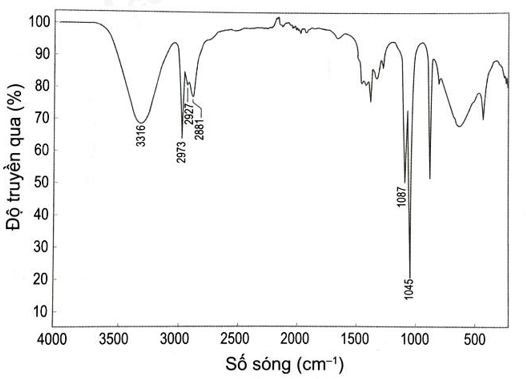
Quan sát phổ hồng ngoại (IR) của hợp chất X có công thức C2H5OH dưới đây, hãy chỉ ra peak nào giúp dự đoán X có nhóm –OH?
Đáp án : A Phương pháp giải :
Vùng tín hiệu đặc trưng của nhóm –OH là: 3650 – 3200 cm-1 Lời giải chi tiết :
Dựa vào phổ hồng ngoại IR ta thấy nhóm –OH có tín hiệu ở vùng 3316 cm-1
Câu 9 :
Khi tách và tinh chế chất lỏng dựa trên sự khác nhau về nhiệt độ sôi của các chất trong hỗn hợp ở áp suất nhất định, người ta thường sử dụng phương pháp nào sau đây?
Đáp án : A Phương pháp giải :
Dựa vào nguyên tắc của các phương pháp tách biệt và tinh chế hợp chất hữu cơ Lời giải chi tiết :
Khi tách và tinh chế chất lỏng dựa vào sự khác nhau về nhiệt độ sôi của các chất là phương pháp chưng cất. Đáp án A
Câu 10 :
Phương pháp kết tinh dùng để tách các chất
Đáp án : C Phương pháp giải :
Nguyên tắc của phương pháp kết tinh: Với hỗn hợp các chất rắn, người ta thường dựa vào độ tan khác nhau và sự thay đổi độ tan theo nhiệt độ của chúng để tách và tinh chế. Lời giải chi tiết :
Phương pháp kết tinh dùng để tách các chất có độ tan khác nhau. → Chọn C
Câu 11 :
Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36 °C), heptane (sôi ở 98 °C), octane (sôi ở 126 °C) và nonane (sôi ở 151°C). Có thể tách riêng các chất đó bằng cách nào sau đây?
Đáp án : D Phương pháp giải :
Chưng cất là phương pháp tách và tinh chế chất lỏng dựa trên sự khác nhau về nhiệt độ sôi của các chất trong hỗn hợp ở áp suất nhất định. Lời giải chi tiết :
Hỗn hợp các alkan trên đều có nhiệt độ sôi khác nhau, do đó có thể tách riêng các chất trên bằng cách chưng cất. → Chọn D.
Câu 12 :
Acetylene là một hydrocarbon được dùng làm nhiên liệu trong đèn xì oxy-acetylene (khi tác dụng với oxygen) để hàn hay cắt kim loại. Kết quả phân tích nguyên tố của acetylene có 7,69% H về khối lượng. Phân tử khối của acetylene gấp 13 lần phân tử khối của hydrogen. Công thức phân tử của acetylene
Đáp án : C Phương pháp giải :
Thiết lập công thức phân tử hợp chất hữu cơ (CxHyOzNt) từ dữ liệu phân tích nguyên tố và phân tử khối (M) được khái quát như sau: \({\rm{x = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{C}}}}}{{{\rm{12}}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{; y = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{H}}}}}{{\rm{1}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{; z = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{O}}}}}{{{\rm{16}}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{; t = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{N}}}}}{{{\rm{14}}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}\) Với x, y, z, t lần lượt là số nguyên tử C, số nguyên tử H, số nguyên tử O, số nguyên tử N; %mC, %mH, %mO, %mN lần lượt là % khối lượng của các nguyên tố C, H, O, N trong hợp chất hữu cơ. Lời giải chi tiết :
Gọi công thức phân tử của acetylene là CxHy. Ta có: %mH = 7,69% => %mC = 100% - 7,69% = 92,31% Vì phân tử khối của acetylene gấp 13 lần phân tử khối của hydrogen nên \({{\rm{M}}_{{\rm{Acetylene}}}} = {\rm{ }}13{{\rm{M}}_{{{\rm{H}}_{\rm{2}}}}} = 13 \times 2 = 26\) \(\begin{array}{l}{\rm{x = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{C}}}}}{{{\rm{12}}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{ = }}\frac{{92,31}}{{{\rm{12}}}} \times \frac{{26}}{{{\rm{100}}}} \approx 2\\{\rm{y = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{H}}}}}{{\rm{1}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{ = }}\frac{{7,69}}{{\rm{1}}} \times \frac{{26}}{{{\rm{100}}}} \approx 2\end{array}\) Vậy công thức phân tử của acetylene là C2H2
Câu 13 :
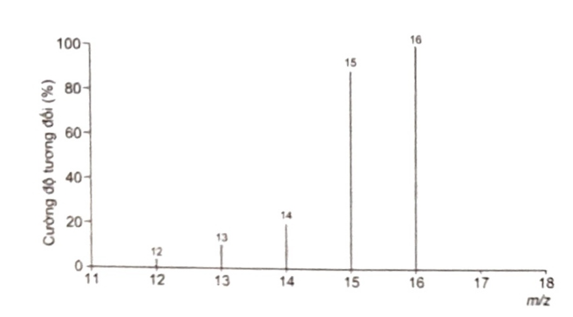
Trong ruộng lúa, ao, hồ, ... thường chứa các vật thể hữu cơ. Khi các vật thể hữu cơ đó bị phân huỷ trong điều kiện không có oxygen sinh ra hydrocarbon (X) ở thể khí. Người ta đã lợi dụng hiện tượng này để làm các hầm biogas trong chăn nuôi gia súc, tạo khí (X) sử dụng đun nấu hoặc chạy máy, ... Công thức phân tử của (X) là, biết kết quả phân tích nguyên tố của (X) có 25% H về khối lượng. Phân tử khối của hợp chất này được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất.
Đáp án : A Phương pháp giải :
Có thể dự đoán phân tử khối của hợp chất hữu cơ đơn giản bằng tín hiệu của mảnh ion phân tử (kí hiệu là [M+]). Mảnh ion phân tử này thường ứng với tín hiệu có giá trị m/z lớn nhất.Thiết lập công thức phân tử hợp chất hữu cơ (CxHyOzNt) từ dữ liệu phân tích nguyên tố và phân tử khối (M) được khái quát như sau:\({\rm{x = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{C}}}}}{{{\rm{12}}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{; y = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{H}}}}}{{\rm{1}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{; z = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{O}}}}}{{{\rm{16}}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{; t = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{N}}}}}{{{\rm{14}}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}\). Với x, y, z, t lần lượt là số nguyên tử C, số nguyên tử H, số nguyên tử O, số nguyên tử N; %mC, %mH, %mO, %mN lần lượt là % khối lượng của các nguyên tố C, H, O, N trong hợp chất hữu cơ. Lời giải chi tiết :
Gọi công thức phân tử của X là CxHy. Ta có: %mH = 25% => %mC = 100% - 25% = 75% Từ phổ khối lượng của (X), ta có: \({{\rm{M}}_{\rm{X}}} = 16\) \(\begin{array}{l}{\rm{x = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{C}}}}}{{{\rm{12}}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{ = }}\frac{{75}}{{{\rm{12}}}} \times \frac{{16}}{{{\rm{100}}}} = 1\\{\rm{y = }}\frac{{{\rm{\% }}{{\rm{m}}_{\rm{H}}}}}{{\rm{1}}} \times \frac{{\rm{M}}}{{{\rm{100}}}}{\rm{ = }}\frac{{25}}{{\rm{1}}} \times \frac{{16}}{{{\rm{100}}}} = 4\end{array}\) Vậy công thức phân tử của X là CH4.
Câu 14 :
Công thức phân tử của methyl formate và glucose lần lượt là C2H4O2 và C6H12O6. Công thức đơn giản nhất của hai chất này là
Đáp án : A Phương pháp giải :
Công thức đơn giản nhất cho biết tỉ lệ số nguyên tử của các nguyên tố có trong phân tử hợp chất hữu cơ (tỉ lệ các số nguyên tối giản). Lời giải chi tiết :
Xét tỉ lệ số nguyên tử của các nguyên tố có trong methyl formate (C2H4O2): \(2:4:2 = 1:2:1\) Xét tỉ lệ số nguyên tử của các nguyên tố có trong glucose (C6H12O6): \(6:12:6 = 1:2:1\) \( \Rightarrow \) Công thức đơn giản nhất của methyl formate và glucose là CH2O. → Chọn A.
Câu 15 :
Từ phổ MS của ethanol, người ta xác định được ion phân tử [C2H6O+] có giá trị m/z bằng 46. Vậy, phân tử khối của ethanol là:
Đáp án : C Lời giải chi tiết :
Ion [C2H6O+] có giá trị m/z bằng 46 nên phân tử khối của ethanol là 46.
Câu 16 :
Thành phần phần trăm về khối lượng C, H, O tron phân tử methanol CH3OH lần lượt là
Đáp án : C Phương pháp giải :
Dựa vào công thức tính % khối lượng của nguyên tố trong hợp chất Lời giải chi tiết :
\(\begin{array}{l}\% C = \frac{{12}}{{32}}.100\% = 37,5\% \\\% H = \frac{{1.4}}{{32}}.100\% = 12,5\% \\\% O = \frac{{16}}{{32}}.100\% = 50\% \end{array}\)
Câu 17 :
Có 4 loại cấu tạo mạch phân tử: (a) mạch hở không phân nhánh; (b) mạch hở phân nhánh; (c) mạch vòng không phân nhánh và (d) mạch vòng phân nhánh. Trong phân tử hợp chất hữu cơ, các nguyên tử carbon có thể liên kết với chính nó hình thành bao nhiêu loại mạch?
Đáp án : D Phương pháp giải :
Trong phân tử chất hữu cơ, carbon có hoá trị IV. Các nguyên tử carbon không những liên kết với nguyên tử của các nguyên tố khác mà còn có thể liên kết trực tiếp với nhau tạo thành mạch carbon (mạch hở không phân nhánh, mạch hở phân nhánh hoặc mạch vòng). Lời giải chi tiết :
Trong phân tử hợp chất hữu cơ, các nguyên tử carbon có thể liên kết với chính nó hình thành (a) mạch hở không phân nhánh; (b) mạch hở phân nhánh; (c) mạch vòng không phân nhánh; (d) mạch vòng phân nhánh. → Chọn D
Câu 18 :
Chọn phát biểu là đúng theo thuyết cấu tạo hóa học?
Đáp án : A Phương pháp giải :
Dựa vào thuyết cấu tạo hóa học Lời giải chi tiết :
Trong hợp chất hữu cơ, carbon có hóa trị IV, nó có thể liên kết với nguyên tử nguyên tố khác và liên kết với nhau để tạo thành mạch carbon gồm: nhánh, không nhánh và vòng. Đáp án A
Câu 19 :
Trong các dãy chất sau đây, dẫy nào gồm các chất là đồng đẳng của nhau
Đáp án : A Phương pháp giải :
Đồng đẳng là những hợp chất có thành phần phân tử hơn hoặc kém nhau một hay nhiều nhóm –CH2 – và có tính chất hóa học tương tự nhau. Lời giải chi tiết :
Đáp án A
Đáp án : A Phương pháp giải :
Hợp chất có cùng công thức phân tử khác nhau về công thức cấu tạo gọi là đồng phân của nhau Lời giải chi tiết :
Đáp án A
II. Tự luận
Phương pháp giải :
Dựa vào dấu hiệu xảy ra phản ứng hóa học Lời giải chi tiết :
(1) Ba2+ + CO32- → BaCO3↓ (2) Ba2+ + SO42- → BaSO4↓ (3) Mg2+ + CO32- → MgCO3↓ (4) Mg2+ + 2OH- → Mg(OH)2↓ (5) NH4+ + OH- → NH3↑ + H2O (6) H+ + OH- → H2O (7) 2H+ + CO32- → CO2↑ + H2O (8) H+ + HCO3- → CO2↑ +H (9) OH- + HCO3- → CO32- + H2O
Lời giải chi tiết :
(a) 10 mL dung dịch HCl 1 M, thêm nước để được 100 mL số mol HCl không thay đổi, thể tích tăng 10 lần \( \Rightarrow \) nồng độ giảm 10 lần \(\left. \begin{array}{l}HCl \to {H^ + } + C{l^ - }\\0,1 \to \,\,0,1\,M\end{array} \right\} \Rightarrow pH = - \lg \left[ {{H^ + }} \right] = - \lg (0,1) = 1\) (b) 10 mL dung dịch NaOH 1 M, thêm nước để được 100 mL số mol NaOH không thay đổi, thể tích tăng 10 lần \( \Rightarrow \) nồng độ giảm 10 lần \(\left. \begin{array}{l}NaOH \to N{a^ + } + O{H^ - }\\0,1\,\,\,\,\,\,\,\,\,\,\, \to \,\,\,\,\,\,\,\,\,\,\,0,1\,\,M\end{array} \right\} \Rightarrow \left[ {{H^ + }} \right] = \frac{{{{10}^{ - 14}}}}{{\left[ {O{H^ - }} \right]}} = {10^{ - 13}} \Rightarrow pH = - \lg \left[ {{H^ + }} \right] = - \lg ({10^{ - 13}}) = 13\)
|