Lý thuyết bài18: Hydrogen halide và hydrohalic acidxu hướng biến đổi nhiệt độ sôi hydrogen halide, biến đổi tính acid, ứng dụng, nhận biết ion halide Lý thuyết: Hydrogen halide và hydrohalic acid I. Hydrogen halide và hydrohalic acid 1. Hydrogen halide Hợp chất gồm nguyên tố halogen và nguyên tố hydrogen có dạng HX, được gọi chung là hydrogen halide. Hydrogen halide là hợp chất cộng hóa trị phân cực. Xu hướng phân cực giảm dần từ HF đến HI Nhiệt độ sôi tăng dần từ hydrogen chloride đến hydrogen iodide 2. Hydrohalic acid Trong dung dịch, hydrogen halide đều phân li ra ion H+ nên được gọi là hydrohalic acid (hay các acid HX) Ví dụ: Sự phân li của hydrogen chloride trong nước Tính acid của các dung dịch HX tăng theo dãy từ HF đến HI. II. Tính khử của một số ion halide X- Các hợp chất Cl-, Br-, I- phản ứng được với sulfuric đặc: Trong các phản ứng, ion Cl- không thể hiện tính khử còn Br-, I-bị khử thành các sản phẩm khác nhau. => Tính khử của ion X- thường tăng từ Cl- đến I- III. Ứng dụng của một số hydrogen halide 1. Ứng dụng của hydrogen fluoride Ứng dụng phổ biến của hydrogen fluoride là sản xuất các hợp chất HCFC sử dụng trong hệ thống làm lạnh - Dùng trong sản xuất cryolite, đóng vai trò “chất chảy” trong quá trình sản xuất nhôm từ aluminium oxit. - Sử dụng trong các quá trình chế biến dầu mỏ, trong công nghiệp, hạt nhân,… Bồn chứa hydrochloric acid ở một nhà máy 2. Ứng dụng của hydrogen chloride - Sản xuất vinyl chloride cung cấp cho ngành nhựa
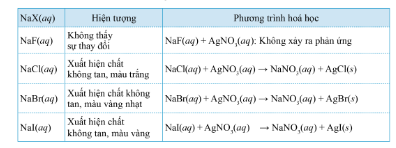
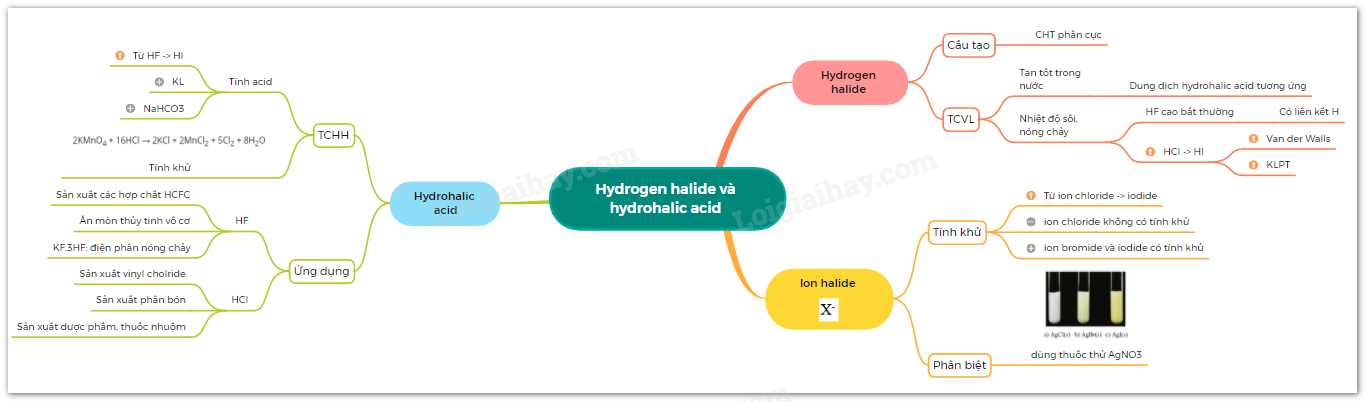
- Ammonium chloride để cung cấp cho ngành sản xuất phân bón - Các chloride kim loại cung cấp cho ngành hóa chất - Hợp chất hữu cơ chứa chlorine phục vị sản xuất dược phẩm, thuốc nhuộm. IV. Phân biệt các ion Halide X- - Sử dụng thuốc thử: silver nitrate Màu sắc của các silver halide không tan Sơ đồ tư duy
|



















Danh sách bình luận