Đề thi giữa kì 1 Hóa 11 Chân trời sáng tạo - Đề số 1Tải về Cho các phát biểu sau: (1) Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau. (2) Phản ứng bất thuận nghịch là phản ứng xảy ra theo 1 chiều xác định
Lựa chọn câu để xem lời giải nhanh hơn
Đề thi Câu 1: Cho các phát biểu sau: (1) Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau. (2) Phản ứng bất thuận nghịch là phản ứng xảy ra theo 1 chiều xác định (3) Cân bằng hóa học là trạng thái mà phản ứng đã xảy ra hoàn toàn. (4) Khi phản ứng thuận nghịch đạt trạng thái cân bằng hóa học, lượng các chất sẽ không đổi. (5) Khi phản ứng thuận nghịch đạt trạng thái cân bằng hóa học, phản ứng dừng lại. Các phát biểu sai là: A. 2,3. B. 3,4. C. 3,5. D. 4,5. Câu 2: Hằng số cân bằng K của phản ứng phụ thuộc vào A. áp suất. B. bản chất của các chất trong cân bằng và nhiệt độ. C. nồng độ. D. phân tử khối Câu 3: Cho cân bằng sau: 2SO2(k) + O2(k) ⇄ 2SO3(k); ∆H = -192,5kJ Để tăng hiệu suất của quá trình sản xuất SO3, người ta cần A. giảm nhiệt độ của hệ phản ứng, dùng xúc tác. B. giữ phản ứng ở nhiệt độ thường, giảm áp suất. C. tăng nhiệt độ của hệ phản ứng, dùng xúc tác. D. giảm nhiệt độ và tăng áp suất của hệ phản ứng. Câu 4: Dãy chất nào dưới đây chỉ gồm những chất điện li mạnh? A. HNO3, Cu(NO3)2, H3PO4, Ca(NO3)2. B. CaCl2, CuSO4, H2S, HNO3. C. H2SO4, NaCl, KNO3, Ba(NO3)2. D. KCl, H2SO4, HNO2, MgCl2. Câu 5: Theo thuyết Bronsted – Lowry chất nào sau đây là base? A. Al3+ B. Cl- C. H3PO4. D. CO32- Câu 6: Giá trị pH của dung dịch HCl 0,001M là A. 3. B. 11. C. 12. D. 2. Câu 7: Nạp đầy khi amoniac vào bình thuỷ tinh trong suốt, đậy bình NH3 bằng nút cao su có ống thuỷ tinh vuốt nhọn xuyên qua. Nhúng đầu ống thuỷ tinh vào một chậu thuỷ tinh chứa nước có pha thêm dung dịch phenolphthalein. Một lát sau, nước trong chậu phun vào bình thành những tia có màu hồng. Thí nghiệm này chứng tỏ được A. NH3 tan nhiều trong nước. B. NH3 là chất khí. C. NH3 có tính bazơ và tan nhiều trong nước. D. NH3 có mùi khai. Câu 8: Trong phản ứng giữa khí ammonia và khí hydrogen chloride thành ammonium chloride ở dạng khí trắng, ammonia đóng vai trò là: A. Acid. B. Base. C. Chất oxi hóa. D. Chất khử. Câu 9: Trong tự nhiên, nguyên tố nitrogen tồn tại chủ yếu ở dạng đồng vị nào sau đây? A. 14N. B. 13N. C. 15N. D. 12N. Câu 10: Áp suất riêng phần của khí nitrogen trong khí quyển là A. 0,21 bar. B. 0,01 bar. C. 0,78 bar. D. 0,28 bar. Câu 11: Cho sơ đồ chuyển hoá nitrogen trong khí quyển thành phân đạm: Số phản ứng thuộc loại oxi hoá-khử trong sơ đồ là A. 3. B. 1. C. 4. D. 2. Câu 12: Quá trình đốt cháy hỗn hợp hơi nhiên liệu và không khí trong động cơ khi đánh tia lửa điện sinh ra khí NO, một tác nhân gây ô nhiễm không khí. Tên gọi của NO là: A. Ammonia. B. Nitrogen dioxide. C. Nitrogen monoxide. D. Nitrogen. Câu 13: Cho các nhận định sau về cấu tạo phân tử nitric acid: (a) Liên kết O – H phân cực về oxygen. (b) Nguyên tử N có số oxi hóa là +5. (c) Nguyên tử N có hóa trị bằng 4. (d) Liên kết cho – nhận N → O kém bền. Số nhận định đúng là A. 1. B. 2. C. 3. D. 4. Câu 14: Cho các nhận định sau về tính chất hóa học của nitric acid: (1) có tính acid mạnh; (2) có tính acid yếu; (3) có tính oxi hóa mạnh; (4) có tính khử mạnh. Số nhận định đúng là A. 1. B. 2. C. 3. D. 4. Câu 15: Cho sơ đồ phản ứng : C + HNO3 (đ) \( \to \) CO2 + NO2 + H2O. Tổng hệ số cân bằng của phản ứng là : A. 12 B. 10 C. 11 D. 13 II. Tự luận Câu 1 (2 điểm): Hỗn hợp X gồm N2 và H2 có tỉ lệ mol tương ứng là 1 : 4. Nung nóng X trong bình kín ở nhiệt độ khoảng 450 °C có bột Fe xúc tác, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 4. Tính hiệu suất của phản ứng tổng hợp NH3. Câu 2: (2 điểm) Xét cân bằng của dung dịch NH3 0,1 M ở 25 °C: .\({\rm{N}}{{\rm{H}}_{\rm{3}}} + {{\rm{H}}_{\rm{2}}}{\rm{O}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{NH}}_4^ + + {\rm{O}}{{\rm{H}}^ - }{\rm{ }}{{\rm{K}}_{\rm{C}}}{\rm{ = 1,74}}{\rm{.1}}{{\rm{0}}^{ - 5}}\). Bỏ qua sự phân li của nước. Xác định giá trị pH của dung dịch trên. ---Hết--- Đáp án I. TRẮC NGHIỆM
Câu 1: Cho các phát biểu sau: (1) Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau. (2) Phản ứng bất thuận nghịch là phản ứng xảy ra theo 1 chiều xác định (3) Cân bằng hóa học là trạng thái mà phản ứng đã xảy ra hoàn toàn. (4) Khi phản ứng thuận nghịch đạt trạng thái cân bằng hóa học, lượng các chất sẽ không đổi. (5) Khi phản ứng thuận nghịch đạt trạng thái cân bằng hóa học, phản ứng dừng lại. Các phát biểu sai là: A. 2,3. B. 3,4. C. 3,5. D. 4,5. Phương pháp giải Dựa vào lí thuyết về cân bằng hóa học Lời giải chi tiết (1) đúng (2) đúng (3) sai (4) đúng (5) sai Đáp án C Câu 2: Hằng số cân bằng K của phản ứng phụ thuộc vào A. áp suất. B. bản chất của các chất trong cân bằng và nhiệt độ. C. nồng độ. D. phân tử khối Phương pháp giải Dựa vào các yếu tố ảnh hưởng đến hằng số cân bằng. Lời giải chi tiết Hằng số cân bằng K của phản ứng chỉ phụ thuộc vào bản chất của các chất trong cân bằng và nhiệt độ. Đáp án B. Câu 3: Cho cân bằng sau: 2SO2(k) + O2(k) ⇄ 2SO3(k); ∆H = -192,5kJ Để tăng hiệu suất của quá trình sản xuất SO3, người ta cần A. giảm nhiệt độ của hệ phản ứng, dùng xúc tác. B. giữ phản ứng ở nhiệt độ thường, giảm áp suất. C. tăng nhiệt độ của hệ phản ứng, dùng xúc tác. D. giảm nhiệt độ và tăng áp suất của hệ phản ứng. Phương pháp giải Dựa vào nguyên lí chuyển dịch Le – cha – tơ – lie Lời giải chi tiết Để tăng hiệu suất quá trình sản xuất SO3, tức là cân bằng chuyển dịch theo chiều thuận Phản ứng có ∆H = -192,5Kj < 0, phản ứng tỏa nhiệt cần gảm nhiệt độ để cân bằng chuyển dịch theo chiều thuận Phản ứng có sự chênh lệch mol khí, tổng mol khí tham gia nhiều hơn sản phẩm nên tăng áp suất để cân bằng chuyển dịch theo chiều thuận Đáp án D Câu 4: Dãy chất nào dưới đây chỉ gồm những chất điện li mạnh? A. HNO3, Cu(NO3)2, H3PO4, Ca(NO3)2. B. CaCl2, CuSO4, H2S, HNO3. C. H2SO4, NaCl, KNO3, Ba(NO3)2. D. KCl, H2SO4, HNO2, MgCl2. Phương pháp giải Chất điện li mạnh: acid mạnh, dung dịch base, dung dịch muối tan Lời giải chi tiết Đáp án C Câu 5: Theo thuyết Bronsted – Lowry chất nào sau đây là base? A. Al3+ B. Cl- C. H3PO4. D. CO32- Phương pháp giải Theo thuyết Bronsted – Lowry base là chất nhận proton H+ Lời giải chi tiết Đáp án B Câu 6: Giá trị pH của dung dịch HCl 0,001M là A. 3. B. 11. C. 12. D. 2. Phương pháp giải pH = -lg [H+] Lời giải chi tiết pH = -lg(0,001) = 3 Đáp án A Câu 7: Nạp đầy khí amoniac vào bình thuỷ tinh trong suốt, đậy bình NH3 bằng nút cao su có ống thuỷ tinh vuốt nhọn xuyên qua. Nhúng đầu ống thuỷ tinh vào một chậu thuỷ tinh chứa nước có pha thêm dung dịch phenolphthalein. Một lát sau, nước trong chậu phun vào bình thành những tia có màu hồng. Thí nghiệm này chứng tỏ được A. NH3 tan nhiều trong nước. B. NH3 là chất khí. C. NH3 có tính bazơ và tan nhiều trong nước. D. NH3 có mùi khai. Phương pháp giải Chất làm đổi màu phenolphthalein có tính base Lời giải chi tiết Đáp án C Câu 8: Trong phản ứng giữa khí ammonia và khí hydrogen chloride thành ammonium chloride ở dạng khí trắng, ammonia đóng vai trò là: A. Acid. B. Base. C. Chất oxi hóa. D. Chất khử. Phương pháp giải Phản ứng giữa khí NH3 và HCl là phản ứng acid – base, trong đó NH3 đóng vai trò base Lời giải chi tiết Đáp án B Câu 9: Trong tự nhiên, nguyên tố nitrogen tồn tại chủ yếu ở dạng đồng vị nào sau đây? A. 14N. B. 13N. C. 15N. D. 12N. Phương pháp giải: Nitrogen trong tự nhiên là hỗn hợp của hai đồng vị: (99,63%) và (0,37%). Lời giải chi tiết: Trong tự nhiên, nguyên tố nitrogen tồn tại chủ yếu ở dạng đồng vị 14N. Đáp án A. Câu 10: Áp suất riêng phần của khí nitrogen trong khí quyển là A. 0,21 bar. B. 0,01 bar. C. 0,78 bar. D. 0,28 bar. Phương pháp: Áp suất riêng phần là áp suất của một loại khí trong hỗn hợp khí tác động lên môi trường xung quanh. Trong một hỗn hợp các chất khí, mỗi khí có một áp suất riêng phần hay áp suất từng phần là áp suất của khí đó nếu giả thiết rằng một mình nó chiếm toàn bộ thể tích của hỗn hợp ban đầu ở cùng một nhiệt độ. Áp suất tổng của một hỗn hợp khí lý tưởng là tổng của các áp suất riêng phần của những khí trong hỗn hợp. Lời giải chi tiết: Trong tự nhiên, áp suất của khí quyển là 1 bar. Khí nitrogen chiếm khoảng 78% thể tích không khí, cũng tương đương với 78% về áp suất. Áp suất riêng phần của khí nitrogen trong khí quyển là 78% . 1 = 0.78 bar → Chọn C. Câu 11: Cho sơ đồ chuyển hoá nitrogen trong khí quyển thành phân đạm: Số phản ứng thuộc loại oxi hoá-khử trong sơ đồ là A. 3. B. 1. C. 4. D. 2. Phương pháp: Phản ứng oxi hóa khử là phản ứng hóa học, trong đó có sự chuyển electron giữa các chất trong phản ứng hay phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một số nguyên tố. Lời giải chi tiết: Các phản ứng (1), (2), (3) có sự thay đổi số oxi hóa của một số nguyên tố. Do đó các phản ứng này là phản ứng oxi hóa khử. → Chọn A.
Câu 12: Quá trình đốt cháy hỗn hợp hơi nhiên liệu và không khí trong động cơ khi đánh tia lửa điện sinh ra khí NO, một tác nhân gây ô nhiễm không khí. Tên gọi của NO là: A. Ammonia. B. Nitrogen dioxide. C. Nitrogen monoxide. D. Nitrogen. Lời giải chi tiết Đáp án C Câu 13: Cho các nhận định sau về cấu tạo phân tử nitric acid: (a) Liên kết O – H phân cực về oxygen. (b) Nguyên tử N có số oxi hóa là +5. (c) Nguyên tử N có hóa trị bằng 4. (d) Liên kết cho – nhận N → O kém bền. Số nhận định đúng là A. 1. B. 2. C. 3. D. 4. Phương pháp giải Dựa vào cấu tạo của nitric acid Lời giải chi tiết (a) đúng vì O có độ âm điện lớn hơn (b) đúng vì N thể hiện hóa trị 5 (c) sai (d) đúng Đáp án C Câu 14: Cho các nhận định sau về tính chất hóa học của nitric acid: (1) có tính acid mạnh; (2) có tính acid yếu; (3) có tính oxi hóa mạnh; (4) có tính khử mạnh. Số nhận định đúng là A. 1. B. 2. C. 3. D. 4. Phương pháp giải Dựa vào tính chất hóa học của HNO3 Lời giải chi tiết (1), (3) đúng Câu 15: Cho sơ đồ phản ứng : C + HNO3 (đ) \( \to \) CO2 + NO2 + H2O. Tổng hệ số cân bằng của phản ứng là : A. 12 B. 10 C. 11 D. 13 Phương pháp giải Cân bằng phương trình theo phương pháp thăng bằng electron Lời giải chi tiết \(\begin{array}{l}{C^o} \to {C^{ + 4}} + 4e|x1\\{N^{ + 5}} + 1e \to {N^{ + 4}}|x4\\C + 4HN{O_3} \to C{O_2} + 4N{O_2} + 2{H_2}O\end{array}\) Đáp án A II. TỰ LUẬN (4 điểm) Câu 1 (2 điểm): Hỗn hợp X gồm N2 và H2 có tỉ lệ mol tương ứng là 1 : 4. Nung nóng X trong bình kín ở nhiệt độ khoảng 450 °C có bột Fe xúc tác, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 4. Tính hiệu suất của phản ứng tổng hợp NH3 ? Phương pháp: Sử dụng công thức: \({\rm{H\% }} = \frac{{{{\rm{n}}_{{\rm{sp(tt)}}}}}}{{{{\rm{n}}_{{\rm{sp(lt)}}}}}} \times 100\% \) Lời giải chi tiết: Hỗn hợp X gồm N2 và H2 có tỉ lệ mol tương ứng là 1 : 4. Chọn \({{\rm{n}}_{{{\rm{N}}_{\rm{2}}}}} = 1{\rm{ (mol)}};{\rm{ }}{{\rm{n}}_{{{\rm{H}}_{\rm{2}}}}} = 4{\rm{ }}({\rm{mol}})\) Gọi x (mol) là số mol N2 phản ứng. Xét cân bằng:
Câu 2: (2 điểm) Xét cân bằng của dung dịch NH3 0,1 M ở 25 °C: \({\rm{N}}{{\rm{H}}_{\rm{3}}} + {{\rm{H}}_{\rm{2}}}{\rm{O}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{NH}}_4^ + + {\rm{O}}{{\rm{H}}^ - }{\rm{ }}{{\rm{K}}_{\rm{C}}}{\rm{ = 1,74}}{\rm{.1}}{{\rm{0}}^{ - 5}}\) Bỏ qua sự phân li của nước. Xác định giá trị pH của dung dịch trên. Phương pháp: Tổng quát, nếu có phản ứng thuận nghịch sau: aA+bB \( \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} \) cC +dD Khi phản ứng ở trạng thái cân bằng, ta có: \({{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[C]}}}^{\rm{c}}}{{{\rm{[D]}}}^{\rm{d}}}}}{{{{{\rm{[A]}}}^{\rm{a}}}{{{\rm{[B]}}}^{\rm{b}}}}}\) Trong đó [A], [B], [C] và [D] là nồng độ mol các chất A, B, C và D ở trạng thái cân bằng; a, b, c và d là hệ số tỉ lượng các chất trong phương trình hoá học. Tính nồng độ ion \({\rm{O}}{{\rm{H}}^ - }\)rồi sử dụng công thức pH = 14 – pOH. Lời giải chi tiết: Xét cân bằng: \({\rm{N}}{{\rm{H}}_{\rm{3}}}{\rm{ }} + {\rm{ }}{{\rm{H}}_{\rm{2}}}{\rm{O }} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{ NH}}_4^ + {\rm{ }} + {\rm{ O}}{{\rm{H}}^ - }{\rm{ }}\) Ban đầu (M): 0,1 0 0 Phản ứng (M): x ← x ← x Cân bằng (M): 0,1 - x x x Ta có: KC = \({\rm{1,74}}{\rm{.1}}{{\rm{0}}^{ - 5}}\) \(\begin{array}{l}\frac{{[{\rm{NH}}_4^ + ][{\rm{O}}{{\rm{H}}^ - }]}}{{[{\rm{N}}{{\rm{H}}_{\rm{3}}}]}} = {\rm{1,74}}{\rm{.1}}{{\rm{0}}^{ - 5}}\\ \Leftrightarrow \frac{{{{\rm{x}}^2}}}{{0,1 - {\rm{x}}}} = {\rm{1,74}}{\rm{.1}}{{\rm{0}}^{ - 5}}\\ \Rightarrow {\rm{x}} \approx 1,{31.10^{ - 3}}{\rm{ (M)}} \Rightarrow {\rm{[O}}{{\rm{H}}^ - }{\rm{] = }}1,{31.10^{ - 3}}{\rm{ (M)}}\\ \Rightarrow {\rm{pOH = - log}}1,{31.10^{ - 3}} \approx 2,88\\ \Rightarrow {\rm{pH = 14 - pOH = }}14 - 2,88 = 11,12\end{array}\)
|













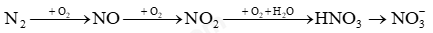
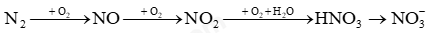



Danh sách bình luận