Đề kiểm tra 15 phút – Đề số 6 – Chương 4 – Hóa học 9Đáp án và lời giải chi tiết đề thi kiểm tra 15 phút – Đề số 6 – Chương 4 – Hóa học 9 Đề bài Câu 1 (1 điểm): Những chất nào sau đây là hợp chất hữu cơ: CH3Cl, C6H5Br, NaHCO3, C2H4O2, CH2O, CO2, NaCN? A.CO2, CH2O, C2H4O2. B. CH3Cl, C6H5Br, NaHCO3. C. CH3Cl, C6H5Br, C2H4O2, CH2O. D.NaCN, NaHCO3, C2H4O2. Câu 2 (1 điểm): Khẳng định nào sau đây luôn đúng? A.Hợp chất hữu cơ nhất thiết phải có cacbon, oxi. B.Thành phần hợp chất hữu cơ có thể có cacbon. C.Thành phần hợp chất hữu cơ nhất thiết phải có cacbon. D.Thành phần hợp chất hữu cơ nhất thiết phải có oxi. Câu 3 (1 điểm): Công thức cấu tạo hợp chất hữu cơ cho biết A.thành phần nguyên tố. B.thành phần của phân tử, và trật tự liên kết của các nguyên tử trong phân tử. C.khối lượng nguyên tử. D.số lượng nguyên tử mỗi nguyên tố. Câu 4 (1 điểm): Ở điều kiện tiêu chuẩn 1 lit chất hữu cơ X cân nặng 3,93 gam. Vậy khối lượng mol phân tử chất X là: A.88 B.46 C.74 D.60. Câu 5 (1 điểm): Công thức cấu tạo của C2H4O là: A.CH3 – CH = O. B.CH2 = O – OH. C. D. Cả A và C. Câu 6 (1 điểm): Thể tích khí C2H2 (đktc) sinh ra khí đem 8,533 gam đất đèn (trong đó có 75% CaC2) tác dụng hết với nước là (C = 12, Ca = 40) A.2,24 lít. B.1,866 lít C.7,466 lít. D.11,2 lít. Câu 7 (1 điểm): Đốt cháy 1 lít khí hidrocacbon X thu được 1 lít CO2 và 2 lít hơi nước (các thể tích đo ở điều kiện tiêu chuẩn). Công thức phân tử của X là: A.C2H2 B.C2H4 C.CH4 D.C6H6. Câu 8 (1 điểm): Biết rằng cacbon có hóa trị 4, hidro có hóa trị 1, ứng với công thức phân tử C4H10 số sông thức cấu tạo là: A.2 B.4 C.5 D.6. Lời giải chi tiết 1.Đáp án
2.Lời giải Câu 1: (C) Các chất: NaHCO3, CO2, NaCN không thuộc chất hữu cơ. Câu 2: (C) Thành phần hợp chất hữu cơ nhất thiết phải có cacbon. Câu 3: (B) Thành phần của phân tử và trật tự liên kết của các nguyên tử trong phân tử. Câu 4: (A) \(M = \dfrac{m.22,4} { V} = \dfrac{3,93.22,4}{1} = 88\) Câu 5: (D) Căn cứ vào hóa trị của C và H thì công thức cấu tạo CH3-CH=O và
Câu 6: (A) \(\eqalign{ & {m_{Ca{C_2}}} = 8,533.0,75 = 6,4gam\cr& \Rightarrow {n_{Ca{C_2}}} = {{6,4} \over {64}} = 0,1mol. \cr & Ca{C_2} + 2{H_2}O \to Ca{(OH)_2} + {C_2}{H_2} \cr & \Rightarrow {n_{{C_2}{H_2}}} = 0,1mol\cr& \Rightarrow {V_{{C_2}{H_2}}} = 0,1.22,4 = 2,24\,lit(đktc). \cr} \) Câu 7: (C) \({C_x}{H_y} + (x + {y \over 4}){O_2} \to xC{O_2} + {y \over 2}{H_2}O\) Tỉ lệ theo thể tích bằng tỉ lệ theo số mol. \( \Rightarrow x = {y \over 4} = 1.\) Vậy công thức phân tử của A là CH4. Câu 8: (A) HocTot.Nam.Name.Vn
|













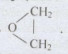
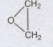 đều có cùng công thức phân tử C2H4O.
đều có cùng công thức phân tử C2H4O.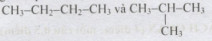

Danh sách bình luận