Bài 18. Nguyên tố nhóm IIA trang 58, 59, 60 SBT Hóa 12 Cánh diềuNguyên tố nhóm IIA được tìm thấy trong tự nhiên dưới dạng nào?
Lựa chọn câu để xem lời giải nhanh hơn
18.1 Nguyên tố nhóm IIA được tìm thấy trong tự nhiên dưới dạng nào? (1) Các cation M2+ trong nước ao hồ, nước ngầm. (2) Các khoáng vật ít tan như carbonate, sulfate, silicate. (3) Các hợp chất ít tan trong răng, xương động vật. A. (1) và (2). B. (1) và (3). C. (1), (2) và (3). D. (2) và (3). Phương pháp giải: Dựa vào trạng thái tự nhiên của kim loại IIA. Lời giải chi tiết: Đáp án C 18.2 Những phát biểu nào sau đây là đúng? (a) Số oxi hóa của các nguyên tố kim loại nhóm IIA trong hợp chất là … hoặc +2. (b) Beryllium là kim loại nhẹ nhất trong các kim loại nhóm IIA. (c) Magnesium là kim loại có nhiệt độ nóng chảy thấp nhất trong nhóm IIA. (d) Các ki loại nhóm IIA đều có cấu trúc mạng tinh thể lập phương tâm khối. (e) Các kim loại nhóm IIA đều dẫn điện. Phương pháp giải: Dựa vào tính chất vật lí của kim loại IIA. Lời giải chi tiết: Đáp án: c, e (a) Sai vì số oxi hóa của các nguyên tố nhóm IIA trong hợp chất chỉ là +2. (b) Sai vì Ca là kim loại nhẹ nhất trong nhóm IIA. (c) Đúng. (d) Sai vì các kim loại nhóm IIA không có cùng một kiểu mạng tinh thể. (e) Đúng. 18.3 Dãy các kim loại nào sau đây tác dụng nhanh với nước ở điều kiện thường? A. Be, Na, Ba. B. Mg, Ca, Ba. C. Li, Ca, Ba. D. Sr, Sn, Ba. Phương pháp giải: Dựa vào tính chất hóa học của kim loại IA, IIA. Lời giải chi tiết: Li, Ca, Ba có thể tác dụng nhanh với nước ở điều kiện thường. Đáp án C 18.4 Barium phản ứng với nước dễ dàng hơn so với magnesium ở điều kiện thường là do các nguyên nhân nào sau đây? (1) Barium có tính khử mạnh hơn magnesium. (2) Độ tan của barium hydroxide trong nước cao hơn nhiều so với magnesium hydroxide. (3) Bọt khí hydrogen sinh ra bám trên bề mặt magnesium nhiều hơn, cản trở phản ứng tiếp diễn. A. (1). B. (1), (2) và (3). C. (1) và (3). D. (1) và (2). Phương pháp giải: Dựa vào tính chất hóa học của kim loại. Lời giải chi tiết: Ba có tính khử mạnh hơnn magnesium và độ tân của Ba(OH)2 trong nước cao hơn nhiều so với magnesium hydroxide. Đáp án D 18.5 Thực hiện phản ứng giữa các dung dịch sau: a) Potasium carbonate và calcium hydroxide. b) Sodium phosphate và barium chloride. c) Magnesium hydrogencarbonate và sulfuric acid. d) Sodium hydrogencarbonate và barium hydroxide. e) Barium hydroxide và nitric acid. Những phản ứng nào thu được kết tủa? Viết phương trình hóa học của các phản ứng xảy ra. Phương pháp giải: Dựa vào tính chất hóa học của kim loại IIA. Lời giải chi tiết: Đáp án: a) b) d) PTHH: a) K2CO3 (aq) + Ca(OH)2 (aq) → 2KOH (aq) + CaCO3 (s) b) 2Na3PO4 (aq) + 3BaCl2 (aq) → 6NaCl (aq) + Ba3(PO4)2 (s) c) Mg(HCO3)2 (aq) + H2SO4 (aq) → MgSO4 (aq) + 2H2O (l) + 2CO2 (g) d) NaHCO3 (aq) + Ba(OH)2 (aq) → NaOH (aq) + BaCO3 (s) + H2O (l) e) Ba(OH)2 (aq) + 2HNO3 (aq) → Ba(NO3)2 (aq) + 2H2O (l) 18.6 Những phát biểu nào sau đây về ứng dụng của một số hợp chất của calcium là đúng? (a) Vôi tôi và vôi sống đều có thể dùng để khử chua đất trong nông nghiệp. (b) Đá vôi và thạch cao đều được dùng trong sản xuất vật liệu xây dựng. (c) Khoáng vật apatite được khai thác để sản xuất phân đạm. (d) Vôi tôi có thể được dùng để làm mềm nước cứng. (e) Thạch cao còn được dùng trong y tế như bó bột cô định xương. Phương pháp giải: Dựa vào ứng dụng của hợp chất nhóm IIA. Lời giải chi tiết: Đáp án: (a), (b), (d), (e). (c) Sai vì apatite dùng để sản xuất phân lân. 18.7 Tìm hiểu và cho biết vai trò của calcium đối với cơ thể người và các vấn đề sức khỏe có thể mắc phải khi thiếu hụt calcium. Liệt kê một số thực phẩm phù hợp để cung cấp calcium cho cơ thể. Phương pháp giải: Dựa vào ứng dụng của hợp chất nhóm IIA. Lời giải chi tiết: a) Vai trò của calcium với cơ thể người: - Một số hợp chất không tan của calcium cấu tạo nên xương và răng, giúp phát triển, ổn định xương và răng. - Một số hợp chất tan của calcium giúp ổn định chức năng truyền dẫn tín hiệu thần kinh đến tế bào, chức năng co giãn của cơ bắp (bao gồm cả cơ tim) b) Các vẫn đề sức khỏe có thể mắc phải khi thiếu hụt calcium: 1. Thiếu calcium gây các vấn đề về cơ Một người bị thiếu calcium có thể gặp các vấn đề như co thắt, đau nhức cơ với các biểu hiện như: Đau đùi khi đi bộ hoặc di chuyển, cảm giác tê bì ở cánh tay, bàn tay, bàn chân… 2. Cảm giác mệt mỏi Thiếu calcium có thể dẫn đến cảm giác kiệt sức và mệt mỏi. Bạn có thể gặp phải các triệu chứng uể oải và thiếu năng lượng trầm trọng, choáng váng, chóng mặt và sương mù não đặc trưng bởi thiếu tập trung, hay quên và lú lẫn... Sự thiếu hụt này cũng có thể dẫn đến mất ngủ. 3. Tác động đến da và tóc Calcium là một chất dinh dưỡng quan trọng cho tóc và da. Nếu không có đủ chất dinh dưỡng này có thể dẫn đến da khô, tóc khô, móng tay dễ gãy… Các rối loạn tự miễn dịch mãn tính như eczema và bệnh vẩy nến cũng có thể khởi phát do thiếu hụt calcium . 4. Phát triển loãng xương Xương cần hàm lượng calcium rất cao để duy trì sự chắc khỏe. Thiếu calcium gây giảm mật độ khoáng xương, dẫn đến loãng xương. Thiếu calcium tổng thể có thể làm cho xương giòn và dễ bị gãy. 5. Hội chứng tiền kinh nguyệt nghiêm trọng (PMS) Mức độ calcium trong cơ thể thấp hơn cũng có liên quan đến hội chứng tiền kinh nguyệt (PMS). Các nhà nghiên cứu đã xác nhận rằng nếu một người có mức calcium và vitamin D thấp trong nửa sau của chu kỳ kinh nguyệt, có thể có các triệu chứng của PMS tăng cao. 6. Vấn đề nha khoa Khi cơ thể thiếu calcium , sẽ làm ảnh hưởng tới sức khỏe của răng, có thể dẫn đến nhiều vấn đề răng miệng như: Sâu răng, chân răng yếu... 7. Trầm cảm Một số nghiên cứu cho rằng sự thiếu hụt calcium có liên quan đến rối loạn tâm trạng, bao gồm cả trầm cảm. Tuy nhiên không có đủ bằng chứng liên quan đến điều này, nhưng các chuyên gia cho rằng có thể cả hai tình trạng này có liên quan đến nhau. c) Một số thực phẩm phù hợp để cung cấp calcium cho cơ thể: sữa, ngũ cốc, các loại hạt rau cải, hải sản… Lưu ý: Ngoài việc bổ sung calcium cho cơ thể bằng cách ăn các thực phẩm chứa nhiều calcium phù hợp, cơ thể cũng cần tổng hợp/ bổ sung đủ lượng vitamin D để việc chuyển hóa calcium được hiệu quả. 18.8 Một học sinh thực hiện các thí nghiệm để nhận biết hai dung dịch chất X và chất Y, thu được một số kết quả như sau: - Dung dịch chất X và chất Y đều làm dung dịch phenolphtalein chuyển sang màu hồng. - Trộn X và Y thu được kết tủa trắng. - Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím. Mỗi kết luận sau đây của học sinh đó về chất X và chất Y là đúng hay sai? Biết mỗi chất X. Y đều chỉ chứa một loại cation và một loại anion. (a) Chất X có chứa cation Ba2+, chất Y chứa cation K+. (b) Chất X không thể là barium chloride. (c) Chất Y phải là potassium carbonate. (d) Chất kết tủa màu trắng phải là hợp chất của barium. Phương pháp giải: Dựa vào tính chất hóa học của kim loại IIA. Lời giải chi tiết: (a) Đúng vì X cháy cho ngọn lửa màu lục, Y cháy cho ngọn lửa màu tím. (b) Đúng vì X chuyển phenolphtalein sang màu hồng. (c) Sai, Y có thể là KHCO3, K2SO3, K3PO4… (d) Đúng vì các hợp chất của K (Y) tan trong nước. 18.9 Nhiệt độ phân hủy thành oxide của các muối carbonate của kim loại nhóm IIA giảm dần theo dãy: A. MgCO3, CaCO3, SrCO3, BaCO3. B. BaCO3, SrCO3, CaCO3, MgCO3. C. BaCO3, CaCO3, SrCO3, MgCO3. D. MgCO3, BaCO3, SrCO3, CaCO3. Phương pháp giải: Dựa vào tính chất hóa học của hợp chất nhóm IIA. Lời giải chi tiết: Đáp án: B: độ bền nhiệt của các muối carbonate giảm dần từ BaCO3 tới MgCO3. 18.10 Xét các phản ứng phân hủy sau: CaCO3 (s) \( \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} \) CaO (s) + CO2 (g) (1) BaCO3 (s) \( \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} \) BaO (s) + CO2 (g) (2) Biến thiên enthalpy chuẩn (\({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)) của phản ứng thuận ở mỗi cân bằng (1) và (2) khi phân hủy 1 mol mỗi chất lần lượt có giá trị là 108,7 kJ và 271,5 kJ. Những phát biểu nào sau đây là đúng? (a) Nhiệt lượng tỏa ra khi phân hủy 1 mol BaCO3 lớn hơn nhiệt lượng tỏa ra khi phân hủy 1 mol CaCO3. (b) BaCO3 bị phân hủy ở nhiệt độ cao hơn CaCO3. (c) Khi tăng nhiệt độ, cả hai phản ứng đều dịch chuyển theo chiều thuận. (d) CO2 cần được lấy ra khỏi lò nung để tăng hiệu suất của phản ứng. Phương pháp giải: Dựa vào biến thiên enthalpy của phản ứng. Lời giải chi tiết: Đáp án: (b), (c), (d) (a) Sai vì 2 phản ứng đều thu nhiệt. (b) Đúng vì biến thiên enthalpy chuẩn của phản ứng (2) lớn hơn của phản ứng (1). (c) Đúng vì 2 phản ứng đều thu nhiệt. (d) Đúng vì giảm nồng độ CO2 thì cân bằng chuyển dịch theo chiều thuận. 18.11 Beryllium carbonate (BeCO3) khan là chất bột màu trắng, dễ phân hủy ngay trong điều kiện thường, tạo thành beryllium oxide. Do đó, BeCO3 thường được bảo quản trong khí quyển tạo bởi chất X. Giống như các muối carbonate của các kim loại nhóm IIA khác, BeCO3 ít tan trong nước; tuy nhiên, điểm khác biệt là chất này dễ bị thủy phân tạo thành các dạng tồn tại khác của beryllium như Be(OH)32-, Be(OH)42-. Điều này chủ yếu là do cation Be2+ có bán kính nhỏ hơn nhiều so với các cation kim loại cùng nhóm IIA. Việc thường xuyên hít phải BeCO3 hay BeO đều có thể dẫn tới ung thư phổi. Nếu đi vào cơ thể, các cation Be2+ có thể vô hiệu hóa chức năng của các enzyme, đặc biệt là các enzyme chứa phức chất có nguyên tử trung tâm được hình thành từ cation Mg2+. Mỗi phát biểu sau đây là đúng hay sai? (a) Phần trăm khối lượng của beryllium trong beryllium carbonate tinh khiết khan là 6,25%. (b) Khí X là carbon dioxide. (c) Mật độ điện tích của ion bằng điện tích của ion chia cho thể tích của ion đó. Ion được coi có dạng cầu nên thể tích của ion tỉ lệ với lũy thừa 3 của bán kính ion. (d) Cation Be2+ có khả năng thay thế nguyên tử trung tâm magnesium của phức chất trong một số enzyme, tạo phức chất bền hơn. Phương pháp giải: Dựa vào tính chất hóa học của kim loại IIA. Lời giải chi tiết: (a) Sai vì %Be= \(\frac{{9.2}}{{9.2 + 12 + 16.3}}.100\)= 23,08 % (b) Đúng. (c) Sai, Be2+ có bán kính nhỏ → thể tích nhỏ → mật độ điện tích lớn hơn so với Ca2+. (d) Đúng. 18.12 a) Barium nitrate là hợp chất cộng hóa trị hay hợp chất ion, là chất dễ tan hay ít tan trong nước? b) Hoàn thành các phương trình hóa học sau: (2) Ba(NO3)2 (aq) + Na2SO4 (aq) → ? c) Độ tan trong nước của Ba(NO3)2 ở 10 oC và 20 oC lần lượt là 6.67 g/100 g nước và 9,02 g/100 g nước. Khi đưa 109,02 g dung dịch Ba(NO3)2 bão hòa ở 20 oC về 10 oC thì thu được bao nhiêu gam tinh thể Ba(NO3)2.6H2O kết tinh? d) Cho các hóa chất cơ bản sau: dung dịch NaOH, dung dịch HCl, dung dịch H2SO4, dung dịch NaCl. Hóa chất nào trong các hóa chất trên có thể được dùng để nhận biết được ion Ba2+ trong dung dịch barium nitrate? Viết phương trình hóa học minh họa. Phương pháp giải: Dựa vào tính chất hóa học của hợp chất nhóm IIA. Lời giải chi tiết: a) Barium nitrate là hợp chất ion, là chất dễ tan trong nước. b) Hoàn thành các phương trình hóa học sau: c) Trong 109,02 g dung dịch Ba(NO3)2 bão hòa ở 20 oC có mBa(NO3)2 = x (g) \(\frac{x}{{109,02 - x}}.100 = 9,02\) → mBa(NO3)2 = x= 9,02 g → mH2O= 100 g Gọi số mol Ba(NO3)2.6H2O kết tinh là a → ở 10 oC, mBa(NO3)2 = 9,02 - 261a mH2O= 100 - 6a \(\frac{{{\rm{9,02 - 261a}}}}{{{\rm{100 - 6}}{\rm{.18a}}}}{\rm{.100 = 6,67}}\) → a= 9,26.10-3 Vậy, khối lượng Ba(NO3)2.6H2O kết tinh là 369a= 3,42 g d) Ba2+ có kết tủa với gốc \(SO_4^{2 - }\)nên có thể dùng H2SO4 để nhận biết barium nitrate theo phản ứng sau: Ba(NO3)2 + H2SO4 → BaSO4 + 2HNO3 Kết tủa BaSO4 rất bền nên không tan trong các acid thông thường. 18.13 Gói làm nóng thức ăn (FRH: Flameless Ration Heater) được phát minh nhằm hâm nóng các bữa ăn tiện lợi cho người lính trên chiến trường. Một số gói lẩu tự sôi cũng sử dụng công nghệ này. FRH có thành phần chính gồm bột kim loại Mg trộn với một lượng nhỏ bột Fe và NaCl. Khi sử dụng, chỉ cần cho khoảng 30 mL nước vào hỗn hợp FRH, hỗn hợp này phản ứng mãnh liệt theo phương trình Mg + 2H2O → Mg(OH)2 + H2 và tỏa rất nhiều nhiệt, đủ để làm nóng thức ăn nhanh chóng. a) Một gói FRH chứa khoảng 8 gam hỗn hợp (Mg 90%, Fe 4% và NaCl 4% về khối lượng) có thể tỏa ra tối đa bao nhiêu nhiệt để làm nóng? Biết rằng enthalpy tạo thành chuẩn () của Mg(OH)2 (s) và H2O (l) lần lượt là -928,4 kJ mol-1 và-285,8 kJ mol-1. Gói FRH trên có đủ làm nóng 300 g súp từ 30 oC lên 100 oC hay không? Biết nhiệt dung của súp khoảng 4,2 J g-1 C-1, giả sử gói súp chỉ nhận được 50% lượng nhiệt tối đa tỏa ra, phần nhiệt còn lại làm nóng các vật dụng khác và thất thoát vào môi trường. b) Magnesium phản ứng chậm với nước ở nhiệt độ thường, giải thích vì sao magnesium trong gói FRH lại có thể phản ứng nhanh chóng với nước. c) Vì sao người ta chỉ dùng khoảng 30 mL nước mà ko dùng lượng nước nhiều hơn? Phương pháp giải: Dựa vào tính chất của hợp chất nhóm IIA Lời giải chi tiết: a) Mg (s) + 2H2O (l)→ Mg(OH)2 (s) + H2 (g) (1) \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)= -928,4 - (-285,8)= -642,6 kJ nMg= \(\frac{{8.\frac{{90}}{{100}}}}{{24}}\)= 0,3 mol → Q tỏa= 0,3.642,6= 192,78 kJ Để làm nóng 300 g súp từ 30 oC lên 100 oC Q thu = 300.(100-30).4,2/ 1000= 88,2 kJ Vì thất thoát nhiệt 50% nên thực tế Q cần = 88,2 *2= 176,4 kJ So sánh Q tỏa > Q cần nên gói FRH trên đủ làm nóng 300 g súp từ 30 oC lên 100 oC. b) Magnesium phản ứng chậm với nước ở nhiệt độ thường do các bọt khí hydrogen bám trên bề mặt magnesium ngăn cản magnesium tiếp xúc với nước. Trong gói FRH, magnesium lại có thể phản ứng nhanh chóng với nước do có mặt Fe tạo thành pin Galvani (trong dung dịch chất điện ly NaCl). Khi đó, hydrogen thoát ra trên bề mặt Fe nên diện tích tiếp xúc của Mg với nước tăng lên. c) Nếu dùng lượng nước nhiều hơn 30 mL thì nhiệt tỏa ra cần cung cấp cho lượng nước dư nóng lên nên nhiệt độ của đồ ăn giảm đi, giảm hiệu quả đun nóng của gọi FRH.
|













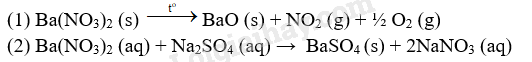

Danh sách bình luận