Trắc nghiệm Bài 9. Liên kết ion - Hóa 10 Chân trời sáng tạoĐề bài
Câu 1 :
Liên kết hóa học trong NaCl được hình thành là do
Câu 2 :
Muối ăn ở thể rắn là:
Câu 3 :
Các ion và nguyên tử 9F-, 10Ne, 11Na+ giống nhau về
Câu 4 :
Cấu hình electron nguyên tử X và Y lần lượt là 1s22s22p63s23p64s1 và 1s22s22p5 Liên kết hoá học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết.
Câu 5 :
X thuộc chu kì 3, nhóm IA, Y thuộc chu kì 3, nhóm VIIA. Công thức phân tử và bản chất liên kết của hợp chất giữa X và Y là
Câu 6 :
Hợp chất trong phân tử có liên kết ion là
Câu 7 :
Khi phản ứng hoá học xảy ra giữa những nguyên tử có cấu hình electron ở trạng thái cơ bản là 1s22s1 và 1s22s22p5 thì liên kết này là
Câu 8 :
Liên kết ion là loại liên kết hóa học được hình thành nhờ lực hút tĩnh điện giữa các phần tử nào sau đây?
Câu 9 :
Tính chất nào sau đây là tính chất của hợp chất ion?
Câu 10 :
Dãy gồm các phân tử đều có liên kết ion là
Lời giải và đáp án
Câu 1 :
Liên kết hóa học trong NaCl được hình thành là do
Đáp án : D Lời giải chi tiết :
Liên kết trong phân tử NaCl là liên kết ion, do vậy sự hình thành NaCl phải là sự cho nhận e của cation (Na+) và anion (Cl-)
Câu 2 :
Muối ăn ở thể rắn là:
Đáp án : C Lời giải chi tiết :
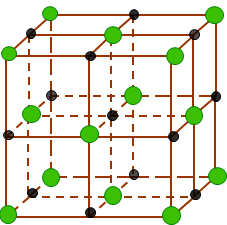
Ở thể rắn, NaCl tồn tại dưới dạng tinh thể ion. Trong mạng tinh thể NaCl, các ion Na+ và Cl- được phân bố luân phiên đều đặn trên các đỉnh của các hình lập phương nhỏ.
Câu 3 :
Các ion và nguyên tử 9F-, 10Ne, 11Na+ giống nhau về
Đáp án : B Phương pháp giải :
Viết cấu hình e, xác định số p, số e, số n, số khối của từng ion và nguyên tử Lời giải chi tiết :
9F-: (Z = 9): 1s22s22p6 => Có 10e, 9p 10Ne: (Z = 10): 1s22s22p6 => Có 10e, 10p 11Na+ (Z = 11): 1s22s22p6 => Có 10e, 11p
Câu 4 :
Cấu hình electron nguyên tử X và Y lần lượt là 1s22s22p63s23p64s1 và 1s22s22p5 Liên kết hoá học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết.
Đáp án : C Lời giải chi tiết :
X thuộc nhóm IA là kim loại điển hình Y thuộc nhóm VIIA là phi kim điển hình => liên kết giữa X và Y là liên kết ion
Câu 5 :
X thuộc chu kì 3, nhóm IA, Y thuộc chu kì 3, nhóm VIIA. Công thức phân tử và bản chất liên kết của hợp chất giữa X và Y là
Đáp án : B Lời giải chi tiết :
X thuộc nhóm IA là kim loại điển hình, điện tích 1+ Y thuộc nhóm VIIA là phi kim điển hình, điện tích 1- => CT là XY, liên kết giữa X và Y là liên kết ion
Câu 6 :
Hợp chất trong phân tử có liên kết ion là
Đáp án : A Lời giải chi tiết :
Liên kết ion là lực hút tĩnh điện giữa 2 ion mang điện tích trái dấu NH4Cl được tạo thành từ ion NH4+ và Cl-
Câu 7 :
Khi phản ứng hoá học xảy ra giữa những nguyên tử có cấu hình electron ở trạng thái cơ bản là 1s22s1 và 1s22s22p5 thì liên kết này là
Đáp án : C Lời giải chi tiết :
1s22s1 thuộc nhóm IA là kim loại điển hình 1s22s22p5 thuộc nhóm VIIA là phi kim điển hình => liên kết giữa 2 nguyên tố trên là liên kết ion
Câu 8 :
Liên kết ion là loại liên kết hóa học được hình thành nhờ lực hút tĩnh điện giữa các phần tử nào sau đây?
Đáp án : A Lời giải chi tiết :
Lực hút tĩnh điện giữa các ion mang điện tích trái dấu trong phân tử tạo ra liên kết => Lực hút tĩnh điện giữa cation và anion
Câu 9 :
Tính chất nào sau đây là tính chất của hợp chất ion?
Đáp án : B Lời giải chi tiết :
Trong tinh thể ion, giữa các ion có lực hút tĩnh điện rất mạnh nên các hợp chất ion thường là chất rắn, khó nóng chảy
Câu 10 :
Dãy gồm các phân tử đều có liên kết ion là
Đáp án : C Phương pháp giải :
Liên kết ion tạo bởi kim loại điển hình và phi kim điển hình Lời giải chi tiết :
A. Sai vì cả 4 chất đều là liên kết cộng hóa trị B. Sai vì HCl, H2S, N2O là liên kết cộng hóa trị C. Đúng D. Sai vì H2SO4, H3PO4, HCl là liên kết cộng hóa trị
|













Danh sách bình luận