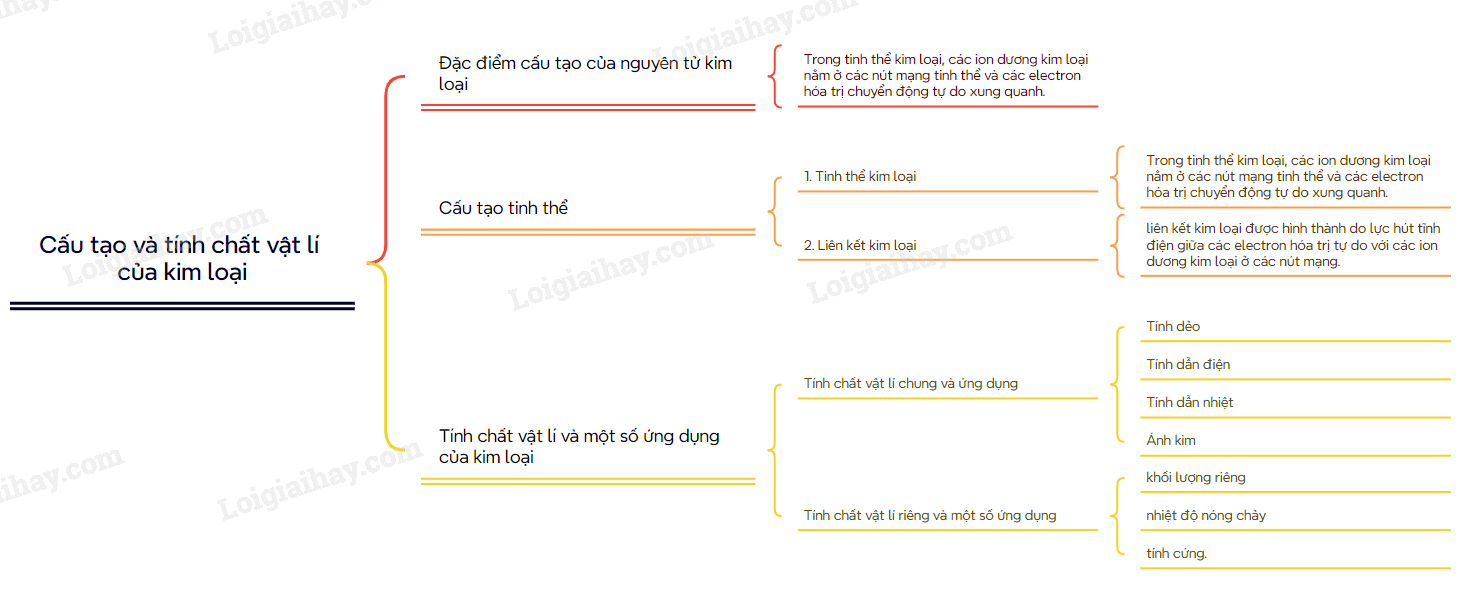
Lý thuyết Cấu tạo và tính chất vật lí của kim loại - Hóa 12 Cánh diềuNguyên tử kim loại có các đặc điểm sau: I. Đặc điểm cấu tạo và liên kết kim loại 1. Đặc điểm cấu tạo Nguyên tử kim loại có các đặc điểm sau: 2. Cấu tạo tinh thể kim loại - Ở điều kiện thường, trừ thủy ngân ở thể lỏng, các kim loại khác đều tồn tại ở thể rắn và có cấu tạo tinh thể. - Trong tinh thể kim loại, do chịu lực hút yếu của hạt nhân nguyên tử nên electron hóa trị dễ tách ra khỏi nguyên tử, tạo thành electron hóa trị tự do và cation kim loại. Vì vậy, tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với electron hóa trị chuyển độ tự do trong tinh thể. 3. Liên kết kim loại Liên kết kim loại là liên kết được hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do trong tinh thể kim loại. II. Tính chất vật lí và một số ứng dụng của kim loại 1. Tính chất vật lí chung và ứng dụng a) Tính dẻo kim loại có tính dẻo nên dễ rèn, dễ dát mỏng và dễ kéo sợi Tính chất này là do các cation kim loại trong tinh thể kim loại có thể trượt lên nhau mà không tách rời nhờ lực hút tĩnh điện giữa chúng với các electron hóa trị tự do. b) Tính dẫn điện Kim loại có tính dẫn điện. Tính dẫn điện tốt nhất là bạc, sau đó đến đồng, vàng, nhôm, sắt,… c) Tính dẫn nhiệt Khi đốt nóng một đầu dây kim loại, các electron hóa trị tự do ở vùng nhiệt độ cao có động năng lớn hơn di chuyển đến vùng có nhiệt độ thấp hơn trong tinh thể kim loại và truyền năng lượng cho các cation kim loại ở đây. d) Ánh kim Các electron hóa trị tự do trong tinh thể kim loại phản xạ hầu hết những tia sáng mà mắt con người nhìn thấy được, do đó kim loại có bề ngoài sáng lấp lánh, còn gọi là ánh kim 2. Tính chất vật lí riêng và một số ứng dụng Kim loại còn có một số tính chất vật lí riêng như khối lượng riêng, nhiệt độ nóng chảy và tính cứng. Kim loại nhẹ nhất là Li, kim loại có khối lượng riêng nặng nhất là Os. Nhiệt độ nóng chảy cao nhất là W, kim loai cứng nhất là Cr. SƠ ĐỒ TƯ DUY
|














Danh sách bình luận