30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 2)Làm bàiCâu hỏi 1 : Dãy chất nào dưới đây chỉ gồm các hợp chất hữu cơ?
Đáp án: A Phương pháp giải: Dựa vào khái niệm hợp chất hữu cơ là hợp chất của cacbon thường có hiđro trừ CO2, muối cacbonat, HCN, muối xianua, muối cacbua kim loại… Lời giải chi tiết: A. Thỏa mãn B. Loại CO2, K2CO3, NaHCO3 là các chất vô cơ. C. Loại NH4HCO3, CCl4 là các chất vô cơ. D. Loại (NH4)2CO3, CO2 là các chất vô cơ. Đáp án A Câu hỏi 2 : Cho các mệnh đề sau: (1) Liên kết hóa học trong hợp chất hữu cơ chủ yếu là liên kết cộng hóa trị. (2) Các hợp chất hữu cơ thường kém bền với nhiệt (3) Các hợp chất hữu cơ thường có nhiệt độ nóng chảy, nhiệt độ sôi cao. (4) Phản ứng hóa học của hợp chất hữu cơ thường xảy ra chậm và theo nhiều hướng khác nhau. Các mệnh đề đúng là
Đáp án: B Phương pháp giải: Dựa vào kiến thức đại cương về hóa hữu cơ trong sgk hóa 11 Lời giải chi tiết: (1), (2), (4) đúng (3) sai vì Các hợp chất hữu cơ thường có nhiệt độ nóng chảy, nhiệt độ sôi thấp Đáp án B Câu hỏi 3 : Chọn định nghĩa đúng: Đồng phân là hiện tượng
Đáp án: B Phương pháp giải: Dựa vào định nghĩa về đồng phân. Lời giải chi tiết: Đồng phân là hiện tượng những chất khác nhau nhưng có cùng công thức phân tử. Lưu ý: D sai vì đồng phân hình học có cùng công thức phân tử và cấu tạo giống nhau, chỉ khác nhau về sự phân bố trong không gian của các nhóm nguyên tử. Đáp án B Câu hỏi 4 : Quá trình nào sau đây thuộc phương pháp kết tinh?
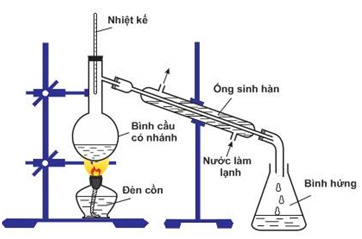
Đáp án: B Phương pháp giải: Lời giải chi tiết: - Ngâm rượu thuốc, giã lá chàm lấy nước để nhuộm vải: phương pháp chiết - Làm đường mía từ nước mía: phương pháp kết tinh - Nấu rượu: phương pháp chưng cất Đáp án B Câu hỏi 5 : Bộ dụng cụ như hình vẽ bên mô tả cho phương pháp tách chất nào :
Đáp án: B Phương pháp giải: Lý thuyết về các phương pháp tách chất hóa học Lời giải chi tiết: Đáp án B Câu hỏi 6 : Tỉ khối hơi của hợp chất hữu cơ A đối với hiđro bằng 23. Vậy khối lượng phân tử chất A là:
Đáp án: A Phương pháp giải: Dựa vào công thức tính tỉ khối để tìm khối lượng phân tử của chất A. Lời giải chi tiết: Tỉ khối hơi của hợp chất hữu cơ A đối với hiđro bằng 23. → dA/H2 = 23 → MA = 23.2 = 46 Đáp án A Câu hỏi 7 : Chất khí nào sau đây không cháy trong oxi?
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Câu hỏi 8 : Cho các chất sau: (1): CH3 – CH2 – OH. (2): CH3 – O – CH3. (3): HO – CH2 – CH3. (4) H – CH2 – CH2 – O – H. Số chất có cùng CTCT là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Câu hỏi 9 : Trong phân tính định tính, để xác định nguyên tử hidro (H) trong phân tử, ta thường:
Đáp án: B Phương pháp giải: Lời giải chi tiết: Khi đôt cháy hợp chất hữu cơ thì sản phẩm chứa H là H2O có thể nhận biết bằng cách cho đi qua CuSO4 khan, nếu có H2O thì sẽ tạo ra CuSO4.5H2O (màu xanh lam) Đáp án B Câu hỏi 10 : Phát biểu nào sau đây không đúng ?
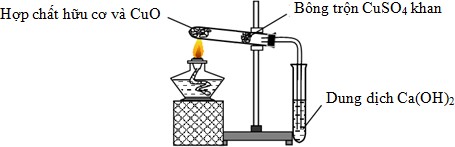
Đáp án: B Phương pháp giải: Lời giải chi tiết: A, C, D đúng B sai vì hợp chất hữu cơ chỉ nhất thiết chứa C, có thể không có H. Đáp án B Câu hỏi 11 : Cho hình vẽ sau:
Phát biểu nào sau đây đúng?
Đáp án: B Phương pháp giải: Lý thuyết về phân tích định tính chất hữu cơ. Lời giải chi tiết: A sai, thí nghiệm này để xác định H và C B đúng, CO2 phản ứng với Ba(OH)2 tương tự như Ca(OH)2 C sai D sai, bông trộn CuSO4 khan có tác dụng phát hiện hơi nước (nếu có hơi nước bông chuyển sang màu xanh) Đáp án B Câu hỏi 12 : Cho các phát biểu sau: 1. Tất cả các hợp chất hữu cơ đều chứa C và H 2. Hợp chất hữu cơ thường dễ cháy, dễ bay hơi 3. Tính chất của hợp chất hữu cơ phụ thuộc vào thành phần phân tử, công thức cấu tạo … của chúng 4. Các chất có thành phần hơn kém nhau một hay nhiều nhóm CH2 được gọi là đồng đẳng của nhau 5. Các chất đồng đẳng có tính chất hóa học tương tự nhau 6. Các chất có cùng phân tử khối là các chất đồng phân Số phát biểu đúng là
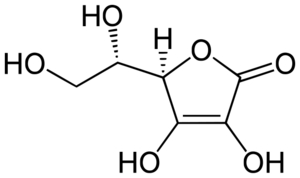
Đáp án: B Phương pháp giải: Lời giải chi tiết: 1. sai vì một số HCHC không chứa H như CCl4 2. đúng 3. đúng 4. sai, các chất có thành phần hơn kém nhau một hay nhiều nhóm CH2 và có tính chất hóa học tương tự nhau được gọi là đồng đẳng của nhau 5. đúng 6. sai vì các chất có cùng công thức phân tử là các chất đồng phân → có 3 phát biểu đúng Đáp án B Câu hỏi 13 : Vitamin C còn gọi là acid ascorbic, tham gia vào nhiều quá trình chuyển hóa trong cơ thể. Nó thúc đẩy sự hình thành collagen, tham gia quá trình chuyển hóa cholesterol, phòng chống ung thư, chống cảm lạnh, bảo vệ da, chống nếp nhăn… Vitamin C có công thức cấu tạo sau:
Công thức phân tử của vitamin C là
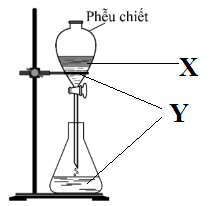
Đáp án: B Phương pháp giải: CTTQ của hợp chất hữu cơ chứa C, H, O là: CnH2n+2-2kOm Từ CTCT đề bài cho ta xác định số C, O và k → n, m, k → CTPT Lời giải chi tiết: CTTQ của hợp chất hữu cơ chứa C, H, O là: CnH2n+2-2kOm Ta đếm được 6C và 6O và xác định được k = 2 π + 1 vòng = 3 → n = 6; m = 6; k = 3 thay vào công thức tổng quát được CTPT của vitamin C là C6H8O6 Đáp án B Câu hỏi 14 : Bộ dụng cụ chiết dùng để tách hai chất lỏng X, Y được mô tả như hình vẽ:
Hai chất X, Y tương ứng là
Đáp án: B Phương pháp giải: Phễu chiết dùng để tách 2 chất lỏng không tan vào nhau. Lời giải chi tiết: Phễu chiết dùng để tách 2 chất lỏng không tan vào nhau => X và Y là 2 chất lỏng không tan (1) Ta thấy X nổi bên trên Y => X phải là chất lỏng nhẹ hơn Y (2) Từ lập luận (1) và (2) => X, Y tương ứng là benzen và nước Đáp án B Câu hỏi 15 : Cho các phát biểu sau: 1) Trong các hợp chất hữu cơ chủ yếu là liên kết cộng hóa trị 2) Hợp chất hữu cơ thường có nhiệt độ sôi, nhiệt độ nóng chảy cao và tan nhiều trong nước 3) Các hợp chất hữu cơ thường kém bền với nhiệt và dễ cháy 4) Phản ứng hóa học của các hợp chất hữu cơ thường xảy ra chậm và theo nhiều hướng khác nhau trong cùng một điều kiện. Các phát biểu đúng là:
Đáp án: D Phương pháp giải: Lời giải chi tiết: 2) Sai: Hợp chất hữu cơ thường có nhiệt độ sôi, nhiệt độ nóng chảy thấp và không tan trong nước Đáp án D Câu hỏi 16 : Đốt cháy hoàn toàn 10ml thể tích hơi 1 HCHC A cần dùng 30ml O2 sản phẩm thu được chỉ gồm CO2 và hơi nước có thể tích bằng nhau và đều bằng thể tích của O2 đã phản ứng. CTPT của A là:
Đáp án: D Phương pháp giải: Lời giải chi tiết: CxHyOz BT “C”: nC = nCO2 = 3 mol => C = 3 BT “H”: nH = 2nH2O = 6 mol => H = 6 BT “O”: nO(A) = 2nCO2 + nH2O – 2nO2 = 2.3 + 3 – 2.3 = 3 => O = 3 => C3H6O3 Đáp án DCâu hỏi 17 : Đốt cháy hoàn toàn 0,9g A chứa C,H, O thu được 0,672 lít CO2( đktc) và 0,54g H2O. Tìm CTPT của A biết tỉ khối hơi của A so với O2 bằng 2,8125.
Đáp án: B Phương pháp giải: Tìm mol C, H, O có trong A Tìm CTĐGN qua công thức : x : y : z = nC : nH : nO Có CTĐGN và phân tử khối => Tìm được CTPT Lời giải chi tiết: Đặt CTPT : CxHyOz n H2O = 0,54 : 18 = 0,03 (mol) n CO2 = 0,672 : 22,4 = 0,03 (mol) n O = (0,9 – 0,03.2 – 0,03.12) : 16 = 0,03 (mol) => x : y : z = 0,03 : 0,06 : 0,03 = 1: 2 : 1 Có: (CH2O) n = 90 => n = 3 => CTPT : C3H6O3 Đáp án: B Câu hỏi 18 : Chất hữu cơ X có CTĐGN là CH2O. Biết trong X có chứa 2 nguyên tử O. Công thức phân tử của A là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án: C CTPT: (CH2O)n vì X chứa 2 nguyên tử O => n = 2 => CTPT C2H4O2 Câu hỏi 19 : Tỉ lệ (tối giản) số nguyên tử C, H, O trong phân tử C2H4O2 lần lượt là:
Đáp án: B Phương pháp giải: Lời giải chi tiết: Tỷ lệ tối giản nC : nH : nO = 2 : 4 : 2 = 1 : 2 : 1 Đáp án B Câu hỏi 20 : Đề nhận biết nguyên tố H trong phân tử hợp chất hữu cơ người ta oxi hóa hoàn toàn X bằng CuO dư rồi dẫn hỗn hợp sản phẩm thu được qua bình chứa
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D Câu hỏi 21 : Metyl salixylat là hợp chất được dùng làm thuốc xoa bóp giảm đau. Oxi hóa hoàn toàn 7,6 gam metyl salixylat rồi dẫn sản phẩm lần lượt qua bình H2SO4 đặc (1) và bình nước vôi trong (2) thấy bình (1) tăng 3,6 gam, bình (2) tăng 17,6 gam. Biết khi hóa hơi 11,4 gam metyl salixylat thì thu được thể tích đúng bằng thể tích của 2,4 gam khí oxi (đo cùng điều kiện). Công thức phân tử của metyl salixylat là (cho NTK: H = 1; C = 12; O = 16)
Đáp án: A Phương pháp giải: - Khối lượng bình 1 tăng chính là khối lượng của nước, suy ra số mol nước và số mol H - Khối lượng bình 2 tăng là khối lượng của CO2, suy ra số mol CO2 và số mol C - Tính tổng khối lượng C và H, so sánh với khối lượng của metyl salixylat, kết luận có O hay không - Gọi công thức phân tử của metyl salixylat là CxHyOz ⟹ Tỉ lệ x : y : z = nC : nH : nO - Suy ra công thức đơn giản nhất - Tính số mol O2. Vì thể tích của metyl salixylat bằng thể tích của oxi nên số mol của chúng bằng nhau → Phân tử khối của metyl salixylat - Kết luận công thức phân tử Lời giải chi tiết: Ta có: mbình 1 tăng = mnước \( \to {m_{{H_2}O}} = 3,6\left( {gam} \right) \to {n_{{H_2}O}} = \frac{{3,6}}{{18}} = 0,2\left( {mol} \right)\) \( \to {n_H} = 2{n_{{H_2}O}} = 2.0,2 = 0,4\left( {mol} \right) \to {m_H} = 1.0,4 = 0,4\left( {gam} \right)\) Ta có: mbình 2 tăng = mCO2 \( \to {m_{C{O_2}}} = 17,6\left( {gam} \right) \to {n_{C{O_2}}} = \frac{{17,6}}{{44}} = 0,4\left( {mol} \right)\) \( \to {n_C} = {n_{C{O_2}}} = 0,4\left( {mol} \right) \to {m_C} = 12.0,4 = 4,8\left( {gam} \right)\) Vì mC + mH = 4,8 + 0,4 = 5,2 < mmetyl salixylat → trong metyl salixylat có O \({m_O} = {m_{metylsalixylat}} - {m_C} - {m_H} = 7,6 - 4,8 - 0,4 = 2,4\left( {gam} \right) \to {n_O} = \frac{{2,4}}{{16}} = 0,15\left( {mol} \right)\) Gọi công thức phân tử của metyl salixylat là CxHyOz \(x:y:z = {n_C}:{n_H}:{n_O} = 0,4:0,4:0,15 = 8:8:3\) Vậy công thức đơn giản nhất của metyl salixylat là C8H8O3. Ta có: \({n_{{O_2}}} = \frac{{2,4}}{{32}} = 0,075\left( {mol} \right)\) Vì thể tích của metyl salixylat bằng thể tích oxi nên \({n_{metylsalixylat}} = {n_{{O_2}}} = 0,075\left( {mol} \right)\) \( \to {M_{metylsal{\rm{ix}}ylat}} = \frac{{11,4}}{{0,075}} = 152 \to (8.12 + 8.1 + 3.16)n = 152 \to n = 1\) Vậy công thức phân tử của metyl salixylat là C8H8O3. Chọn A. Câu hỏi 22 : Mentol là chất tự nhiên có trong tinh dầu bạc hà, tạo cảm giác mát khi bôi lên da hoặc các mô trong khoang miệng. Khi phân tích thành phần metanol cho thấy tỉ lệ về khối lượng của cacbon, oxi và hiđrô lần lượt là 2,1 : 0,28: 0,35. Biết metanol có công thức phân tử trùng với công thức đơn giản nhất. Công thức phân tử của mentol là:
Đáp án: C Phương pháp giải: Đặt công thức phân tử của Mentol có dạng: CxHyOz (đk: x,y, z € N*) Áp dụng công thức: x : y : z = \(\frac{{{m_C}}}{{12}}:\frac{{{m_H}}}{1}:\frac{{{m_O}}}{{16}}\) Sau đó rút gọn tỉ lệ được công thức đơn giản nhất. Vì công thức phân tử trùng với công thức đơn giản nhất nên từ đó tìm được CTPT. Lời giải chi tiết: Đặt công thức phân tử của Mentol có dạng: CxHyOz (đk: x,y, z € N*) Đặt khối lượng của cacbon,oxi, hiđrô lần lượt là 2,1 ; 0,28; 0,35 gam Áp dụng công thức ta có: x : y : z = \(\frac{{{m_C}}}{{12}}:\frac{{{m_H}}}{1}:\frac{{{m_O}}}{{16}}\) \(\begin{array}{l} = \frac{{2,1}}{{12}}:\frac{{0,35}}{1}:\frac{{0,28}}{{16}}\\ = 0,175:0,35:0,0175\\ = \,\,\,\,\,\,10\,\,\,\,:\,\,\,\,20\,\,\,:\,\,1\end{array}\) → Công thức đơn giản nhất: C10H20O Vì công thức phân tử trùng với công thức đơn giản nhất nên CTPT của Mentol là: C10H20O Chọn C. Câu hỏi 23 : Axit Salixylic là hoạt chất có trong các chế phẩm dùng ngoài da để điều trị mụn cóc thông thường ở da và bàn chân, loại bỏ chai sạn và sẹo. Ngoài ra, axit Salixylic là nguyên liệu để điều chế thuốc xoa bóp hay thuốc cảm (aspirin). Khi thực hiện các thí nghiệm phân tích người ta thấy rằng axit này chứa 60,87% C; 4,348% H; còn lại là O về khối lượng. Biết axit Salixylic có công thức phân tử trùng với công thức đơn giản nhất. Công thức phân tử của axit này là
Đáp án: A Phương pháp giải: Trong hợp chất hữu cơ CxHyOz: \(x:y:z = {n_C}:{n_H}:{n_O} = \frac{{{m_C}}}{{12}}:\frac{{{m_H}}}{1}:\frac{{{m_O}}}{{16}} = \frac{{\% {m_C}}}{{12}}:\frac{{\% {m_H}}}{1}:\frac{{\% {m_O}}}{{16}}\) Lời giải chi tiết: Phần trăm khối lượng của O là: 100% - 60,87% - 4,348% = 34,782% Giả sử công thức phân tử của axit Salixylic là CxHyOz Ta có: \(\begin{array}{l}x:y:z = \frac{{\% {m_C}}}{{12}}:\frac{{\% {m_H}}}{1}:\frac{{\% {m_O}}}{{16}}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, = \frac{{60,87\% }}{{12}}:\frac{{4,348\% }}{1}:\frac{{34,782\% }}{{16}}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, = 5,0725:4,348:2,174\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, = 7:6:3\end{array}\) Do công thức phân tử trùng với công thức đơn giản nhất nên công thức phân tử của axit Salixylic là C7H6O3. Chọn A. Câu hỏi 24 : Ma túy đá hay còn gọi là hàng đá, chấm đá là tên gọi chỉ chung cho các loại ma túy tổng hợp, có chứa chất Methamphetamine (Meth). Những người thường xuyên sử dụng ma túy gây ra hậu quả là suy kiệt thể chất, hoang tưởng, thậm chí mất kiểm soát hành vi, chém giết người vô cớ, nặng hơn sẽ mắc tâm thần. Khi oxi hóa hoàn toàn 104,3 gam Meth bằng CuO dư, dẫn sản phẩm cháy lần lượt qua bình 1 đựng H2SO4 đặc, bình 2 đựng Ba(OH)2 dư. Sau khi kết thúc thí nghiệm thấy khối lượng bình 1 tăng 94,5 gam, ở bình 2 tạo thành 1379 gam kết tủa và còn 7,84 lít khí (đktc) thoát ra. Biết Meth có công thức phân tử trùng với công thức đơn giản nhất. Công thức phân tử của Meth là
Đáp án: C Phương pháp giải: Phản ứng oxi hóa hoàn toàn bằng CuO tương đương như việc đốt cháy bằng O2. Khối lượng bình 1 tăng là khối lượng của H2O → \({n_{{H_2}O}}\) Do Ba(OH)2 dư → \({n_{C{O_2}}} = {n_{BaC{O_3}}}\) Khí thoát ra là N2 → \({n_{{N_2}}}\) Bảo toàn C → \({n_C} = {n_{C{O_2}}}\) Bảo toàn H → \({n_H} = 2{n_{{H_2}O}}\) Bảo toàn N → \({n_N} = 2{n_{{N_2}}}\) Ta thấy: \({m_C} + {m_H} + {m_N}\) = mmeth → Meth không chứa O → nC : nH : nN Do CTPT trùng CTĐGN → CTPT Lời giải chi tiết: Phản ứng oxi hóa hoàn toàn bằng CuO tương đương như việc đốt cháy bằng O2. Khối lượng bình 1 tăng là khối lượng của H2O → \({m_{{H_2}O}} = \frac{{94,5}}{{18}} = 5,25(mol)\) Do Ba(OH)2 dư → \({n_{C{O_2}}} = {n_{BaC{O_3}}} = \frac{{1379}}{{197}} = 7(mol)\) Khí thoát ra là N2 → \({n_{{N_2}}} = \frac{{7,84}}{{22,4}} = 0,35(mol)\) Bảo toàn C → \({n_C} = {n_{C{O_2}}} = 7(mol)\) Bảo toàn H → \({n_H} = 2{n_{{H_2}O}} = 2.5,25 = 10,5(mol)\) Bảo toàn N → \({n_N} = 2{n_{{N_2}}} = 2.0,35 = 0,7(mol)\) Ta thấy: \({m_C} + {m_H} + {m_N} = 7.12 + 10,5 + 0,7.14 = 104,3(g)\) = mMeth → Meth không chứa O Ta có: nC : nH : nN = 7 : 10,5 : 0,7 = 10 : 15 : 1 Do CTPT trùng CTĐGN nên CTPT là C10H15N. Chọn C. Câu hỏi 25 : β-Caroten (chất hữu cơ có trong củ cà rốt) có màu da cam. Nhờ tác dụng của enzim trong ruột non, β-caroten chuyển thành vitamin A nên nó còn được gọi là tiền vitamin A. Oxi hoá hoàn toàn 6,7 gam β-caroten rồi dẫn sản phẩm cháy qua bình (1) đựng dung dịch H2SO4 đặc thấy khối lượng bình (1) tăng 6,3 gam. Sau đó, khí thoát ra được dẫn qua qua bình (2) đựng dung dịch Ca(OH)2 thu được 30,0 gam kết tủa và dung dịch X. Thêm dung dịch KOH 1,0 M vào X, thu được kết tủa. Để lượng kết tủa thu được là lớn nhất thì cần tối thiểu 100,0 ml dung dịch KOH. Công thức đơn giản nhất của β-caroten là
Đáp án: B Phương pháp giải: - Dẫn sản phẩm cháy qua bình (1) đựng H2SO4 đặc và bình (2) đựng dung dịch Ca(OH)2: + Axit H2SO4 đặc có tính háo nước nên hấp thụ nước ⟹ Lượng H2O + Khí thoát ra là CO2, cho hấp thụ vào Ca(OH)2: ▪ Tính được số mol CaCO3 và số mol KOH. ▪ Do thêm KOH vào dung dịch X thu được kết tủa ⟹ dung dịch X có chứa Ca(HCO3)2. Theo đề bài, để lượng kết tủa lớn nhất thì cần lượng tối thiểu KOH nên phản ứng là: Ca(HCO3)2 + KOH → CaCO3 ↓ + KHCO3 + H2O Từ PTHH và số mol KOH ⟹ Số mol Ca(HCO3)2 ▪ Bảo toàn nguyên tố C ⟹ \({n_{C{O_2}}} = {n_{CaC{{\rm{O}}_3}}} + 2{n_{Ca{{(HC{O_3})}_2}}}\) - Xét phản ứng cháy của β-caroten: + Bảo toàn nguyên tố C ⟹ \({n_C} = {n_{C{O_2}}}\) + Bảo toàn nguyên tố H ⟹ \({n_H} = 2{n_{{H_2}O}}\) So sánh (mC + mH) và mβ-caroten ⟹ β-caroten không chứa O Lập tỉ lệ số mol nguyên tố C và H ⟹ CTĐGN Lời giải chi tiết: - Dẫn sản phẩm cháy qua bình (1) đựng H2SO4 đặc và bình (2) đựng dung dịch Ca(OH)2: + Axit H2SO4 đặc có tính háo nước nên hấp thụ nước ⟹ \({m_{{H_2}O}} = {m_{binh(1)\tan g}} = 6,3\left( g \right) \to {n_{{H_2}O}} = \frac{{6,3}}{{18}} = 0,35\left( {mol} \right)\) + Khí thoát ra là CO2, cho hấp thụ vào Ca(OH)2: Ta có: \({n_{CaC{{\rm{O}}_3}}} = \frac{{30}}{{100}} = 0,3\left( {mol} \right);{n_{K{\rm{O}}H}} = 0,1.1 = 0,1\left( {mol} \right)\) Do thêm KOH vào dung dịch X thu được kết tủa ⟹ dung dịch X có chứa Ca(HCO3)2 Theo đề bài, để lượng kết tủa lớn nhất thì cần lượng tối thiểu KOH nên phản ứng là: Ca(HCO3)2 + KOH → CaCO3 ↓ + KHCO3 + H2O 0,1 ← 0,1 (mol) Bảo toàn nguyên tố C ⟹ \({n_{C{O_2}}} = {n_{CaC{{\rm{O}}_3}}} + 2{n_{Ca{{(HC{O_3})}_2}}} = 0,3 + 2.0,1 = 0,5\left( {mol} \right)\) - Xét phản ứng cháy của β-caroten: + Bảo toàn nguyên tố C ⟹ \({n_C} = {n_{C{O_2}}} = 0,5\left( {mol} \right)\) + Bảo toàn nguyên tố H ⟹ \({n_H} = 2{n_{{H_2}O}} = 2.0,35 = 0,7\left( {mol} \right)\) Ta thấy: mC + mH = 0,5.12 + 0,7.1 = 6,7 = mβ-caroten ⟹ β-caroten không chứa O ⟹ nC : nH = 0,5 : 0,7 = 5 : 7 Vậy CTĐGN của β-caroten là C5H7. Chọn B. Câu hỏi 26 : Khoảng giữa tháng 12 năm 2019, dịch viêm phổi cấp COVID-19 do chủng virus corona mới đã bùng phát tại thành phố Vũ Hán, thuộc tỉnh Hồ Bắc ở miền trung Trung Quốc. Triệu chứng của bệnh bao gồm sốt, ho, khó thở,… và có thể gây tử vong cho con người. Trong thời gian dịch bệnh diễn biến phức tạp, Bộ Y tế Việt Nam đã đưa ra các khuyến cáo phòng dịch trong đó có việc sử dụng nước rửa tay khô. Thành phần chính của nước rửa tay khô là chất hữu cơ X, chất này ở nồng độ thích hợp có tính sát khuẩn cao. Biết đốt cháy 6,9 gam X cần dùng 10,08 lít khí O2 (đktc) thu được CO2 và H2O. Hấp thụ sản phẩm cháy vào dung dịch Ba(OH)2 dư thấy khối lượng dung dịch giảm 37,8 gam. Công thức cấu tạo thu gọn của X là
Đáp án: A Phương pháp giải: - Tính số mol O2 - Đặt ẩn là số mol của CO2 và H2O + Bảo toàn khối lượng cho phản ứng cháy lập được phương trình (1) + Từ khối lượng dung dịch giảm lập được phương trình (2) Giải hệ thu được số mol CO2, H2O - Tìm CTPT của X: + Dùng bảo toàn nguyên tố C, H tính được số mol C, H trong X + So sánh thấy mC + mH < mX → X có chứa O → nO + Lập tỉ lệ nC : nH : nO ⇒ CTĐGN + Mà trong hợp chất hữu cơ chứa C, H, O ta luôn có: 0 < H ≤ 2C + 2 ⇒ CTPT + Viết các CTCT có thể có. Sau đó dựa vào dữ kiện đề bài cho chọn được CTCT thỏa mãn. Lời giải chi tiết: Ta có: \({n_{{O_2}}} = \frac{{10,08}}{{22,4}} = 0,45\left( {mol} \right)\) Đặt số mol của CO2 và H2O lần lượt là a và b (mol) - Bảo toàn khối lượng cho phản ứng cháy → \({m_{C{O_2}}} + {m_{{H_2}O}} = {m_X} + {m_{{O_2}}}\) ⇔ 44a + 18b = 6,9 + 0,45.32 = 21,3 (1) - Khi hấp thụ sản phẩm cháy vào bình đựng Ba(OH)2 dư có phản ứng: CO2 + Ba(OH)2 → BaCO3 ↓ + H2O Theo PTHH → \({n_{BaC{{\rm{O}}_3}}} = {n_{C{O_2}}} = a\left( {mol} \right)\) Mặt khác, khối lượng dung dịch giảm: mdd giảm = \({m_{BaC{{\rm{O}}_3}}} - ({m_{C{O_2}}} + {m_{{H_2}O}})\) ⇔ 197a - (44a + 18b) = 37,8 ⇔ 153a - 18b = 37,8 (2) Giải hệ (1) (2) ta được a = 0,3 và b = 0,45 Xét phản ứng đốt cháy X: Bảo toàn nguyên tố C → \({n_C} = {n_{C{O_2}}} = 0,3\left( {mol} \right) \to {m_C} = 0,3.12 = 3,6\left( g \right)\) Bảo toàn nguyên tố H → \({n_H} = 2{n_{{H_2}O}} = 0,9\left( {mol} \right) \to {m_H} = 0,9.1 = 0,9\left( g \right)\) Ta thấy mC + mH = 3,6 + 0,9 = 4,5 gam < mX → Trong X có chứa Oxi Ta có: mO = mX - mC - mH = 6,9 - 3,6 - 0,9 = 2,4 gam → nO = 0,15 mol Gọi công thức phân tử của X là CxHyOz Ta có: x : y : z = nC : nH : nO = 0,3 : 0,9 : 0,15 = 2 : 6 : 1 Vậy công thức đơn giản nhất của A là C2H6O Suy ra CTPT của A có dạng (C2H6O)n hay C2nH6nOn. Trong hợp chất hữu cơ chứa C, H, O ta luôn có: H ≤ 2C + 2 ⟹ 6n ≤ 2.2n + 2 ⟹ n ≤ 1 ⟹ n = 1 → CTPT là C2H6O Các CTCT có thể có là CH3CH2OH và CH3OCH3 Do X ở nồng độ thích hợp có tính sát khuẩn cao nên là CH3CH2OH (Etanol). Chọn A. Câu hỏi 27 : Đốt cháy hoàn toàn 6,2 một hợp chất hữu cơ A cần một lượng O2 (đktc) vừa đủ thu được hỗn hợp sản phẩm cháy. Cho sản phẩm cháy hấp thụ hết vào bình đựng dung dịch Ca(OH)2 thấy có 10,0 gam kết tủa xuất hiện và khối lượng dung dịch tăng 4,2 gam. Lọc bỏ kết tủa, đun nóng nước lọc lại thu được 5,0 gam kết tủa nữa (biết H = 1, C = 12, O = 16, Ca = 40). Công thức phân tử của A là
Đáp án: C Phương pháp giải: - Từ số mol kết tủa thu được khi đun nóng nước lọc, tính được số mol Ca(HCO3)2 - Bảo toàn nguyên tố C, tìm được số mol CO2. Từ đó tính được số mol và khối lượng nguyên tố C - Áp dụng công thức khối lượng dung dịch giảm, tính số mol H2O. Từ đó tính số mol và khối lượng nguyên tố H - So sánh tổng khối lượng C và H với khối lượng của A, kết luận trong A có nguyên tố O - Áp dụng bảo toàn khối lượng cho các nguyên tố trong A, tính số mol O - Lập công thức đơn giản nhất và từ đó biện luận tìm được công thức phân tử của A Lời giải chi tiết: \({n_{CaC{{\rm{O}}_3}(lan\,1)}} = \frac{{10}}{{100}} = 0,1\,\,mol\) Vì đun nóng nước lọc lại thu được kết tủa ⟹ trong nước lọc có chứa Ca(HCO3)2 Khi đun nước lọc ta có phản ứng: Theo phương trình, \({n_{Ca{{(HC{O_3})}_2}}} = {n_{CaC{{\rm{O}}_3}(lan\,2)}} = \frac{5}{{100}} = 0,05\,\,mol\) Bảo toàn nguyên tố C cho phản ứng CO2 và Ca(OH)2: \({n_{C{O_2}}} = {n_{CaC{{\rm{O}}_3}}} + 2{n_{Ca{{(HC{O_3})}_2}}} = 0,1 + 2.0,05 = 0,2\,\,mol\) \( \to {n_C} = {n_{C{O_2}}} = 0,2\,\,mol \to {m_C} = 0,2.12 = 2,4\,\,gam\) Lại có mdung dịch tăng = \(({m_{C{O_2}}} + {m_{{H_2}O}}) - {m_{CaC{{\rm{O}}_3}}} \to 4,2 = (0,2.44 + {m_{{H_2}O}}) - 10\) \( \to {m_{{H_2}O}} = 5,4\,\,gam \to {n_{{H_2}O}} = \frac{{5,4}}{{18}} = 0,3\,\,mol\) \( \to {n_H} = 2{n_{{H_2}O}} = 0,6\,\,mol \to {m_H} = 0,6\,\,gam\) Ta thấy mC + mH = 2,4 + 0,6 = 3 gam < mA ⟹ trong A có chứa Oxi Ta có: mO = mA – mC – mH = 6,2 – 2,4 – 0,6 = 3,2 gam ⟹ nO = 0,2 mol Đặt công thức phân tử của A là CxHyOz (đk: x,y, z nguyên dương) Ta có: x : y : z = nC : nH : nO = 0,2 : 0,6 : 0,2 = 1 : 3 : 1 → công thức đơn giản nhất của A là CH3O Suy ra CTPT của A có dạng (CH3O)n hay CnH3nOn. Trong hợp chất hữu cơ chứa C, H, O ta luôn có: H ≤ 2C + 2 ⟹ 3n ≤ 2n + 2 ⟹ n ≤ 2 + Nếu n = 1 ⟹ CTPT là CH3O (loại) + Nếu n = 2 ⟹ CTPT là C2H6O2 (nhận) Chọn C. Câu hỏi 28 : Nicotine là chất hữu cơ có trong thuốc lá, gây nghiện và là mầm mống của bệnh ung thư. Hợp chất này được tạo thành bởi 3 nguyên tố C, H, N. Đốt cháy hết 2,349 gam nicotine thu được N2, 1,827 gam H2O và 3,248 lít CO2 (đktc). Công thức đơn giản của nicotine là?
Đáp án: C Phương pháp giải: Đổi n xenlulozơ trinitrat = 29,7 : 297 = 0,1 (mol) Tính toán theo PT: [C6H7O2(OH)3]n + 3nHNO3 → [C6H7O2(ONO2)3]n + 3nH2O mHNO3 thực tế = mHNO3 lí thuyết :%H (với lượng lí thuyết là lượng tính theo phương trình) Lời giải chi tiết: Gọi công thức của Nicotine là CxHyOz nH2O = 1,827 : 18 = 0,1015 (mol) nCO2(đktc) = 3,248 : 22,4 = 0,145 (mol) BTKL: mN = mnicotine – mC – mH = 2,349 – 0,1015.2 – 0,145.12 = 0,406 (g) => nN = 0,029 (mol) Ta có: x : y : z = nC : nH : nN = 0,145 : 0,203 : 0,029 = 5 : 7 :1 Vậy công thức đơn giản của nicotine là C5H7N Đáp án C Câu hỏi 29 : Paracetamol (X) là thành phần chính của thuốc hạ sốt và giảm đau. Oxi hóa hoàn toàn 5,285 gam X bằng CuO dư, dẫn sản phẩm cháy lần lượt qua bình 1 đựng H2SO4 đặc, bình 2 đựng Ba(OH)2 dư. Sau khi kết thúc thí nghiệm thấy khối lượng bình 1 tăng 2,835 gam, ở bình 2 tạo thành 55,16 gam kết tủa và còn 0,392 lít khí (đktc) thoát ra. CTPT (trùng với công thức đơn giản nhất ) của paracetamol là:
Đáp án: D Phương pháp giải: HCHC + [O] → CO2 + H2O + N2 +) Bình 1 đựng H2SO4 đặc hấp thụ nước +) Bình 2 đựng Ba(OH)2 dư hấp thụ CO2 Lời giải chi tiết: *Bình 1: m bình 1 tăng = mH2O = 2,835 gam => nH2O = 0,1575 mol => nH = 0,315 mol *Bình 2: nBaCO3 = nCO2 = 55,16 : 197 = 0,28 mol => nC = 0,28 mol *Khí thoát ra là N2: nN2 = 0,392 : 22,4 = 0,0175 mol => nN = 0,035 mol mO = mX – mC – mH – mN = 5,285 – 0,28.12 – 0,315.1 – 0,035.14 = 1,12 gam => nO = 0,07 mol Ta có: C : H : O : N = 0,28 : 0,315 : 0,07 : 0,035 = 8 : 9 : 2 : 1 Vậy công thức phân tử (trùng với CTĐGN) là C8H9O2N Đáp án D Câu hỏi 30 : Đốt cháy hoàn toàn một chất hữu cơ X mạch hở, sau phản ứng thu được hỗn hợp Y gồm CO2 và H2O. Mặt khác, hoá hơi hoàn toàn 11,6 gam X thì thu được thể tích đúng bằng thể tích của 5,6 gam N2 (đo ở cùng điều kiện ). Số công thức cấu tạo có thể của X là:
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D
|