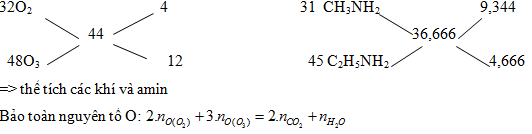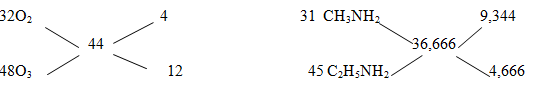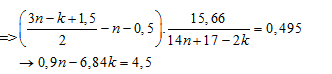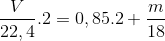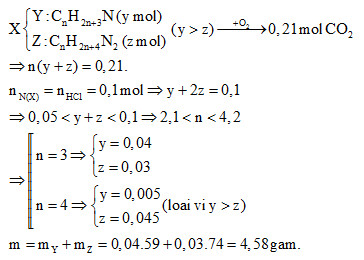30 bài tập về đốt cháy amin mức độ vận dụng có lời giảiLàm bàiCâu hỏi 1 : Đốt cháy hoàn toàn m gam một amin bằng không khí vừa đủ. Trong hỗn hợp sau phản ứng chỉ có 0,4 mol CO2, 0,7 mol H2O và 3,1 mol N2. Giả sử trong không khí chỉ gồm N2 và O2 với tỉ lệ VN2 : VO2 = 4 : 1 thì giá trị của m là
Đáp án: A Phương pháp giải: + Bảo toàn nguyên tố O + Bảo toàn khối lượng: m = mC + mH + mN Lời giải chi tiết: - BTNT "O" => nO2 = (2nCO2 + nH2O)/2= 0,75 mol => nN2 (kk) = 4nO2 = 3 mol => nN2(do amin cháy) = 3,1 - 3 = 0,1 mol - BTNT "N" => mN = 2nN2 = 0,2 mol - BTKL: m = mC + mH + mN = 0,4.12 + 0,7.2 + 0,2.14 = 9 (g) Đáp án A Câu hỏi 2 : Đốt cháy hoàn toàn 0,02 mol amin X bậc 1 với lượng O2 vừa đủ, cho toàn bộ sản phẩm cháy qua bình chứa Ca(OH)2 dư thấy khối lượng bình tăng 3,02 gam và còn lại 0,224 lít (ở đktc) một chất khí không bị hấp thụ. Khi lọc dung dịch thu được 4 gam kết tủa. Công thức cấu tạo của X là.
Đáp án: D Phương pháp giải: + nCO2 = nCaCO3 + mbình tăng = mH2O + mCO2 => nH2O + Khí không bị hấp thụ vào dung dịch Ca(OH)2 là N2 => nN2 Lời giải chi tiết: - Do dẫn CO2 vào dd Ca(OH)2 dư nên: nCO2 = nCaCO3 = 4/100 = 0,04 mol => nC = mCO2 = 0,04 mol (BTNT "C") Số nguyên tử C = nC/nX = 0,04/0,02 = 2 - Khối lượng bình tăng: m bình tăng = mCO2 + mH2O => mH2O = 3,02 - 0,04.44 = 1,26 gam => nH2O = 0,07 mol => nH = 2nH2O = 0,14 mol (BTNT "H") => Số nguyên tử H = nH/nX = 0,14/0,02 = 7 - Khí không bị hấp thụ vào dd Ca(OH)2 là N2: nN2 = 0,01 mol => nN = 2nN2 = 0,02 mol (BTNT "N") Số nguyên tử N = nN/nX = 0,02/0,02 = 1 => CTPT là C2H7N. Mà X là amin bậc 1 => CTCT của X là CH3CH2NH2 Đáp án D Câu hỏi 3 : Đốt cháy hoàn toàn một amin đơn chức X cần vừa đủ 37,8 lít không khí ( trong không khí oxi chiếm 20%, nitơ chiếm 80% về thể tích) thu được CO2, H2O và 30,8 lít khí N2(cho biết các khí đo ở đktc). Công thức cấu tạo của amin X là
Đáp án: C Phương pháp giải: + Viết PT đốt cháy, tính toán theo PT Lời giải chi tiết: nO2 = 0,3375 mol ; nN2(kk) = 1,35 mol nN2 sau pứ = 1,375 mol => nN2 tạo ra = 0,025 mol CxHyN + (x + 0,25y)O2 -> xCO2 + 0,5yH2O + 0,5N2 x + 0,25y 0,5 0,3375 0,025 => 4x + y = 27 => x = 4 ; y = 11 => C4H11N Đáp án C Câu hỏi 4 : Đốt cháy hoàn toàn m gam một amin A bằng lượng không khí vừa đủ thu được 13,2 gam CO2, 8,1 gam H2O và 48,16 lít N2. Giả thiết không khí chỉ gồm nitơ và oxi trong đó nito chiếm 80% theo thể tích, các thể tích khí đo ở đktc. Xác định m
Đáp án: B Phương pháp giải: + Bảo toàn nguyên tố O => nO2 (đốt cháy) = nCO2 + ½ nH2O => nN2 trong không khí => nN2 sinh ra do đốt A + Bảo toàn khối lượng: mA = mC + mH + mN Lời giải chi tiết: Ta có: nCO2 = 0,3 mol; nH2O = 0,45 mol; nN2 = 2,15 mol - BTNT "O" => nO2 = (2nCO2 + nH2O)/2= 0,525 mol => nN2 (kk) = 4nO2 = 2,1 mol => nN2(do amin cháy) = 2,15 - 2,1 = 0,05 mol - BTNT "N" => mN = 2nN2 = 0,1 mol - BTKL: m = mC + mH + mN = 0,3.12 + 0,45.2 + 0,1.14 = 5,9 (g) Đáp án B Câu hỏi 5 : Đốt cháy hoàn toàn V lít hơi một amin X (no, mạch hở, đơn chức, bậc 1) bằng O2 vừa đủ thì thu được 12V hỗn hợp khí và hơi gồm CO2; H2O và N2. Các thể tích khí đều đo ở cùng điều kiện nhiệt độ, áp suất. Số đồng phân cấu tạo thỏa mãn các điều kiện trên của X là
Đáp án: C Phương pháp giải: + Viết PTHH: CnH2n+3N + O2 → nCO2 + (n + 1,5) H2O + 0,5N2 + Biểu diễn thể tích CO2, H2O, N2 theo amin X và theo đầu bài cho => giá trị n Lời giải chi tiết: Amin cần tìm có dạng CnH2n+3N, khi cháy: CnH2n+3N + O2 → nCO2 + (n + 1,5)H2O + 0,5N2 => 12V = (n + n + 1,5 + 0,5)V => n = 5 Amin là C5H13N có 8 đồng phân cấu tạo: CH3-CH2-CH2-CH2-CH2-NH2 CH3-CH2-CH2-CH(NH2)-CH3 CH3-CH2-CH(NH2)-CH2-CH3 (CH3)2CH-CH2-CH2-NH2 (CH3)2CH-CH(NH2)-CH3 (CH3)2C(NH2)-CH2-CH3 CH2(NH2)CH(CH3)-CH2-CH3 (CH3)3C-CH2-NH2 Đáp án C Câu hỏi 6 : Đốt cháy hoàn toàn m gam một amin đơn chức X bằng lượng không khí vừa đủ thu được 1,76 gam CO2; 1,26 gam H2O và V lít N2 (đktc). Giả sử không khí chỉ gồm N2 và O2 trong đó O2 chiếm 20% thể tích. Công thức phân tử của X và giá trị của V lít lần lượt là
Đáp án: C Phương pháp giải: + BTNT "O" => 2nO2 = 2nCO2 + nH2O => nO2 => nN2 (do kk) + BTNT "C": nC = nCO2 BTNT "H": nH = 2nH2O => nC : nH Mà amin là đơn chức => CTPT Lời giải chi tiết: Ta có: nCO2 = 0,04 mol; nH2O = 0,07 mol + BTNT "O" => 2nO2 = 2nCO2 + nH2O => nO2 = 0,075 mol => nN2 (do kk) = 4nO2 = 4.0,075 = 0,3 mol + BTNT "C": nC = nCO2 = 0,04 mol BTNT "H": nH = 2nH2O = 0,14 mol => nC : nH = 0,04 : 0,14 = 2 : 7 Mà amin là đơn chức => CTPT amin là C2H7N + nC2H7N = nCO2/2 = 0,02 mol BTNT "N" => nN2 (do amin) = 0,5.nC2H7N = 0,01 mol => ∑nN2 = 0,3 + 0,01 = 0,31 mol => V = 6,944 lít Đáp án C Câu hỏi 7 : Đốt cháy hoàn toàn 1,18 gam một chất hữu cơ X có chứa C,H,N (chỉ chưa 1 nguyên tử N) bàng 1 lượng không khí vừa đủ (chứa 20% O2, 80%N2). dẫn toàn bộ sản phẩm qua bình đựng nước vôi trong dư thu được 6 gam kết tủa và có 9,632 lít khí duy nhất thoát ra. CTPT của X là
Đáp án: C Phương pháp giải: Phương pháp:Phương trình đốt cháy \({C_x}{H_y}N + (x + {y \over 4}){O_2} \to xC{O_2} + {y \over 2}{H_2}O + {1 \over 2}{N_2}\) Khi đốt cháy 1 amin ngoài không khí thì: nN2 sau phản ứng = nN2 sinh ra từ phản ứng đốt cháy amin + nN2 có sẵn trong không khí
Lời giải chi tiết:
Hướng dẫn giải: \({C_x}{H_y}N + (x + {y \over 4}){O_2} \to xC{O_2} + {y \over 2}{H_2}O + {1 \over 2}{N_2}\) 0,06 \({{0,03} \over x}\) Theo PT:\({n_{{O_2}}} = {{0,06} \over x}\left( {x + {y \over 4}} \right) \to {n_{{N_2}}} = {{4.0,06} \over x}\left( {x + {y \over 4}} \right)\) =>\(\sum {{n_{{N_2}}} = {{0,03} \over x} + } {{4.0,06} \over x}\left( {x + {y \over 4}} \right) = {{9,632} \over {22,4}} = 0,43\) => 0,19x - 0,06y =0,03 (1) namin =\({{0,06} \over x} \Leftrightarrow {{1,18} \over {12{\rm{x}} + y + 14}} = {{0,06} \over x} \to 0,46{\rm{x}} - 0,06y = 0,84\) (2) Từ (1) và (2) => x=3, y=9 => C3H9N Chọn C Câu hỏi 8 : Cho hỗn hợp X có thể tích V1 gồm O2 và O3 có tỉ khối so với H2 bằng 22. Cho hỗn hợp Y có thể tích V1 gồm metylamin và etylamin có tỉ khối so với H2 bằng 17,8333. Đốt cháy hoàn toàn V2 lít hỗn hợp Y cần V1 lít hỗn hợp X. Tỉ lệ V1/V2 là
Đáp án: B Phương pháp giải: Phương pháp: Phương pháp đường chéo
Lời giải chi tiết:
\(\left\{ \matrix{ {O_2}\,\,{{{V_1}} \over 4} \hfill \cr {O_3}{{3{V_1}} \over 4} \hfill \cr} \right.\,\,\,\,\,\,\,\,\,\& \,\,\,\left\{ \matrix{ C{H_3}N{H_2}\,\,{{2{V_2}} \over 3} \hfill \cr {C_2}{H_5}N{H_2}{{{V_2}} \over 3} \hfill \cr} \right.\,\,\, \Leftrightarrow \left\{ \matrix{ C{O_2}\,\,{{4{V_2}} \over 3} \hfill \cr {H_2}O{{17{V_2}} \over 6} \hfill \cr} \right.\) Bảo toàn nguyên tố O
\(\eqalign{ & 2.{n_{O({O_2})}} + 3.{n_{O({O_3})}} = 2.{n_{C{O_2}}} + {n_{{H_2}O}} \cr & {{2.{V_1}} \over 4} + {{3.3{V_1}} \over 4} = {{2.4{V_2}} \over 3} + {{17{V_2}} \over 6} \to {{{V_1}} \over {{V_2}}} = 2 \cr} \) Chọn B Câu hỏi 9 : Đốt cháy hoàn toàn 0,1 mol amin đơn chức X bằng không khí, sau phản ứng cho hỗn hợp qua dung dịch NaOH dư đun nóng thấy khối lượng dung dịch tăng 21,3 gam và thấy thoát ra 48,16 lít khí N2 (khí duy nhất thoát ra ở đktc). CTPT của amin là
Đáp án: C Phương pháp giải: Bảo toàn nguyên tố O , tính theo phương trình, tăng giảm khối lượng \({n_{{N_2}(sau\,p/u)}} = {n_{{N_2}(kk)}} + {n_{{N_2}(sp)}}\) Lời giải chi tiết: Đăt a,b lần lượt là số mol của CO2 và H2O \({C_x}{H_y}N + (x + {y \over 2}){O_2} \to xC{O_2} + y{H_2}O + 0,5{N_2}\) 0,1 a b 0,05 Vì đốt cháy trong không khí nên
\(\eqalign{ & {n_{{N_2}(sau\,p/u)}} = {n_{{N_2}(kk)}} + {n_{{N_2}(sp)}} \to {{48,16} \over {22,4}} = {n_{{N_2}(kk)}} + 0,05 \cr & \to {n_{{N_2}(kk)}} = 2,1\,\,mol \to {n_{{O_2}(kk)}} = {1 \over 4}.{n_{{N_2}(kk)}} = 0,525\,\,mol \cr} \) Do chỉ thu được duy nhất khí N2 => O2 (kk) phản ứng hết mtăng= \({m_{C{O_2}}} + {m_{{H_2}O}} = 44{\rm{a}} + 18b = 21,3\,\,\,\,\,\,\,(1)\) Bảo toàn nguyên tố O => 2a+b=0,525.2=1,05 (2) Từ (1) và (2) => a=0,3 => x=\({{0,3} \over {0,1}} = 3\); b=0,45 =>y= \({{0,45.2} \over {0,1}} = 9\) => X:C3H9N Chọn C Câu hỏi 10 : Đốt cháy hoàn toàn 7,6 gam hỗn hợp X gồm 2 amin no, đơn chức , mạch hở bằng không khí, sau đó cho hỗn hợp qua NaOH dư thấy khối lượng dung dịch tăng 24 gam và thấy thoát ra V lít khí hỗn hợp Y(đktc) gồm 2 khí có tỉ lệ mol là 1:9. Giá trị của V là
Đáp án: B Phương pháp giải: Phương pháp: Đặt số mol của amin : x, trong không khí : O2 a mol, N2 4a mol BTKL : ${m_X} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}} + {m_{{N_2}}} \to {n_{{O_2}(p/u)}}$ Hỗn hợp Y gồm: ${n_{{O_2}}} = {\rm{a}} - {n_{{O_2}(p/u)}}\,\,\,\,{n_{{N_2}}} = 4{\rm{a}} - {n_{{N_2}(\sinh \,ra)}}\,$ ${n_{{O_2}}}:{n_{{N_2}}} = 1:9 \to a \to {n_Y} \to V$ Lời giải chi tiết: Hướng dẫn giải CnH2n+3N nCO2 + (n+1,5)H2O + 0,5 N2 x nx (n+1,5)x 0,5x Vì N2là khí trơ nên dung dịch NaOH chỉ hấp thụ CO2 và H2O => mdd tăng = ${m_{C{O_2}}} + {m_{{H_2}O}} = 44n{\rm{x}} + 18x(n + 1,5) = \,\,(62n + 27)x = 24\,\,\,\,(1)$ mX=(14n+17)x =7,6 (2) Từ (1) và (2) => $\left\{ \matrix{ n{\rm{x}} = 0,3 \hfill \cr x = 0,2 \hfill \cr} \right. \to \left\{ \matrix{ n = 1,5 \hfill \cr x = 0,2 \hfill \cr} \right.$ Theo định luật BTKL $\eqalign{ & {m_X} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}} + {m_{{N_2}}} \to 7,6 + 32.{n_{{O_2}}} = 24 + 2,8 \cr & \to {n_{{O_2}}} = 0,6\,\,mol \cr} $ Trong không khí : O2 a mol, N2 4a mol Hỗn hợp Y gồm: ${n_{{O_2}}} = a - 0,6\,\,\,mol\,\,\,\,{n_{{N_2}}} = 4a + 0,1\,\,\,mol$
$\eqalign{ & {n_{{O_2}}}:{n_{{N_2}}} = 1:9 \to 0,9(a - 0,6) = 4{\rm{a}} + 0,1 \to a = 1,1\,mol \cr & {n_Y} = 1,1 - 0,6 + 4.1,1 + 0,1 = 5mol \to V = 22,4.5 = 112\,\,lit \cr} $ Chọn B Câu hỏi 11 : Hỗn hợp A gồm 1 amin đơn chức, 1 anken, 1ankan. Đốt cháy hoàn toàn 12,95 gam A cần V lít khí O2 thu được 19,04 lít khí CO2, 0,56 lít khí N2 và m gam H2O. Giá trị của m là
Đáp án: C Phương pháp giải: Phương pháp: Bảo toàn nguyên tố Lời giải chi tiết: Hướng dẫn giải
\(\eqalign{ & {n_{C{O_2}}} = {{19,04} \over {22,4}} = 0,85mol \cr & {n_{{N_2}}} = {{0,56} \over {22,4}} = 0,025\,\,\,mol \cr} \) mA=mC+mH+mN => 12,95=0,85.12+ 0,025.28+ mH => mH= 2,05 gam=> nH=2,05 mol => \({m_{{H_2}O}} = 18.{{2,05} \over 2} = 18,45g\) Chọn C Câu hỏi 12 : Đốt cháy 0,02 mol một amin bậc nhất với lượng oxi vừa đủ. Cho toàn bộ sản phẩm cháy qua bình chứa Ca(OH)2 dư thấy khối lượng bình tăng 3,2 gam và 0,448 lít khí (đktc) không bị hấp thụ. Khi lọc thu được 4 gam kết tủa. CTPT của amin
Đáp án: B Phương pháp giải: Phương pháp: bảo toàn nguyên tố: nC(X)= nCO2 , nH(X) = 2\({n_{{H_2}O}}\) , nN(X)= 2\({n_{{N_2}}}\) Lời giải chi tiết: Hướng dẫn giải \({n_{{N_2}}} = 0,02\,\,\,mol\) \({n_{C{O_2}}} = 0,04\,mol\) mbình tăng=\({m_{C{O_2}}} + {m_{{H_2}O}} = 0,04.44 + {m_{{H_2}O}} = 3,2g\) =>\({m_{{H_2}O}} = 1,44 = > {n_{{H_2}O}} = 0,08\,\,mol\)
\(\Leftrightarrow \left\{ \matrix{ {n_C} = 0,04mol \hfill \cr {n_H} = 0,16\,\,\,mol \hfill \cr {n_N} = 0,04\,mol \hfill \cr} \right.\) Công thức CxHyNz => x=0,04:0,02 =2 . tương tự y=8, z=2 Amin có CTPT C2H8N2 Chọn B Câu hỏi 13 : Lấy 15,66 gam amin đơn chức, mạch hở,X (có không quá 4 liên kết )trộn với 168 lít không khí (đktc). Bật tia lửa điện để đốt cháy hoàn toàn X. Hỗn hợp sau phản ứng được đưa về 0oC, 1atm, để ngưng tụ hết hơi nước thì có thể tích là 156,912 lít. Xác định số đồng phân amin bậc 3 của X là
Đáp án: A Phương pháp giải: Phương pháp: nkhí giảm= \({{{V_t} - {V_s}} \over {22,4}}$=\({n_{{O_2}(p/u)}} - {n_{C{O_2}}} - {n_{{N_2}}}\) Đặt công thức X là CnH2n+3-2kN (k 4). Từ phương trình tính số mol khí giảm. Biện luận n và k
Lời giải chi tiết: Hướng dẫn giải: nkhí giảm=\({{168 - 156,912} \over {22,4}} = 0,495\,\,mol\)=\({n_{{O_2}(p/u)}} - {n_{C{O_2}}} - {n_{{N_2}}}\) Đặt công thức X là CnH2n+3-2kN (k 4) \({C_n}{H_{2n + 3 - 2k}}N + ({{3n - k + 1,5} \over 2}){O_2} \to nC{O_2} + (n - k + 1,5){H_2}O + 0,5{N_2}\)
=> X: C5H13N Amin bậc 3 + (CH3)2NC3H7 có 2 đồng phân + (C2H5)2NCH3 CÓ 1 đồng phân Vậy có 3 đồng phân amin bâc 3 Chọn A Câu hỏi 14 : Đốt cháy hoàn toàn V lít hơi một amin X bằng một lượng oxi vừa đủ tạo ra 8V lít hỗn hợp gồm khí cacbonic, khí nitơ và hơi nước (các thể tích khí và hơi đều đo ở cùng điều kiện). Amin X có cùng bậc với ancol metylic. Chất X là
Đáp án: C Phương pháp giải: Phương pháp giải : amin X bậc 1 có dạng CTHH là CxHyNH2 Lập tỉ lệ giữa thể tích sản phẩm với thể tích X để tìm liên hệ giữa x và y Lời giải chi tiết:
Lời giải : Amin X bậc 1 nên X là CxHyNH2 Khi X tác dụng với O2 thì tạo ra CO2, N2 và H2O có thể tích là 8V = x.V + V:2 + (y+2).V : 2 nên 13 = 2x + y Chọn x = 3 và y=7 Đáp án C Câu hỏi 15 : Hỗn hợp A gồm 1 amin đơn chức, 1 anken và 1 ankan. Đốt cháy hoàn toàn 12,95 g hỗn hợp cần V lít O2 thu được 19,04 lít CO2 ; 0,56 lít N2 và m gam nướC. Biết các thể tích khí đo ở đktc. Tính V
Đáp án: B Phương pháp giải: Bảo toàn khối lượng Bảo toàn nguyên tố Lời giải chi tiết:
Hướng dẫn giải : nCO2 = 0,85 mol và nN2 = 0,025 mol Bảo toàn khối lượng có Bảo toàn nguyên tố O có Giải được V=30,52 lít Đáp án B Câu hỏi 16 : Cho 13,35 gam hỗn hợp X gồm 2 amin no đơn chức mạch hở đồng đẳng kế tiếp tác dụng với dung dịch HCl vừa đủ thu được dung dịch chứa 22,475 gam muối. Nếu đốt cháy hoàn toàn 13,35 gam hỗn hợp X thì trong sản phẩm cháy có VCO2 ÷ VH2O bằng
Đáp án: D Phương pháp giải: RNH2 + HCl → RNH3Cl C\(\overline x \)H2\(\overline x \)+3N + O2→\(\overline x \) CO2 + ( \(\overline x \) + 1,5 ) H2O Bảo toàn khối lượng : m amin + m HCl = m muối Tính toán theo giá trị trung bình : với \(\overline x \) là giá trị trung bình của 2 amin Lời giải chi tiết: m amin + m HCl = m muối => m HCl = 22,475 – 13,35 = 9,125 => n HCl = n amin = 0,25 mol => \(\overline M \)Amin = 13,35 : 0,25 = 53,4 g => \(\overline x \)= ( 53,4 – 17 ) : 14 = 2,6 => n CO2 : n H2O = VCO2 : VH2O = 2,6 : ( 2,6 + 1,5 ) = 26 : 41 Đáp án D Câu hỏi 17 : Đốt cháy hoàn toàn một amin X, bằng lượng không khí vừa đủ thu được 17,6 gam CO2, 12,6 gam H2O và 69,44 lít khí N2( đktc). Giả thiết không khí chỉ gồm N2 và O2, trong đó oxi chiếm 20% thể tích không khí. Số đồng phân cấu tạo của X là
Đáp án: D Phương pháp giải: + BTNT O: 2nO2=2nCO2+nH2O=>nO2 pư=> nN2(kk)=4nO2pư => nN2(amin cháy) =>nN(amin) + Lập tỉ lệ C:H:O => CTĐGN + Dựa vào điều kiện H≤2C+2+N => CTPT Lời giải chi tiết: nCO2=0,4 mol; nH2O=0,7 mol; nN2=3,1 mol + BTNT O: 2nO2=2nCO2+nH2O=>nO2 pư=(2.0,4+0,7)/2=0,75 mol=> nN2(kk)=4nO2pư=3 mol => nN2(amin cháy)=0,1 mol =>nN(amin)=0,2 mol C:H:N=0,4:1,4:0,2=2:7:1 CTPT: (C2H7N)n Mà H≤2C+2+N =>7n≤2.2n+2+n => n≤1 Vậy n=1, amin là C2H7N Các CTCT có thể có: CH3CH2NH2 và CH3-NH-CH3 Đáp án D Câu hỏi 18 : Đốt cháy hoàn toàn 9 gam hỗn hợp X gồm C2H5NH2 và (CH3)2NH bằng lượng vừa đủ khí O2. Cho toàn bộ sản phẩm cháy vào bình đựng dung dịch Ba(OH)2, sau khi các phản ứng xảy ra hoàn toàn thu được 59,1 gam kết tủa và một dung dịch có khối lượng giảm m gam so với khối lượng dung dịch Ba(OH)2 ban đầu. Giá trị của m là
Đáp án: B Phương pháp giải: 2 chất trong X đều có CTPT là C2H7N => nX Viết PTHH của phản ứng đốt cháy, đặt mol vào tính được số mol của CO2 và H2O => m dung dịch giảm = m↓ - mCO2 – mH2O Lời giải chi tiết: 2 chất trong X đều có CTPT là C2H7N. nX = 9/45 = 0,2 mol C2H7N + 3,75O2 → 2CO2 + 3,5 H2O + 0,5N2 0,2 0,4 0,7 Khi dẫn sản phẩm vào dung dịch Ba(OH)2 thì CO2 và H2O bị hấp thụ. Khi đó m dung dịch giảm = m↓ - mCO2 – mH2O = 59,1 – 0,4.44 – 0,7.18 = 28,9 gam Đáp án B Câu hỏi 19 : Đốt cháy hoàn toàn một amin mạch hở X bằng một lượng không khí (chứa 20% thể tích O2, còn lại là N2) vừa đủ, thu được 0,08 mol CO2; 0,2 mol H2O và 0,54 mol N2. Khẳng định nào sau đây là đúng?
Đáp án: B Phương pháp giải: Bảo toàn nguyên tố O => nO2 = nCO2 + 1/2nH2O = ?(mol) => nN2 ( trong kk) = 4nO2 = ? (mol) => nN2 (sinh ra do đốt amin) = 0,54 – nN2 ( trong kk) = ? (mol) Gọi CTPT của amin là CxHyOz x: y : z = nC : nH : nN => CT ĐGN là ? Biện luận để tìm được CTPT của amin và xét xem đáp án nào đúng Lời giải chi tiết: Bảo toàn nguyên tố O => nO2 = nCO2 + 1/2nH2O = 0,08 + 0,1/2 = 0,13 (mol) Vì O2 chiếm 20% thể tích không khí => N2 chiếm 80% thể tích không khí => nN2 ( trong kk) = 4nO2 = 4.0,13 = 0,52 (mol) => nN2 (sinh ra do đốt amin) = 0,54 – 0,52 = 0,02 (mol) Gọi CTPT của amin là CxHyOz x: y : z = nC : nH : nN = 0,08 : 0,2 : 0,04 = 2 : 5 : 1 => CT ĐGN là C2H5N Ta thấy (nH2O – nCO2) = 2nN2 => amin này là đơn chức, mạch hở, có 1 liên kết pi trong phân tử => CTCT của amin là CH2=CH-NH2 A. Sai, số nguyên tử cacbon của X bằng 2 B. đúng C. sai, phân tử X có 1 liên kết đôi D. Sai, số nguyên tử H là 5 Đáp án B Câu hỏi 20 : Đốt cháy hoàn toàn 0,15 mol một amin no, mạch hở X bằng oxi vừa đủ, thu được 0,75 mol hỗn hợp Y gồm khí và hơi. Cho 6,21 gam X tác dụng với lượng dư dung dịch HCl. Số mol HCl phản ứng là
Đáp án: A Phương pháp giải: + Đốt cháy X: X là amin no, mạch hở → X: CnH2n+2+aNa CnH2n+2+aNa + O2 → nCO2 + (n+1+0,5a)H2O + 0,5aN2 0,15 mol nY = 0,15.(n + n + 1 + 0,5a + 0,5a) = 0,15.(2n + 1+ a) = 0,75 → 2n + a = 4 → n = 1 và a = 2 → X: H2NCH2NH2. + Cho X tác dụng với HCl dư: X là amin hai chức, do đó X phản ứng với HCl theo tỉ lệ mol tương ứng là 1: 2. Lời giải chi tiết: + Đốt cháy X: X là amin no, mạch hở → X: CnH2n+2+aNa CnH2n+2+aNa + O2 → nCO2 + (n+1+0,5a)H2O + 0,5aN2 0,15 mol nY = 0,15.(n + n + 1 + 0,5a + 0,5a) = 0,15.(2n + 1+ a) = 0,75 → 2n + a = 4 → n = 1 và a = 2 → X: H2NCH2NH2. + Cho X tác dụng với HCl dư: nHCl (pư) = 2nX = 2.6,21/46 = 0,27 mol. Đáp án A Câu hỏi 21 : Cho hỗn hợp X gồm 2 amin no, đơn chức, mạch hở là đồng đẳng kế tiếp nhau tác dụng vừa đủ với dung dịch HCl thu được 34 gam hỗn hợp muối. Cho hỗn hợp muối đó vào dung dịch AgNO3 dư thu được 57,4 gam kết tủa. Phần trăm khối lượng của amin có phân tử khối nhỏ hơn trong hỗn hợp X là
Đáp án: A Phương pháp giải: CnH2n+1NH2 (X) → CnH2n+1NH3Cl (Y) → AgCl nX = nY = nAgCl = 0,4 mol → MY = 34/0,4 = 85 → n = 2,25 → X gồm C2H7N (x mol) và C3H9N (y mol) Ta có: x + y = 0,4 (1) và 2x + 3y = 2,25.0,4 = nC (X) (2). Từ (1) và (2): x = 0,3 và y = 0,1 → % C2H7N. Lời giải chi tiết: \(\begin{array}{l} Đáp án A Câu hỏi 22 : Hỗn hợp E chứa C2H4, C3H6 và một amin no, đơn chức, mạch hở X. Đốt cháy hoàn toàn 140 ml hỗn hợp E cần dùng 630 ml O2 thu được hỗn hợp F gồm CO2, H2O và N2. Ngưng tụ toàn bộ F thấy thể tích giảm 500 ml. Các khí đều đo ở cùng điều kiện. Nếu cho một lượng X tác dụng vừa đủ với 100 ml dung dịch HCl 0,8M thì thu được m gam muối. Giá trị của m là
Đáp án: C Phương pháp giải: Lời giải chi tiết: Khi ngưng tụ F, H2O bị ngưng tụ → Thể tích giảm = 500 ml = thể tích nước. Trong cùng điều kiện (nhiệt độ, áp suất), tỉ lệ về thể tích = tỉ lệ về số mol. Coi các thê tích = số mol. \(\begin{array}{l} Đáp án C Câu hỏi 23 : Đốt cháy hoàn toàn m gam hỗn hợp X gồm 2 amin no, đơn chức, mạch hở trong oxi dư thu được 1,792 lít khí CO2 (đktc) và 2,25 gam H2O. Cho m gam hỗn hợp X tác dụng vừa đủ với dung dịch HClloãng thu được a gam muối. Giá trị của a gần nhất với giá trị nào sau đây?
Đáp án: C Phương pháp giải: nCO2 = 0,08 mol; nH2O = 0,125 mol → nC (X) = 0,08 mol; nH (X) = 0,25 mol. X gồm 2 amin no, đơn chức, mạch hở → gọi CTTQ của X: CnH2n+3N (x mol). Ta thấy: nH2O – nCO2 = 1,5x → x = 0,03 mol → nN (X) = 0,03 mol → nHCl = nN (X) = 0,03 mol. Tính m: m = mC (X) + mH (X) + mN (X) Tính a: dùng BTKL Lời giải chi tiết: + Đốt cháy X: nCO2 = 0,08 mol; nH2O = 0,125 mol → nC (X) = 0,08 mol; nH (X) = 0,25 mol. X gồm 2 amin no, đơn chức, mạch hở → gọi CTTQ của X: CnH2n+3N (x mol). Ta thấy: nH2O – nCO2 = 1,5x → x = 0,03 mol → nN (X) = 0,03 mol Ta có: m = mC (X) + mH (X) + mN (X) = 0,08.12 + 0,25.1 + 0,03. 14 = 1,63 gam. + Cho X tác dụng với dung dịch HCl: nHCl (phản ứng) = nN (X) = 0,03 mol → mHCl (pư) = 1,095 gam. Áp dụng ĐLBTKL: mX + mHCl (pư) = mmuối → a = mmuối = 1,63 + 1,095 = 2,725 gam. Đáp án C Câu hỏi 24 : Hỗn hợp E chứa 3 amin no, đơn chức, mạch hở. Đốt cháy hoàn toàn m gam E cần 0,255 mol O2. Sản phẩm cháy thu được có chứa 0,03 mol N2. Nếu cho lượng E trên tác dụng hết với HNO3 dư thì khối lượng muối thu được là
Đáp án: B Phương pháp giải: E có công thức tổng quát là CnH2n+3N. nE = 2nN2 = 0,06 mol. Kết hợp với số mol O2 → tìm được n → tính được m. nHNO3 (phản ứng) = nE → mHNO3 (phản ứng). Bảo toàn khối lượng để tìm khối lượng muối. Lời giải chi tiết: E có công thức tổng quát là CnH2n+3N. \(\begin{array}{l}{C_n}{H_{2n + 3}}N + (1,5n + 0,75){O_2} \to nC{O_2} + (n + 1,5){H_2}O + 0,5{N_2}\\\,\,\,\,\,\,0,06\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,255\,\,\,\,\,\,\, \leftarrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,03\,(mol)\\ \Rightarrow 0,06.(1,5n + 0,75) = 0,255 \Rightarrow n = \frac{7}{3}\\m = (14.\frac{7}{3} + 3 + 14).0,06 = 2,98\,gam.\\{n_{HN{O_3}(pu)}} = {n_E} = 0,06\,mol \Rightarrow {m_{HN{O_3}(pu)}} = 3,78\,gam\\BTKL:{m_{muoi}} = m + {m_{HN{O_3}(pu)}} = 6,76\,gam\end{array}\) Đáp án B Câu hỏi 25 : Đốt cháy hoàn toàn V lít X gồm metan, metylamin và trimetylamin bằng oxi vừa đủ được V1 lít hỗn hợp Y gồm khí và hơi. Dẫn toàn bộ Y qua bình đựng H2SO4 đặc, dư thấy thoát ra V2 lít hỗn hợp khí Z (các thể tích khí đo ở đktc). Mối quan hệ giữa V, V1 và V2 là
Đáp án: C Phương pháp giải: Y gồm CO2, H2O và N2. Khi qua bình đựng H2SO4 đặc, H2O bị giữ lại. Z gồm CO2 và N2. \(\begin{array}{l}V\,lit\,X\left\{ \begin{array}{l}{C_n}{H_{2n + 2}}\\{C_n}{H_{2n + 3}}N\end{array} \right. + {O_2} \to ({V_1} - {V_2})\,lit\,{H_2}O + {V_2}\,lit\left\{ \begin{array}{l}C{O_2}\\{N_2}\end{array} \right.\\NX:\,\,{n_{{H_2}O}} - ({n_{C{O_2}}} + {n_{{N_2}}}) = {n_X}\end{array}\) Lời giải chi tiết: Y gồm CO2, H2O và N2. Khi qua bình đựng H2SO4 đặc, H2O bị giữ lại. Z gồm CO2 và N2. \(\begin{array}{l}V\,lit\,X\left\{ \begin{array}{l}C{H_4}\\{C_n}{H_{2n + 3}}N\end{array} \right. + {O_2} \to ({V_1} - {V_2})\,lit\,{H_2}O + {V_2}\,lit\left\{ \begin{array}{l}C{O_2}\\{N_2}\end{array} \right.\\NX:\,\,{n_{{H_2}O}} - ({n_{C{O_2}}} + {n_{{N_2}}}) = {n_X} \Rightarrow V = ({V_1} - {V_2}) - {V_2}\\ \Rightarrow V = {V_1} - 2{V_2}\end{array}\) Đáp án C Câu hỏi 26 : Hỗn hợp X gồm một amin no, đơn chức, mạch hở Y và một amin no, hai chức, mạch hở Z (Y và Z có cùng số nguyên tử cacbon; số mol của Y nhiều hơn số mol của Z). Đốt cháy hoàn toàn m gam X sinh ra 9,24 gam CO2. Trung hòa m gam X cần vừa đủ 500 ml dung dịch HCl 0,2M. Giá trị m là
Đáp án: C Phương pháp giải: Lời giải chi tiết:
Đáp án C Câu hỏi 27 : Hỗn hợp M gồm một anken và 2 amin no, đơn chức, mạch hở X và Y là đồng đẳng kế tiếp (MX <MY). Đốt cháy hoàn toàn một lượng M cần dùng 18,144 lít O2 (đktc) thu được H2O, N2 và 8,960 lít CO2 (đktc). Chất Y là
Đáp án: C Phương pháp giải: \(M\left\{ \begin{array}{l}{C_n}{H_{2n}}(n \ge 2):a\,mol\\{C_m}{H_{2m + 3}}N:b\,mol\end{array} \right. + {O_2}:0,81\,mol \to C{O_2}:0,4\,mol\) Với các dữ kiện đã có, ta có thể nghĩ đến: + Có số mol O2 và CO2 → dùng BTNT oxi ta có thể tìm được nH2O. + Khi có số mol H2O, ta thấy: nH2O – nCO2 = 1,5b → tìm được b. Lời giải chi tiết: \(\begin{array}{l}M\left\{ \begin{array}{l}{C_n}{H_{2n}}(n \ge 2):a\,mol\\{C_m}{H_{2m + 3}}N:b\,mol\end{array} \right. + {O_2}:0,81\,mol \to C{O_2}:0,4\,mol\\BTNT\,O:2{n_{{O_2}}} = 2{n_{C{O_2}}} + {n_{{H_2}O}} \Rightarrow {n_{{H_2}O}} = 2{n_{{O_2}}} - 2{n_{C{O_2}}} = 0,82\,mol\\{n_{{H_2}O}} - {n_{C{O_2}}} = 1,5b \Rightarrow b = \frac{{0,82 - 0,4}}{{1,5}}=0,28\,mol\\\overline C = \frac{{0,4}}{{a + b}} < \frac{{0,4}}{b} = 1,43\end{array}\) Vì anken có số nguyên tử C>1 mà số nguyên tử C trung bình bằng 1,43; X và Y là đồng đẳng kế tiếp → X: CH5N (CH3NH2) và Y là CH3CH2NH2 (etylamin). Đáp án C Câu hỏi 28 : Hỗn hợp khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hỗn hợp X bằng một lượng oxi vừa đủ, thu được 550 ml hỗn hợp Y gồm khí và hơi nước. Nếu cho Y đi qua dd axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). CTPT của hai hiđrocacbon là
Đáp án: A Phương pháp giải: Lời giải chi tiết: Trong cùng điều kiện (nhiệt độ, áp suất), tỉ lệ về thể tích = tỉ lệ về số mol. Để đơn giản, ta lấy số mol = thể tích. \(\begin{array}{l}100\,molX\left\{ \begin{array}{l}{C_2}{H_7}N:a\\{C_m}{H_{2m + 2 - 2k}}:b\end{array} \right. + {O_2} \to 300\,mol\,{H_2}O + 250\,mol\left\{ \begin{array}{l}C{O_2}\\{N_2}\end{array} \right.\\ \Rightarrow \left\{ \begin{array}{l}a + b = 100\\2a + 0,5a + mb = 250\\3,5a + (m + 1 - k)b = 300\end{array} \right. \Rightarrow \left\{ \begin{array}{l}a + b = 100\,\,\,\,\,\,\,\,\,\,\,\,\,(1)\\2,5a + bm = 250\,(2)\\a + b(1 - k) = 50\,(3)\end{array} \right. \Rightarrow \left\{ \begin{array}{l}a + b = 100\\m = 2,5\\bk = 50\end{array} \right.\end{array}\) Từ (1) và (2) ta thấy m = 2,5. b.k = 50 nên k phải khác 0. Ngoài ra, trong các đáp án đã cho, 2 hiđrocacbon hoặc là anken (k=1) hoặc là ankan (k=0) → 2 hiđrocacbon cần tìm là C2H4 và C3H6. Đáp án A Câu hỏi 29 : Hỗn hợp E chứa axetilen, propin và một amin no, đơn chức, mạch hở. Đốt cháy hoàn toàn 5,46 gam hỗn hợp E cần dùng 11,088 lít O2 (đktc) thu được hỗn hợp F gồm CO2, H2O và khí N2, trong đó tỉ lệ mol CO2: H2O là 1:1. Phân tử khối của amin là
Đáp án: A Phương pháp giải: \(5,46g\,E\left\{ \begin{array}{l}{C_n}{H_{2n - 2}}:x\\{C_m}{H_{2m + 3}}N:y\end{array} \right. + {O_2}:0,495\,mol \to \left\{ \begin{array}{l}C{O_2}:a\\{H_2}O:a\\{N_2}\end{array} \right.\) Từ dữ kiện đề bài: + Biết số mol O2 và tỉ lệ mol CO2 : H2O → dùng BTNT oxi ta có thể tìm được số mol nước và CO2. + Dùng bảo toàn khối lượng để tìm số mol của N2 → số mol của amin (y mol) + Khi có số mol H2O và CO2, ta thấy: nH2O – nCO2 = 1,5y – x → tìm được x. + Xử lí tiếp bài toán theo các hướng như: tìm số nguyên tử C trung bình hoặc dựa vào số mol CO2 để tìm số nguyên tử C của từng chất, …. Lời giải chi tiết: \(\begin{array}{l}5,46g\,E\left\{ \begin{array}{l}{C_n}{H_{2n - 2}}:x\\{C_m}{H_{2m + 3}}N:y\end{array} \right. + {O_2}:0,495\,mol \to \left\{ \begin{array}{l}C{O_2}:a\\{H_2}O:a\\{N_2}\end{array} \right.\\BTNT\,oxi:2{n_{{O_2}}} = 2{n_{C{O_2}}} + {n_{{H_2}O}} \Rightarrow 0,495.2 = 2a + a \Rightarrow a = 0,33\,mol\\5,46 = {m_E} = {m_C} + {m_H} + {m_N} = 0,33.12 + 0,33.2 + {m_N}\\ \Rightarrow {m_N} = 0,84 \Rightarrow y = 0,06\,mol\\{n_{{H_2}O}} - {n_{C{O_2}}} = 0 \Rightarrow x = 1,5y = 0,09\,mol\\\left\{ \begin{array}{l}nx + my = {n_{C{O_2}}} = 0,33\\2 < n < 3\end{array} \right. \Rightarrow \left\{ \begin{array}{l}0,09n + 0,06m = 0,33\\2 < n < 3\end{array} \right.\\ \Rightarrow 1 < m < 2,5 \Rightarrow n = 2 \Rightarrow A\min :\,{C_2}{H_7}N\end{array}\) Đáp án A Câu hỏi 30 : Hỗn hợp khí E gồm một amin bậc III no, đơn chức, mạch hở và hai ankin X, Y (MX< MY). Đốt cháy hoàn toàn 0,15 mol hỗn hợp E cần dùng 11,2 lít O2 (đktc), thu được hỗn hợp F gồm CO2, H2O và N2. Dẫn toàn bộ F qua bình đựng dung dịch KOH đặc, dư đến phản ứng hoàn toàn thấy khối lượng bình bazơ nặng thêm 20,8 gam. Số cặp công thức cấu tạo ankin X, Y thỏa mãn là
Đáp án: C Phương pháp giải: Đặt a, b là số mol CO2, H2O mBình nặng = mCO2 + mH2O => 44a + 18b = 20,8 (1) BTNT O: 2nO2 = 2nCO2 + nH2O => 2a+ b = 2.0,5 (2) Từ (1) và (2) => a = ? và b = ?(mol) Hỗn hợp E gồm: \(\left\{ \begin{array}{l}{C_m}{H_{2m + 3}}N:v\,mol\\{C_{\overline n }}{H_{2\overline n - 2}}:\,u\,mol\end{array} \right.\) Ta có: \(\left\{ \begin{array}{l}{n_E} = v + u = 0,15\\{n_{C{O_2}}} = mv + \overline n u = 0,35\\{n_{{H_2}O}} = v(m + 1,5) + u(\overline n - 1) = 0,3\end{array} \right. \Rightarrow \left\{ \begin{array}{l}v = ?\\u = ?\end{array} \right.\) => mối quan hệ m, \(\overline n \) => chọn giá trị và viết các CTCT thỏa mãn Lời giải chi tiết: Đặt a, b là số mol CO2, H2O mBình nặng = mCO2 + mH2O => 44a + 18b = 20,8 (1) BTNT O: 2nO2 = 2nCO2 + nH2O => 2a+ b = 2.0,5 (2) Từ (1) và (2) => a = 0,35 và b = 0,3 (mol) Hỗn hợp E gồm: \(\left\{ \begin{array}{l}{C_m}{H_{2m + 3}}N:v\,mol\\{C_{\overline n }}{H_{2\overline n - 2}}:\,u\,mol\end{array} \right.\) Ta có: \(\begin{array}{l}\left\{ \begin{array}{l}{n_E} = v + u = 0,15\\{n_{C{O_2}}} = mv + \overline n u = 0,35\\{n_{{H_2}O}} = v(m + 1,5) + u(\overline n - 1) = 0,3\end{array} \right. \Rightarrow \left\{ \begin{array}{l}v = 0,04\\u = 0,11\end{array} \right.\\ \Rightarrow {n_{C{O_2}}} = 0,04m + 0,11\overline n = 0,35\end{array}\) Vì m ≥ 3 và \(\overline n \ge 2\) \( \Rightarrow \left\{ \begin{array}{l}m = 3\\\overline n = \frac{{23}}{{11}}\end{array} \right.\)là nghiệm duy nhất thỏa mãn Vậy 2 cặp ankin thỏa mãn là: \(\left\{ \begin{array}{l}{C_2}{H_2}\\{C_3}{H_4}\end{array} \right.\,va\left\{ \begin{array}{l}{C_2}{H_2}\\{C_4}{H_6}\end{array} \right.\) (Vì MX < MY và các chất ở thể khí) => Các cặp CTCT thỏa mãn là: Cặp 1: CH≡ CH và CH≡C-CH3 Cặp 2: CH≡ CH và CH≡ C-CH2-CH3 Cặp 3: CH≡ CH và CH3- C≡C -CH3 Đáp án C
|