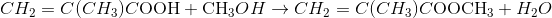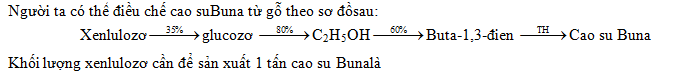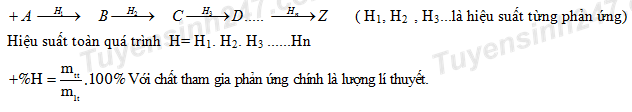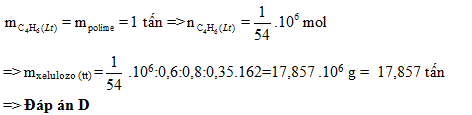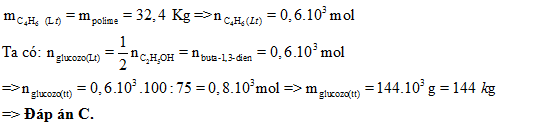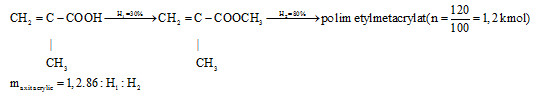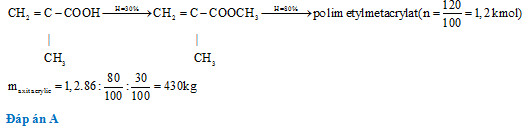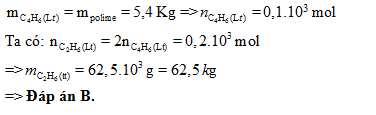30 bài tập về điều chế polime có lời giảiLàm bàiCâu hỏi 1 : Poli (vinyl clorua) (PVC) được điều chế từ khí thiên nhiên (chứa 95% thể tích khí metan) theo sơ đồ chuyển hóa và hiệu suất mỗi giai đoạn như sau: $Metan\xrightarrow{{hs15\% }}Axetilen\xrightarrow{{hs95\% }}Vinylclorua\xrightarrow{{hs90\% }}PVC$ Muốn tổng hợp 3,125 tấn PVC thì cần bao nhiêu m3 khí thiên nhiên (đo ở đktc)?
Đáp án: B Phương pháp giải: + %H= (npư/ nban đầu ).100% Lời giải chi tiết: Ta có thể tóm tắt toàn bộ quá trình phản ứng như sau \(2nC{H_4}\xrightarrow{{15\% }}n{C_2}{H_2}\xrightarrow{{95\% }}nC{H_2}CHCl\xrightarrow{{90\% }}{(C{H_2} - CHCl)_n}\) \({n_{PVC}} = \frac{{3,{{125.10}^6}}}{{62,5}} = {5.10^4}mol\) => nCH4 phản ứng = 2 nPVC = 105 mol => nCH4 ban đầu = (nCH4 phản ứng).100% : %H với (% H = H1. H2. H3 ) = 105: 0,15: 0,95: 0,9 = 779727,0955 mol Vì khí thiên nhiên chứa 95% metan => Vkhí thiên nhiên = Vmetan : 0,95 = 779727,0955 . 22,4 : 0,95 = 18385144 lít = 18385 m3 Đáp án B
Câu hỏi 2 : Để điều chế 60kg poli(metyl metacrylat) cần tối thiểu m1 kg ancol và m2 kg axit tương ứng. Biết hiệu suất của cả quá trình là 75%. Giá trị của m1, m2 lần lượt là
Đáp án: D Phương pháp giải: Phương pháp giải Tính khối lượng của từng chất theo lý thuyết rồi chia hiệu suất để tìm lượng thực tế với mtt = mlt :75.100 Lời giải chi tiết:
Lời giải chi tiết : Theo lý thuyết 51,6 kg ← 60:100.32=19,2 kg ← 60kg Thực tế 68,8 kg 25,6 kg Đáp án D Câu hỏi 3 : Cho sơ đồ chuyển hóa: CH4 → C2H2 → C2H3Cl → PVC. Muốn tổng hợp 250 kg PVC theo sơ đồ trên thì cần V m3 khí thiên nhiên (ở đktc). Giá trị của V là (biết CH4 chiếm 80% thể tích khí thiên nhiên và hiệu suất cả quá trình là 50%).
Đáp án: A Phương pháp giải: Viết sơ đồ phản ứng và tính toán theo sơ đồ phản ứng Lời giải chi tiết: nPVC = 250 : 62,5 = 4 mol 2CH4 → C2H2 → C2H3Cl → PVC 8 mol ← 4 mol => V khí thiên nhiên = 8.22,4.(100/80).(100/50) = 448 (lít) Đáp án A Câu hỏi 4 : Điều chế cao su buna từ xenlulozo theo sơ đồ sau: Xenlulozo \(\xrightarrow{{35\% }}\) Glucozo \(\xrightarrow{{80\% }}\) Etanol \(\xrightarrow{{60\% }}\) Buta-1,3-đien \(\xrightarrow{{100\% }}\) Cao su buna Khối lượng xenlulozơ cần để sản xuất 1 tấn cao su buna là
Đáp án: C Phương pháp giải: Công thức tính khối lượng chất tham gia phản ứng khi có hiệu suất \({m_{thuc\,te}} = {{m{\,_l}_{i\,thuyet}} \over {\% H}}.100\% \) Lời giải chi tiết: (C6H10O5)n \(\buildrel {35\% } \over\longrightarrow \)C6H12O6 \(\buildrel {80\% } \over\longrightarrow \) 2C2H5OH \(\buildrel {60\% } \over\longrightarrow \) CH2=CH-CH=CH2 \(\buildrel {TH 100\% } \over\longrightarrow \) Cao su buna Nhìn hệ số sơ đồ đầu cuối => nC6H10O5 = ncao su bu na = 1/ 54 (tấn mol) => mC6H10O5 lí thuyết = 1/54. 162 = 3 (tấn) Vì có hiệu suất phản ứng nên khối lượng tinh bột cần lấy thực tế là: \({m_{{C_6}{H_{10}}{O_{5\,}}tt}} = 3.{{100\% } \over {100\% }}.{{100\% } \over {60\% }}.{{100\% } \over {80\% }}.{{100\% } \over {35\% }} = 17,857\,(\tan )\) Đáp án C Câu hỏi 5 : Trùng hợp 65,0 g stiren bằng cách đun nóng chất này với một lượng nhỏ chất xúc tác benzoyl peoxit. Cho toàn bộ hỗn hợp sau phản ứng (đã loại hết benzoyl peoxit) vào 1,0 lít dung dịch brom 0,15M ; sau đó cho thêm KI (dư) thấy sinh ra 6,35 g iot. Hiệu suất của phản ứng trùng hợp stiren là
Đáp án: B Phương pháp giải: Lời giải chi tiết: Các phương trình hoá học: \(nC_6H_5CH=CH_2 \xrightarrow {{t^0},xt,p}\)\((-CH(C_6H_5)-CH_2-)_n\) \(C_6H_5-CH=CH_2 + Br_2 \to\)\( C_6H_5-CHBr-CH_2Br(1)\) \(2KI+Br_2 \to I_2+2KBr(2)\) Số mol Br2 tham gia 2 phản ứng là 0,15 mol. \(n_{Br_2 (2)} = n_{I_2} \)=\(\dfrac{{6,35}}{{254}}=0,025(mol)\) Số mol Br2 tác dụng với stiren \(= 0,15 - 0,025 = 0,125 (mol)\) Khối lượng sitren không trùng hợp \(= 0,125\times104 = 13 (g)\) Khối lượng stiren đã trùng hợp \(= 65 -13 = 52 (g)\) Hiêu suất trùng hợp \(H_{pư}=\dfrac{{m_{LT}}}{{m_{TT}}}\times 100%\) \(=\dfrac{{52}}{{65}}\times100\% = 80\% \) Đáp án B Câu hỏi 6 : Sau khi trùng hợp 1 mol etilen thì thu được sản phẩm có phản ứng vừa đủ với 16 gam brom. Hiệu suất phản ứng và khối lượng polime thu được là
Đáp án: B Phương pháp giải: + nBr2 = netilen dư \(\% H = \frac{{{m_{tt}}}}{{{m_{lt}}}}.100\% \,\,\,hay\,\,\,\% H = \frac{{{m_{pu}}}}{{{m_{bd}}}}.100\% \) Lời giải chi tiết: nBr2 = 0,1 mol = nC2H4 dư => nC2H4 pư = nC2H4 bđ - nC2H4 dư = 1 - 0,1 = 0,9 mol H% = \(\frac{{{n_{{C_2}{H_4}_{\,pu}}}}}{{{n_{{C_2}{H_4}_{\,bd}}}}}.100\% \) = \(\frac{{0,9}}{1}.100\% \) = 90% Đáp án B Câu hỏi 7 : Người ta sản xuất cao su Buna từ gỗ theo sơ đồ sau: \(Go{\text{ }}\xrightarrow{{{H_1} = 35\% }}{\text{Glucozo}}\xrightarrow{{{H_2} = 80\% }}Ancol{\text{ }}etylic\xrightarrow{{{H_3} = 60\% }}Butadien - 1,3\xrightarrow{{{H_4} = 100\% }}Cao{\text{ }}su{\text{ }}Buna.\) Tính lượng gỗ cần thiết để sản xuất được 1 tấn cao su, giả sử trong gỗ chứa 50% xenlulozơ?
Đáp án: A Phương pháp giải:
Lời giải chi tiết: Để dễ tính toán ta coi như tất cả các mắt xích là n = 1 Sơ đồ phản ứng của bài toán như sau: C6H10O5 -> C6H12O6 -> 2C2H5OH -> C4H6 -> Caosu buna Hiệu suất toàn bộ quá trình là: H = H1.H2.H3.H4 = 35%.80%.60%.100% = 16,8% m Xenlulozo = (1:54).(100/16,8).162 = 17,857 tấn Vì trong gỗ chứa 50% xenlulozo nên khối lượng gỗ cần dùng là: 17,857.(100/50) = 35,714 tấn Đáp án A Câu hỏi 8 : Từ 15kg metyl metacrylat có thể điều chế được bao nhiêu gam thuỷ tinh hữu cơ có hiệu suất 90%?
Đáp án: B Phương pháp giải: \(\% H = \frac{{{m_{tt}}}}{{{m_{lt}}}}.100\% \,hay\,\,\% H = \frac{{{m_{pu}}}}{{{m_{bd}}}}.100\% \) Lời giải chi tiết: 15 . 90% = 13,5 kg = 13 500 g Đáp án B Câu hỏi 9 : Poli(vinyl clorua) (PVC) được điều chế từ khí thiên nhiên (metan chiếm 95% khí thiên nhiên) theo sơ đồ chuyển hóa và hiệu suất mỗi giai đoạn như sau: Metan \(\xrightarrow{{H = 15\% }}\) Axetilen \(\xrightarrow{{H = 95\% }}\) Vinyl clorua \(\xrightarrow{{H = 90\% }}\) PVC Muốn tổng hợp 1 tấn PVC thì cần bao nhiêu m3 khí thiên nhiên (đo ở đktc)?
Đáp án: B Phương pháp giải:
Lời giải chi tiết: Sơ đồ: 2CH4 → C2H2 → C2H3Cl → PVC Hiệu suất cả quá trình: H = H1.H2.H3 = 0,15.0,95.0,9 = 0,12825 = 12,825% Thể tích CH4 cần là: VCH4 = (1000/62,5) . 2 . 22,4 . (100/12,825) = 5589 m3 Thể tích khí thiên nhiên (chứa 95% CH4) cần dùng: V khí = 5589 . (100/95) = 5883 m3 Đáp án B Câu hỏi 10 : Tiến hành phản ứng trùng hợp 5,2 gam stiren, sau phản ứng ta thêm 400 ml dung dịch nước brom 0,125M, khuấy đều cho phản ứng hoàn toàn thấy dư 0,04 mol Br2. Khối lượng polime sinh ra là
Đáp án: A Phương pháp giải: + nBr2 = n liên kết II bị phá vỡ = n stiren dư + Bảo toàn khối lượng mpolime = mstiren phản ứng Lời giải chi tiết: Số mol Br2 phản ứng cũng chính là số mol stiren dư là 0,01 mol BTKL: mpolime = mstiren ban đầu - mstiren dư = 5,2 - 0,01.104 = 4,16 gam Đáp án A Câu hỏi 11 :
Đáp án: D Phương pháp giải:
Lời giải chi tiết:
Câu hỏi 12 : Muốn tổng hợp 120 kg poli(metylmetacrylat) thì khối lượng của axit và ancol tương ứng cần dùng là bao nhiêu ?Biết hiệu suất quá trình este hoá và trùng hợp lần lượt là 60% và 80%.
Đáp án: A Phương pháp giải: \( + \% H = {{{m_{tt}}} \over {{m_{lt}}}}.100\% \) Với sản phẩm thu được chính là lượng thực tế. Lời giải chi tiết: \({m_{metylmetacrylat}} = {{{m_{PMM}}.100} \over {{H_{trung\,hop}}}} = {{120.100} \over {80}} = 150\,Kg = > \,\,{n_{metylmetacrylat}} = 1,5.1{0^3}\,mol\) Ta có: \(\eqalign{& {n_{C{H_2} = C\left( {C{H_3}} \right) - COOH}} = {n_{C{H_3}OH}} = {{{n_{metylmetacrylat}}.100} \over H} = 2,5.1{0^3}\,mol & \cr & = > \,\,{n_{C{H_2} = C\left( {C{H_3}} \right) - COOH}} = 215.1{0^3}\,g = 215\,Kg,\,\,\,{n_{C{H_3}OH}} = 80.1{0^3}\,g = 80\,kg \cr} \) Đáp án A Câu hỏi 13 : Thủy phân hoàn toàn 24,6 g một tetrapeptit X trong môi trường axit thì thu được 30g một aminoaxit Y. Y là:
Đáp án: A Phương pháp giải: Bảo toàn khối lượng. Lời giải chi tiết: X + 3H2O \(\buildrel {{H^ + }} \over\longrightarrow \) 4Y Áp dụng ĐLBTKL: mH2O = mY –mX = 30-24,6 = 5,4 g => nH2O = 0,3 mol Ta có: nY = (4nH2O/3) = 0,4 mol => MY = 75 g/mol => glyxin Đáp án A Câu hỏi 14 : Từ glucozơ điều chế cao su buna theo sơ đồ sau đây: Glucozơ → rượuetylic→buta-1,3-đien→ caosubuna. Hiệu suất của quá trình điều chế là 75%,muốn thu được 32,4 kg cao su thì khối lượng glucozơ cần dùng là
Đáp án: C Phương pháp giải: \( + \% H = {{{m_{tt}}} \over {{m_{lt}}}}.100\% \) Với chất tham gia phản ứng chính là lượng lí thuyết. + C6H12O6 → 2C2H5OH → CH2=CH-CH=CH2 → polime => nglocozo = npolime Lời giải chi tiết:
Câu hỏi 15 : Poli( vinyl clorua) (PVC) được điều chế từ khí thiên nhiên ( chứa 95% thể tích khí metan) theo sơ đồ chuyển hóa và hiệu suất mỗi giai đoạn như sau: Metan (15%) -> Axetilen (95%) -> Vinyl clorua (90%) -> PVC Muốn tổng hợp 3,125 tấn PVC thì cần bao nhiêu m3 khí thiên nhiên ( đo ở đktc) ?
Đáp án: B Phương pháp giải: Phương pháp : Tính lượng chất dựa vào hiệu suất phản ứng. Sơ đồ : 2nCH4 → nC2H2→ nCH2=CHCl → (-CH2-CHCl-)n (PVC) Lời giải chi tiết: Hướng dẫn giải: Đáp án B Có : nPVC = 0,05/n (tấn mol) = 50 000/n (mol) => nCH4(Cần dùng) = 2n.nPVC : (15%.95%.90%) = 779 727 mol => VCH4 = 17 465 887 lit = 17 466 m3 => Vkhí = 18 385 m3 Câu hỏi 16 : Poli( vinyl clorua) được điều chế từ khí thiên nhiên ( chứa 95% metan theo thể tích) theo sơ đồ chuyển hóa và hiệu suất ( H) như sau: \(Me\tan \xrightarrow{{H = 15\% }}\,Axetilen\xrightarrow{{H = 95\% }}Vinyl\,clorua\xrightarrow{{H = 90\% }}Poli(vinyl\,clorua).\) Thể tích khí thiên nhiên (đktc) cần để điều chế được 1 tấn PVC là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Ta có: \(\sum {H = \frac{{{H_1}.{H_2}.{H_3}}}{{100}} = 0,12825 \Rightarrow {n_{C{H_4}}} = \frac{{2{n_{{C_2}{H_3}Cl}}}}{{\sum H }} = 0,{{25.10}^3}mol} \,\,\,\) VCH4(trong tự nhiên)= $\frac{{{n_{C{H_4}}}}}{{0,95}}.22,4 = 5883,25({m^3})$ Đáp án C Câu hỏi 17 : Tổng hợp 120 kg polimetylmetacrylat từ axit và ancol thích hợp, hiệu suất của phản ứng este hóa là 30% và phản ứng trùng hợp là 80%. Khối lượng của axit cần dùng là
Đáp án: A Phương pháp giải:
Lời giải chi tiết:
Câu hỏi 18 : Poli(vinylclorua) được điều chế từ khí axetilen theo sơ đồ sau: C2H2 \(\xrightarrow{{H = 80\% }}\) CH2=CHCl \(\xrightarrow{{H = 90\% }}\) PVC Thể tích khí axetilen (đktc) cần dùng để điều chế được 450 gam PVC là:
Đáp án: D Phương pháp giải: Bài toán hiệu suất: A → B → C (H1, H2 là hiệu suất phản ứng A → B và B → C) => nC = nB.H2% = nA.H1%.H2% Lời giải chi tiết: C2H2 \(\xrightarrow{{H = 80\% }}\) CH2=CHCl \(\xrightarrow{{H = 90\% }}\) PVC 26n (g) 62,5n (g) 187,2 (g) ← 450 (g) => nC2H2 (LT) = 187,2 : 26 = 7,2 mol => V C2H2 (LT) = 161,28 lít Do hiệu suất 2 quá trình là H = 80% và H = 90% nên lượng C2H2 cần dùng thực tế là: VC2H2 cần dùng = 161,28.(100/80).(100/90) = 224 lít Đáp án D Câu hỏi 19 : Người ta tổng hợp poli(metyl metacrylat) từ axit và ancol tương ứng qua hai giai đoạn là este hoá (hiệu suất 60%) và trùng hợp (hiệu suất 80%). Khối lượng axit và ancol cần dùng để thu được 1,2 tấn polime là
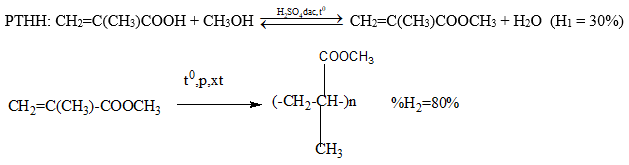
Đáp án: A Phương pháp giải: - Viết phương trình hóa học xảy ra - Áp dụng công thức tính hiệu suất \(H_{pư}= \dfrac{{m_{LT}}}{{m_{TT}}}\) Lời giải chi tiết: CH2=C(CH3)-COOH + CH3OH \(\xrightarrow{{t^0},H^+}\) CH2=C(CH3)-COOCH3 +H2O nCH2=C(CH3)COOCH3 \(\xrightarrow{{{t^0},p,xt}}\) (-CH2-C(CH3)(COOCH3)-)n Nếu hiệu suất của các giai đoạn đều là 100% thì: Để tạo ra 100 tấn polime cần 86 tấn axit và 32 tấn ancol. Thực tế, các hiệu suất là 60% và 80% nên để tạo ra 1,2 tấn polime, khối lượng axit cần dùng là: \(\dfrac{{86\times1,2}}{{100}}\times\dfrac{{100}}{{60}}\times\dfrac{{100}}{{80}}=2,15 tấn\) Khối lượng ancol cần dùng là: \(\dfrac{{32\times1,2}}{{100}}\times\dfrac{{100}}{{60}}\times\dfrac{{100}}{{80}}=0,8 tấn\) Đáp án A Câu hỏi 20 : Tổng hợp 120kg poli(metyl metacrylat) từ axit và ancol thích hợp, hiệu suất của phản ứng este hóa là 30% và phản ứng trùng hợp là 80%. Khối lượng của axit tương ứng cần dùng là
Đáp án: B Phương pháp giải: - Tính số mol polime và suy ra số mol axit - Tính khối lượng axit. Lời giải chi tiết: \({n_{{C_3}{H_5}COOH}} = {n_{{C_5}{H_8}{O_2}}} = 1,2(kmol)\) \( \to {m_{{C_3}{H_5}COOH}} = \frac{{1,2.86}}{{30\% .80\% }} = 430(kg)\) Đáp án B Câu hỏi 21 : Tiến hành trùng hợp 5,2 gam stiren. Hỗn hợp sau phản ứng cho tác dụng 100 ml dung dịch brom 0,15M. Sau đó cho tiếp dung dịch KI dư vào thì thu được 0,635 gam iot. Hiệu suất trùng hợp stiren là
Đáp án: B Phương pháp giải: - Tính số mol brom ban đầu - Từ số mol iot, suy ra số mol brom dư - Suy ra số mol brom phản ứng - Tính số mol stiren dư từ số mol brom phản ứng - Tính hiệu suất phản ứng trùng hợp. Lời giải chi tiết: Số mol brom ban đầu: \({n_{B{{\rm{r}}_2}(b{\rm{d}})}} = 0,015\,\,mol\) Số mol brom dư: \({n_{B{{\rm{r}}_2}\,\,du}} = {n_{{I_2}}} = 0,0025\,\,mol\) \( \to {n_{B{{\rm{r}}_2}(pu)}} = 0,0125\,\,mol\) \( \to {n_{{C_6}{H_5}CH = C{H_2}(du)}} = 0,0125\,\,mol\) Hiệu suất phản ứng: \(H = \frac{{5,2 - 0,0125.104}}{{5,2}}.100\% = 75\% \) Đáp án B Câu hỏi 22 : Từ xenlulozơ người ta điều chế cao su buna theo sơ đồ: xenlulozơ → C6H12O6 → C2H5OH → C4H6 → cao su buna. Với hiệu suất của mỗi phản ứng đạt 80%, để điều chế được 1 tấn cao su thì khối lượng nguyên liệu ban đầu (có 19% tạp chất) cần là
Đáp án: D Phương pháp giải: - Tính số mol cao su - Tính số mol xenlulozơ - Tính khối lượng xenlulozơ Lời giải chi tiết: Ta có: ncao su \( = \frac{{1000}}{{54}}(kmol)\) \( \to {n_{xenlulozo}} = \frac{{1000}}{{54}}.{(\frac{{100}}{{80}})^4} = 45,211(kmol)\) \( \to {m_{xenlulozo}} = \frac{{45,211.162.100\% }}{{81\% }} = 9042kg = \)9,042 tấn. Đáp án D Câu hỏi 23 : Tổng hợp 120 kg polimetylmetacrylat từ axit và ancol thích hợp, hiệu suất của phản ứng este hóa là 30% và phản ứng trùng hợp là 80%. Khối lượng của axit cần dùng là
Đáp án: B Phương pháp giải: nCH2=C(CH3)COOH lí thuyết = npolimetaacylat = 1,2 (mol) => nCH2=C(CH3)COOH thực tế = nCH2=C(CH3)COOH lí thuyết :%H2 : %H1 = ?(mol) => mCH2=C(CH3)COOH thực tế = ? Lời giải chi tiết:
npolimetaacylat = 12:100 = 1,2 (mol) => nCH2=C(CH3)COOH lí thuyết = npolimetaacylat = 1,2 (mol) => nCH2=C(CH3)COOH thực tế = nCH2=C(CH3)COOH lí thuyết :%H2 : %H1 = 1,2 : 0,8 : 0,3 = 5 (mol) => mCH2=C(CH3)COOH thực tế = 5. 86 = 430 (kg) Đáp án B Câu hỏi 24 : Người ta điều chế cao su Buna từ gỗ theo sơ đồ sau: Xenlulozơ → Glucozơ → Etanol → Buta -1,3 - đien → cao su Buna Biết hiệu suất 3 phản ứng đầu lần lượt là 35%, 80%, 60%. Khối lượng xenlulozơ cần để sản xuất 1 tấn cao su Buna là:
Đáp án: B Phương pháp giải: Sơ đồ: (C6H10O5)n → nC6H12O6 → 2nC2H5OH →nCH2=CH-CH=CH2 → (-CH2-CH=CH-CH2-)n (cao sư Bu –Na) Không mất tính tổng quát của bài toán, bỏ qua hệ số n để tính toán cho thuận tiện Khối lượng tinh bột là:\({m_{tinh\,bot\,}} = {n_{tinh\,bot\,}}.{M_{tinh\,bot}}.{{100\% } \over {\% {H_3}}}.{{100\% } \over {\% {H_2}}}\,.{{100\% } \over {\% {H_1}}} = ?(\tan )\) Lời giải chi tiết: Sơ đồ: (C6H10O5)n → nC6H12O6 → 2nC2H5OH →nCH2=CH-CH=CH2 → (-CH2-CH=CH-CH2-)n (cao sư Bu –Na) Không mất tính tổng quát của bài toán, bỏ qua hệ số n để tính toán cho thuận tiện 1 tấn cao su buna có số mol là: \(n = {1 \over {54}}\,(\tan \,mol)\) Từ sơ đồ pư => \({n_{tinh\,bot\,}} = n{\,_{cao\,su\,bu\,na}}\, = {1 \over {54}}\,(\tan \,mol)\) Khối lượng tinh bột là: \({m_{tinh\,bot\,}} = {1 \over {54}}.162.{{100\% } \over {60\% }}.{{100\% } \over {80\% }}\,.{{100\% } \over {35\% }} = 17,857(\tan )\) Đáp án B Câu hỏi 25 : Tiến hành trùng hợp 1 mol etilen ở điều kiện thích hợp, đem sản phẩm sau trùng hợp tác dụng với dung dịch brom dư thì lượng brom phản ứng là 36 gam. Hiệu suất phản ứng trùng hợp và khối lượng polietilen (PE) thu được là :
Đáp án: B Phương pháp giải: Phương pháp: Bảo toàn khối lượng Lời giải chi tiết: CH2=CH2 + Br2 → C2H4Br2 =>nC2H4 dư = nBr2 = 0,225 mol => nC2H4 pư = 1 - 0,225 = 0,775 mol Đáp án B Câu hỏi 26 :
Đáp án: B Phương pháp giải: \( + \% H = {{{m_{tt}}} \over {{m_{lt}}}}.100\% \) Với chất tham gia phản ứng chính là lượng lí thuyết. Lời giải chi tiết:
Câu hỏi 27 : Tiến hành thí nghiệm của 1 vài vật liệu polime với dung dịch kiềm theo các bước sau đây : - Bước 1 : Lấy 4 ống nghiệm đựng lần lượt các chất PE, PVC , sợi len, xenlulozo theo thứ tự 1,2,3,4 - Bước 2 : Cho vào mỗi ống nghiệm 2 ml dung dịch NaOH 10% đun sôi, để nguội - Bước 3 : Gạt lấy lớp nước ở mỗi ống nghiệm ta được tương ứng là các ống nghiệm 1’,2’,3’,4’ - Bước 4 : Thêm HNO3 và vài giọt AgNO3 vào ống nghiệm 1’,2’. Thêm vài giọt CuSO4 vào ống 3’,4’. Phát biểu nào sau đây sai :
Đáp án: B Phương pháp giải: Lý thuyết về tính chất hóa học của polime Lời giải chi tiết: - PE (-CH2-CH2-)n không phản ứng với NaOH và AgNO3 - PVC (-CH2-CHCl-)n + nNaOH → (CH2-CHOH-)n + NaCl Khi gạt lấy lớp nước thì cũng bao gồm các chất tan trong nước => không còn NaCl => không có phản ứng với AgNO3/HNO3 => không thể có kết tủa trắng - Sợi len nếu làm từ hữu cơ (polypeptit) thì sẽ phản ứng với Cu(OH)2/OH- tạo màu tím đặc trưng CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4 - Xenlulozo không phản ứng với NaOH, khi thêm CuSO4 vào thì xuất hiện màu xanh của CuSO4. Đáp án B Câu hỏi 28 : Từ 4 tấn C2H4 có chứa 30% tạp chất có thể điều chế bao nhiêu tấn PE ? (Biết hiệu suất phản ứng là 90%)
Đáp án: C Phương pháp giải: + Bảo toàn khối lượng cacbon + Công thức tính hiệu suất: \(\% H = \frac{{{m_{tt}}}}{{{m_{lt}}}}.100\% \) Với chất tạo ra ( sản phẩm) là lượng thực tế thu được. Lời giải chi tiết: Do C2H4 có chứa 30% tạp chất nên lượng C2H4 tinh khiết chiếm 70%. Khối lượng C2H4 phản ứng là: 4 . 70% . 90% = 2,52 tấn Theo BTKL: mPE = mC2H4 pư = 2,52 tấn Đáp án C Câu hỏi 29 : Từ 2 tấn C2H4 có chứa 20% tạp chất có thể điều chế bao nhiêu tấn PE? (biết hiệu suất phản ứng là 95%)
Đáp án: D Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải: m C2H4 = 2.0,8 = 1,6 (tấn) nC2H4 (phản ứng) = 1,6. 0,95 = 1,52 (tấn) mPE = 1,52 (tấn) Đáp án D Câu hỏi 30 : Khi trùng ngưng 13,1 gam axit ε-aminocaproic với hiệu suất 80%, ngoài aminoaxit còn dư ta còn thu được m gam polime và 1,44 gam nước. m có giá trị là
Đáp án: B Phương pháp giải: ε-aminocaproic có công thức là H2N-(CH2)5-COOH Phản ứng trùng ngưng: nH2N-(CH2)5-COOH → [-HN-(CH2)5-CO-]n + nH2O BTKL: m polime = m aminoaxit pư – mH2O = ? Lời giải chi tiết: ε-aminocaproic có công thức là H2N-(CH2)5-COOH Phản ứng trùng ngưng: nH2N-(CH2)5-COOH → [-HN-(CH2)5-CO-]n + nH2O BTKL: m polime = m aminoaxit pư – mH2O = 13,1.80% - 1,44 = 9,04 gam Đáp án B
|