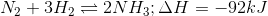40 câu hỏi lý thuyết về amoniac và muối amoni có lời giải (phần 2)Làm bàiCâu hỏi 1 : Trong phương trình phản ứng sau: NH3 + HNO3 → NH4NO3. Vai trò của NH3 là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: NH3 là chất nhận proton (H+) nên thể hiện tính bazo. Đáp án C Câu hỏi 2 : Bột nở là chất bột thường được sử dụng trong nấu ăn và tạo xốp cho nhiều loại bánh vì có khả năng tạo thành khí, làm tăng thể tích của bánh. Điều này được thể hiện qua phương trình
Đáp án: D Phương pháp giải: Lời giải chi tiết: Bột nở là NH4HCO3, bị nhiệt phân theo PTHH: NH4HCO3 Đáp án D Câu hỏi 3 : Tiến hành làm thí nghiệm đun nóng muối amoni clorua trên ngọn lửa đèn cồn, để một mẫu quỳ tím ẩm gần miệng ống nghiệm. Quỳ tím sẽ chuyển thành:
Đáp án: D Phương pháp giải: Viết PTHH nhiệt phân NH4Cl, dựa vào khối lượng riêng của các khí sinh ra để nêu hiện tượng thí nghiệm. Lời giải chi tiết: NH4Cl → NH3 + HCl Vì NH3 bay hơi nhanh hơn, nhẹ hơn bay lên trước => làm quì hóa xanh Sau đó, NH3 bay hết thì HCl bay lên và làm quì tím hóa đỏ Đáp án D Câu hỏi 4 : Cho phản ứng tổng hợp sau : Yếu tố không giúp tăng hiệu suất phản ứng là:
Đáp án: A Phương pháp giải: Dựa vào nguyên lí chuyển dịch cân bằng Lơ-sa-tơ-li-ê. Lời giải chi tiết: Các biện pháp nhằm tăng hiệu suất phản ứng thực chất là tăng chiều thuận của phản ứng. A. Phản ứng là phản ứng tỏa nhiệt vì có ΔH<0. Tăng nhiệt độ → phản ứng xảy ra theo chiều thu nhiệt → CB chuyển dịch theo chiều nghịch → giảm hiệu suất B. Tăng áp suất → phản ứng xảy ra theo chiều làm giảm số mol phân tử khí → CB chuyển dịch theo chiều thuận → tăng hiệu suất C. Lấy NH3 → phản ứng xảy ra theo chiều làm tăng lượng NH3 → CB chuyển dịch theo chiều thuận → tăng hiệu suất D. Bổ sung khí N2 → phản ứng xảy ra theo chiều làm giảm lượng N2 → CB chuyển dịch theo chiều thuận → tăng hiệu suất Đáp án A Câu hỏi 5 : Hiện tượng quan sát được khi cho từ từ đến dư dung dịch NH3 vào muối Al(NO3)3 là:
Đáp án: A Phương pháp giải: Lời giải chi tiết: Khi cho từ từ đến dư dung dịch NH3 vào muối Al(NO3)3 xảy ra phản ứng hóa học: 3NH3 + 3H2O + Al(NO3)3 → Al(OH)3 ↓ + 3NH4NO3 NH3 có tính bazo rất yếu nên không hòa tan được Al(OH)3. Vậy hiện tượng quan sát được là xuất hiện kết tủa keo trắng tăng dần đến cực đại và không tan trong dung dịch NH3 dư. Đáp án A Câu hỏi 6 : Sục khí NH3 đến dư vào dung dịch nào dưới đây để thu được kết tủa?
Đáp án: D Phương pháp giải: Lời giải chi tiết: AlCl3 + 3NH3 + 3H2O → Al(OH)3 ↓ + 3NH4Cl CuCl2 + 2NH3 + 2H2O → Cu(OH)2 ↓ + 2NH4Cl Cu(OH)2 + 4NH3 -> [Cu(NH3)4](OH)2 (tan) Đáp án D Câu hỏi 7 : Cho NH3 dư lần lượt vào các dung dịch: CuSO4, AgNO3, Zn( NO3 )2, AlCl3, FeSO4, NaBr, MgCl2. Có bao nhiêu dung dịch tạo phức với NH3 ?
Đáp án: B Phương pháp giải: Lời giải chi tiết: Trừ AlCl3, FeSO4, NaBr, MgCl2 Chú ý đây là phản ứng dùng để phân biệt các hợp chất của Al và Zn Đáp án B Câu hỏi 8 : Có bao nhiêu liên kết cộng hóa trị trong phân tử amoniac
Đáp án: B Phương pháp giải: Phương pháp: Mỗi dấu “-” trong công thức cấu tạo ứng với 1 liên kết cộng hóa trị Lời giải chi tiết:
Hướng dẫn giải: CTCT => Trong phân tử NH3 có 3 liên kết cộng hóa trị Đáp án B. Câu hỏi 9 : Nhận định nào sau đây đúng về tính chất vật lí của muối amoni
Đáp án: D Phương pháp giải: Phương pháp: Tính chất vật lí của muối amoni -Tính tan: tốt - Độ bền với nhiệt: kém bền Lời giải chi tiết:
Hướng dẫn giải: => cả A,B đều đúng Đáp án D. Câu hỏi 10 : Hiện tượng quan sát được (tại vị trí chứa CuO) khi dẫn khí NH3 đi qua ống đựng bột CuO nung nóng là
Đáp án: C Phương pháp giải: Phương pháp: Do khí NH3 có khả năng khử oxít của các kim loại đứng sau nhôm => kim loại + N2 + H2O Lời giải chi tiết:
Hướng dẫn giải: Do khí NH3 có khả năng khử oxít của các kim loại đứng sau nhôm => NH3 khử CuO tạo ra Cu => hiện tượng là chất rắn màu đen chuyển sang màu đỏ NH3 +CuO -> Cu + N2 +H2O đen đỏ Đáp án C. Câu hỏi 11 : Nhận định nào sau đây đúng về NH3 1. Tan tốt trong nước 2. Là chất khí không màu , không mùi, không vị 3. Là chất khí không màu, mùi khai 4. NH3 có tính bazơ yếu 5. Là chất khí nhẹ hơn không khí
Đáp án: A Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải: 1. Tan tốt trong nước => đúng. NH3 tan rất tốt trong nước => dung dịch amoniac 2. Là chất khí không màu , không mùi, không vị => sai (NH3 là chất khí không màu , mùi khai) 3. Là chất khí không màu, mùi khai=> đúng 4. NH3 có tính bazơ yếu => đúng. NH3 làm quỳ ẩm chuyển màu xanh 5. Là chất khí nhẹ hơn không khí => đúng. MNH3 = 17< Mkk Đáp án A. Câu hỏi 12 : Dung dịch amoniac có thể hòa tan được Cu(OH)2 là do
Đáp án: C Phương pháp giải: Phương pháp: Dung dịch amoniac có khả năng hòa tan hidroxit hay muối ít tan của một số kim loại (Cu, Ag, Zn...) để tạo dung dịch phức chất Lời giải chi tiết:
Hướng dẫn giải: Dung dịch amoniac có thể hòa tan được Cu(OH)2 là do Cu(OH)2 có khả năng tạo phức chất tan với dung dịch amoniac Cu(OH)2 + 4NH3 -> [Cu(NH3)4](OH)2 (dung dịch phức màu xanh thẫm) Đáp án C. Câu hỏi 13 : Cho các phát biểu về NH3 và NH4+ như sau: (1) Trong NH3 và NH4+, nitơ đều có số oxi hóa -3; (2) NH3 có tính bazơ, NH4+ có tính axit; (3) Trong NH3 và NH4+, đều có cộng hóa trị 3; (4) Phân tử NH3 và ion NH4+ đều chứa liên kết cộng hóa trị. Số phát biểu đúng là
Đáp án: D Phương pháp giải: Lời giải chi tiết: Các phát biểu đúng là: (1), (2), (3), (4) Đáp án D Câu hỏi 14 : Sản phẩm khi nhiệt phân muối (NH4)2Cr2O7
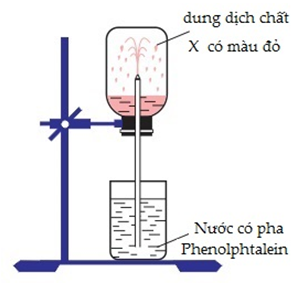
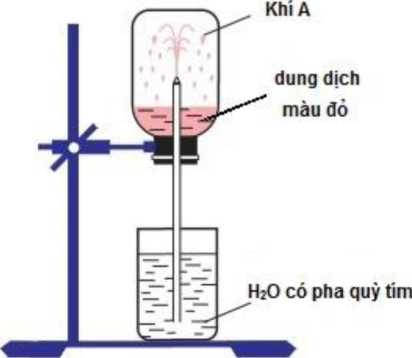
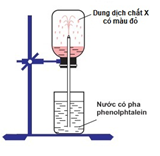
Đáp án: B Phương pháp giải: Lời giải chi tiết: (NH4)2Cr2O7 \(\xrightarrow{{{t^o}}}\) Cr2O3 + N2 + 2H2O Đáp án B Câu hỏi 15 : Thí nghiệm được tiến hành như hình vẽ chứng minh được tính chất gì của khí A
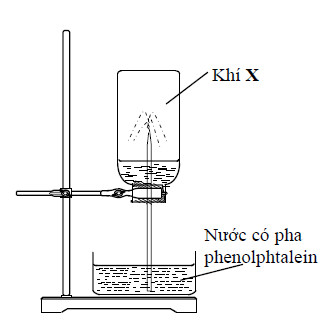
Đáp án: A Phương pháp giải: Lời giải chi tiết: Thí nghiệm cho thấy X làm dd phenol phatalein có màu đỏ → X có tính bazo Và X tan trong nước thành dung dịch đồng nhất → Đáp án A Đáp án A Câu hỏi 16 : Nạp đầy khí X vào bình thủy tinh trong suốt, đậy bình bằng nút cao su có ống thủy tinh có vuốt nhọn xuyên qua.Nhúng đầu ống thủy tinh vào chậu thủy tinh chứa nước có pha phenolphtalein. Một lát sau nước trong chậu phun vào bình thành những tia có màu hồng (hình vẽ minh họa ở bên). Khí X là
Đáp án: A Phương pháp giải: Lời giải chi tiết: Khí X tan trong nước tạo thành dd làm hồng dd phenol phatalein => dd tạo thành có môi trường bazo => Khí X là NH3 Đáp án A Câu hỏi 17 : Cho vài giọt quỳ tím vào dung dịch NH3 thì dung dịch chuyển thành?
Đáp án: D Phương pháp giải: Lời giải chi tiết: Dd NH3 có môi trường bazo nên làm quỳ tím chuyển sang màu xanh Đáp án D Câu hỏi 18 : Cho vài giọt phenolphtalein vào dung dịch NH3 thì dung dịch chuyển thành
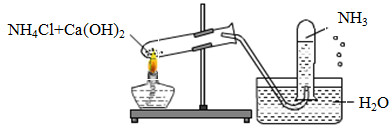
Đáp án: C Phương pháp giải: Lời giải chi tiết: PVC : (-CH2-CH)-n Cl Khí X là HCl HCl + AgNO3 → AgCl↓ trắng + HNO3 Đáp án C Câu hỏi 19 : Một học sinh đã điều chế và thu khí NH3 theo sơ đồ sau đây, nhưng kết quả thí nghiệm không thành công. Lí do chính là:
Đáp án: B Phương pháp giải: Dựa vào tính tan của NH3 Lời giải chi tiết: NH3 tan nhiều trong nước nên ta không sử dụng phương pháp đẩy nước để thu khí. Đáp án B Câu hỏi 20 : Ion NH4+ có tên gọi:
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án A Câu hỏi 21 : Thành phần của dung dịch NH3 gồm:
Đáp án: C Phương pháp giải: Viết phương trình điện li của NH3 trong nước Lời giải chi tiết: \(N{H_3} + {H_2}O \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over Như vậy dung dịch NH3 gồm: NH4+, OH-, NH3 và H2O Đáp án C Câu hỏi 22 : Phát biểu nào dưới đây không đúng:
Đáp án: C Phương pháp giải: Dựa vào tính chất vật lý và hóa học của NH3. Lời giải chi tiết: C sai vì NH3 là chất có mùi khai Đáp án C Câu hỏi 23 : Tính chất hóa học cơ bản của NH3 là
Đáp án: B Phương pháp giải: Dựa vào tính chất hóa học của NH3. Lời giải chi tiết: NH3 có tính bazo yếu do còn 1 cặp e chưa tham gia liên kết. NH3 có tính khử vì N có số oxi hóa thấp nhất là -3 nên chỉ có khả năng nhường e. Đáp án B Câu hỏi 24 : Trong phòng thí nghiệm, người ta điều chế N2 từ
Đáp án: A Phương pháp giải: Dựa vào kiến thức được học về điều chế N2 trong PTN trong sgk hóa 11 – trang 31 Lời giải chi tiết: Trong phòng thí nghiệm, người ta điều chế khí N2 từ NH4NO2 \(N{H_4}N{O_2}\buildrel {{t^0}} \over Đáp án A Câu hỏi 25 : Dung dịch (đặc) nào sau đây khi tiếp xúc với dung dịch NH3 đặc sẽ tạo thành khói trắng ?
Đáp án: A Phương pháp giải: Lời giải chi tiết: Dd HCl đậm đặc tiếp xúc với NH3 đặc sẽ tạo ra khói trắng HCl + NH3 → NH4Cl (khói trắng) Đáp án A Câu hỏi 26 : Cho vài giọt quỳ tím vào dung dịch NH3 thì dung dịch chuyển thành
Đáp án: D Phương pháp giải: Ghi nhớ sự đổi màu của quỳ tím + Môi trường axit chuyển sang màu đỏ + Môi trường bazo chuyển sang màu xanh Lời giải chi tiết: Dd NH3 có môi trường bazo nên làm quỳ tím chuyển sang màu xanh Đáp án D Câu hỏi 27 : Chất X ở điều kiện thường là chất khí, có mùi khai, xốc và tan tốt trong nước. X là
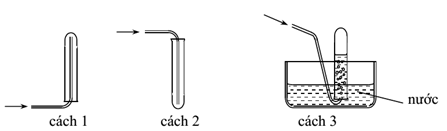
Đáp án: C Phương pháp giải: Dựa vào tính chất vật lí được học về các khí Lời giải chi tiết: Chất X là khí NH3 Đáp án C Câu hỏi 28 : Các chất khí điều chế trong phòng thí nghiệm thường được thu theo phương pháp đẩy không khí (cách 1, cách 2) hoặc đẩy nước (cách 3) như hình vẽ sau đây:
Có thể dùng cách nào trong 3 cách trên để thu khí NH3?
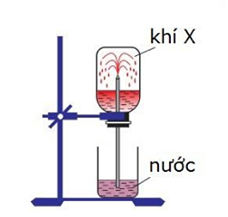
Đáp án: B Phương pháp giải: Cách 1: dùng để điều chế các khí có tỉ khối nhẹ hơn so với không khí Cách 2: dùng để điều chế các khí có tỉ khối nặng hơn so với không khí Cách 3: dùng để điều chế các khí không tan hoặc tan rất ít trong nước Lời giải chi tiết: NH3 là khí mùi khai, tan rất nhiều trong nước => không thể thu NH3 bằng cách 3 đẩy nước được. NH3 có phân tử khối = 17 => nhẹ hơn không khí, do vậy khi thu NH3 bằng cách đẩy không khí mình phải úp ống nghiệm xuống dưới => cách 1 dùng để thu khí NH3 Đáp án B Câu hỏi 29 : Trong phòng thí nghiệm, có thể chứng minh khả năng hòa tan rất tốt trong nước của một số chất khí theo hình vẽ:
Thí nghiệm trên được sử dụng với các khí nào sau đây
Đáp án: B Phương pháp giải: Theo hình vẽ thì khí này tan tốt trong nước Xem lại tính tan của các khí CO2, Cl2, SO2,N2,O2,H2,HCl và NH3 Lời giải chi tiết: Theo hình vẽ chất khí này tan tốt trong nước → Thí nghiệm trên được sử dụng với các khí : HCl và NH3 là hai khí tan tốt trong nước Đáp án B Câu hỏi 30 : Hình vẽ bên mô tả hiện tượng của thí nghiệm thử tính tan của khí A trong nước. Khí A có thể là khí nào trong các khí sau:
Đáp án: C Phương pháp giải: Tính chất hóa học của phi kim Lời giải chi tiết: Khí trong bình khi hòa tan trong dung dịch quì tím có màu đỏ => dung dịch có tính axit Mặt khác, khi khí tan khiến có nước ở bình dưới phun lên bình trên => chứng tỏ khí tan rất mạnh trong nước làm giảm áp suất trong bình trên => chênh lệch áp suất => nước bị kéo từ bình dưới đi lên. => Chỉ có khí HCl thỏa mãn 2 điều kiện trên Đáp án C Câu hỏi 31 : Thử tính tan của X bằng cách úp ngược bình đựng khí vào chậu nước có pha sẵn vài giọt phenolphtalein như hình vẽ sau: Khí X là:
Đáp án: D Phương pháp giải: Lời giải chi tiết: X làm dung dịch phenolphtalein chuyển hồng => dung dịch X có tính bazo => khí X là NH3 Đáp án D Câu hỏi 32 : Thuốc thử để nhận biết khí NH3 là
Đáp án: Phương pháp giải: Dựa vào tính chất hoá học của ammonium Lời giải chi tiết: - Thuốc thử để nhận biết khí NH3 là quỳ tím ẩm vì NH3 làm quỳ tím chuyển sang màu xanh. - NH3 không phản ứng với 3 chất còn lại nên không dùng 3 chất này để nhận biết. Đáp án B Câu hỏi 33 : Cho các phản ứng sau: (1) 2NH3 + H2SO4 → (NH4)2SO4. (2) 4NH3 + 3O2 2N2 + 6H2O. (3) 2NH3 + 3Cl2 N2 + 6HCl. (4) 3NH3 + 3H2O + Al(NO3)3 → Al(OH)3 +3NH4NO3. (5) 4NH3 + 5O2 4NO + 6H2O. (6) 2NH3 + 3CuO 3Cu + 3N2 + 3H2O Các phản ứng trong đó NH3 có tính khử là
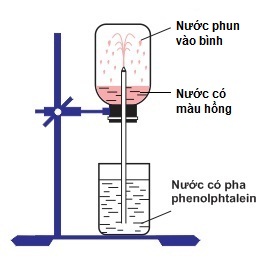
Đáp án: C Phương pháp giải: Chất khử là chất nhường electron → Số oxi hóa tăng Lời giải chi tiết: (1) sai vì số oxi hóa của nguyên tố N không đổi (trước và sau pư đều là -3) (2) đúng vì N-3 → N0 (3) đúng vì N-3→ N0 (4) sai vì số oxi hóa của nguyên tố N không đổi (trước và sau pư đều là -3) (5) đúng vì N-3 → N+2 (6) đúng vì N-3 → N0 Đáp án C Câu hỏi 34 : Thực hiện thí nghiệm như hình vẽ dưới đây:
Bên trong bình, lúc đầu có chứa khí X. Hiện tượng xảy ra khi tiến hành thí nghiệm: nước phun mạnh vào bình và chuyển thành màu hồng. Khí X là
Đáp án: A Phương pháp giải: - Vì nước phun mạnh vào bình chứa khí X nên khí X tan tốt trong nước - Nước chứa phenolphthalein chuyển màu hồng nên X tác dụng H2O tạo thành dung dịch có tính bazo → X Lời giải chi tiết: - Vì nước phun mạnh vào bình chứa khí X nên khí X tan tốt trong nước (khi bị hòa tan thì thể tích khí trong bình giảm nên nước phun vào bình). - Nước chứa phenolphthalein chuyển màu hồng nên X tác dụng H2O tạo thành dung dịch có tính bazo Vậy X là NH3 Đáp án A Câu hỏi 35 : NH3 có thể phản ứng được với tất cả các chất trong nhóm nào sau đây (các điều kiện coi như có đủ)
Đáp án: B Phương pháp giải: Dựa vào tính chất hóa học của NH3 trong sgk hóa 11 Lời giải chi tiết: A. Loại KOH không có pư B. Thỏa mãn NH3 + HCl → NH4Cl NH3 + O2 \(\buildrel {{t^0}} \over\longrightarrow \) N2 + H2O NH3 + Cl2 → NH4Cl + N2 NH3 + CuO \(\buildrel {{t^0}} \over\longrightarrow \) Cu + N2 + H2O NH3 + AlCl3 + H2O → Al(OH)3 + NH4Cl C. Loại KOH D. Loại NaOH Đáp án B Câu hỏi 36 : Phát biểu nào sau đây sai?
Đáp án: A Phương pháp giải: Lý thuyết về amoniac. Lời giải chi tiết: A sai vì NH3 không phải là nhiên liệu tên lửa mà là N2H4 B, C, D đúng Đáp án A Câu hỏi 37 : Cho NH3 dư vào dung dịch chất nào sau đây, thu được kết tủa?
Đáp án: C Phương pháp giải: Ghi nhớ: NH3 có thể hòa tan Cu(OH)2, Zn(OH)2, Ag2O tạo thành dung dịch phức chất nên không thu được kết tủa. Lời giải chi tiết: Cho NH3 dư vào dung dịch FeSO4 ta thu được kết tủa. FeSO4 + 2NH3 + 2H2O → Fe(OH)2 ↓ + (NH4)2SO4 Chú ý: NH3 có thể hòa tan Cu(OH)2, Zn(OH)2, Ag2O tạo thành dung dịch phức chất nên không thu được kết tủa. Đáp án C Câu hỏi 38 : Sản phẩm thu được khi nhiệt phân hoàn toàn muối NH4HCO3 là
Đáp án: D Phương pháp giải: Viết PTHH của phản ứng nhiệt phân NH4HCO3 từ đó xác định các sản phẩm thu được. Lời giải chi tiết: PTHH: \(N{H_4}HC{O_3}\xrightarrow{{{t^o}}}N{H_3} + {H_2}O + C{O_2}\) Vậy sản phẩm thu được khi nhiệt phân hoàn toàn muối NH4HCO3 là NH3, H2O, CO2. Đáp án D Câu hỏi 39 : Phương trình phản ứng nhiệt phân nào sau đây sai?
Đáp án: B Phương pháp giải: Dựa vào kiến thức về phản ứng nhiệt phân của muối amoni Lời giải chi tiết: Sai sửa lại: NH4NO3 \(\xrightarrow{{{t^0}}}\) N2O + 2H2O Đáp án B Câu hỏi 40 : Phản ứng nào dưới đây NH3 không đóng vai trò chất khử?
Đáp án: C Phương pháp giải: NH3 + 3CuO \(\xrightarrow{{{t^0}}}\) 3Cu + N2 + 3H2O Lời giải chi tiết: Phản ứng mà số oxi hóa của N trong NH3 không tăng sau phản ứng thì NH3 không đóng vai trò chất khử \(A.\,4\mathop N\limits^{ - 3} {H_3} + 5{O_2}\xrightarrow{{{t^0}}}4\mathop N\limits^{ + 2} O + 6{H_2}O\) \(B.\,2\mathop N\limits^{ - 3} {H_3} + 3\mathop {C{l_2}}\limits^0 \to \mathop {{N_2}}\limits^0 + 6HCl\) \(C.\,\,\mathop N\limits^{ - 3} {H_3} + {H_2}{O_2} + MnS{O_4} \to Mn{O_2} + {(\mathop N\limits^{ - 3} {H_4})_2}S{O_4}\) \(D.\,\,\mathop N\limits^{ - 3} {H_3} + 3CuO\xrightarrow{{{t^0}}}3Cu + \mathop {{N_2}}\limits^0 + 3{H_2}O\) Ta thấy phản ứng ở đán án C NH3 không có sự thay đổi số oxi hóa trước và sau phản ứng → không đóng vai trò là chất khử. Các phản ứng còn lại số oxi hóa của N trong NH3 đều tăng sau phản ứng nên NH3 đóng vai trò là chất khử Đáp án C
|













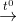 N2O + 2H2O.
N2O + 2H2O.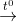 N2 + 2H2O.
N2 + 2H2O.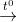 NH3 + HCl.
NH3 + HCl.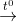 NH3 + CO2 + H2O.
NH3 + CO2 + H2O.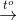 NH3 + CO2 + H2O
NH3 + CO2 + H2O