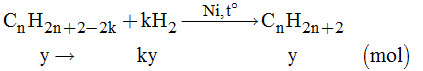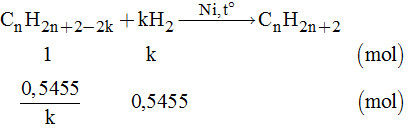Đề kiểm tra 1 tiết (45 phút) - Đề số 2 - Chương VI - Hóa học 11Đáp án và lời giải chi tiết Đề kiểm tra 1 tiết (45 phút) - Đề số 2 - Chương VI - Hóa học 11 Đề bài I. PHẦN TRẮC NGHIỆM Câu 1. Dẫn một hỗn hợp khí gồm etan và etilen (đktc) đi qua dung dịch nước brom, thấy khối lượng brom tăng tham gia phản ứng là 8 gam. Thể tích khí bị nước brom hấp thụ là: A.3,36 lít B.5,60 lít C.4,48 lít C.1,12 lít Câu 2. Một hỗn hợp khí chứa ankan X và anken Y có cùng số cacbon và cùng số mol. Nếu dẫn a gam hỗn hợp khí này vào nước brom thì cần vừa đủ 80 gam dung dịch brom 20%. Đốt cháy hoàn toàn a gam hỗn hợp trên thu được 0,6 mol CO2. Công thức phân tử của X và Y lần lượt là: A.C2H6 và C2H4 B.C3H8 và C3H6 C.C5H10 và C5H12 D.C4H10 và C4H8 Câu 3. Khi đốt cháy hoàn toàn hiđrocacbon X thu được số mol CO2 bằng số mol H2O. Hỏi X thuộc dãy đồng đẳng nào sau đây? A.Ankanđien B.Ankan C.Xicloankan D.Anken hoặc xicloankan. Câu 4. Cho các công thức cấu tạo sau đây: \(\begin{array}{l}\left( a \right)C{H_3}CH = C{H_2}{\rm{ }}\\\left( b \right)C{H_3}CH = CHCl{\rm{ }}\\\left( c \right)C{H_3}CH = C{\left( {C{H_3}} \right)_2}\\\left( d \right){C_2}{H_5}C\left( {C{H_3}} \right) = C\left( {C{H_3}} \right){C_2}{H_5}{\rm{ }}\\\left( e \right)C{H_3}C\left( {{C_2}{H_5}} \right) = CHCl\end{array}\) Những hợp chất nào ở trên có đồng phân cis – trans? A.(a). (b), (c) B.(b), (d), (e) C.(c), (d), (e) D.(a), (b), (d) Câu 5. Khi cho hai anken có công thức phân tử C3H6 và C4H8 phản ứng với HBr thu được ba sản phẩm. Công thức cấu tạo của hai anken trên là: A. propen và but-1-en B. propilen và but-1-en C. propen và but-2-en D. xiclopropan và but-2-en. Câu 6. Khi đốt cháy hỗn hợp (X) gồm một ankan và một anken thu được a mol H2O và b mol CO2. Tỉ số \(T = \dfrac{a}{b}\) có giá trị trong khoảng nào sau đây? A.T = 1 B. 1 < T < 2 C. T = 2 D. 2 < T < 3 Câu 7. Cho 4 lọ mất nhãn lần lượt chứa các khí sau: butan; but-2-en; but-1-in và CO2. Dùng thuốc thử nào sau đây để nhận biết các lọ khí trên? A.Dung dịch Br2 và dung dịch AgNO3/NH3 B.Dung dịch Br2; dung dịch AgNO3/NH3 và dung dịch Ca(OH)2 C.Dung dịch KMnO4 và khí Cl2 D.Dung dịch Ca(OH)2 và dung dịch AgNO3/NH3 Câu 8. Cho phản ứng sau: \({C_2}{H_4} + KMn{O_4} + {H_2}O \to \left( X \right) + \left( Y \right) + KOH\) Trong đó (X) và (Y) lần lượt là các chất nào sau đây? A. C2H5OH và K2MnO4 B. C2H4(OH)2 và K2MnO4 C. C2H5OH và MnO2 D. C2H4(OH)2 và MnO2. II. PHẦN TỰ LUẬN Câu 9. Dẫn 1,12 lít (đktc) hỗn hợp khí gồm C2H2 và C2H4 vào dung dịch nước brom, lượng brom đã tham gia phản ứng là 11,2 gam. Tính thành phần phần trăm theo thể tích mỗi khí trong hỗn hợp ban đầu. Câu 10.Trộn một hỗn hợp X gồm hiđrocacbon A và H2 với \({d_{X/{H_2}}} = 6,1818\). Cho X qua niken đun nóng đến khi phản ứng xảy ra hoàn toàn thì thu được hỗn hợp Y với \({d_{Y/{H_2}}} = 13,6.\) Xác định công thức phân tử của A. Câu 11. Đốt cháy hỗn hợp hai anken X và Y thu được (a + 14) gam H2O và (a + 40) gam CO2. Tính giá trị của a. Lời giải chi tiết I. PHẦN TRẮC NGHIỆM
II. PHẦN TỰ LUẬN Câu 9. nhỗn hợp \( = \dfrac{{1,12}}{{22,4}} = 0,05\left( {mol} \right);\) \({n_{B{r_2}}} = \dfrac{{11,2}}{{160}} = 0,07\left( {mol} \right)\) \(\begin{array}{l}{C_2}{H_4} + B{r_2} \to {C_2}{H_4}B{r_2}{\rm{ }}\left( 1 \right)\\\;\;\;{\rm{ a }} \to {\rm{ \;\;\; a }}\left( {mol} \right)\\{C_2}{H_2} + 2B{r_2} \to {C_2}{H_2}B{r_4}{\rm{ }}\left( 2 \right)\\{\rm{\;\;\; b }} \to {\rm{ \;\;\; 2b }}\left( {mol} \right)\end{array}\) Theo đề bài, ta có hệ phương trình: \(\left\{ \begin{array}{l}a + b = 0,05\\a + 2b = 0,07\end{array} \right. \Rightarrow \left\{ \begin{array}{l}a = 0,03\\b = 0,02\end{array} \right.\) Vậy: \(\% {V_{{C_2}{H_4}}} = \dfrac{{0,03 \times 22,4}}{{1,12}} \times 100\% = 60\% \) \(\% {V_{{C_2}{H_2}}} = 100\% - 60\% = 40\% .\) Câu 10. Gọi x là số mol của H2 và y là số mol của (A): \({C_n}{H_{2n + 2 - 2k}}\) + Giả sử hiđrocacbon hết mà H2 dư
Áp dụng ĐLBTKL ta có: mhỗn hợp trước = mhỗn hợp sau \(\begin{array}{l} \Leftrightarrow \left( {x + y} \right){\overline M _X} = \left( {y + x - ky} \right){\overline M _Y}\\ \Leftrightarrow \dfrac{{{{\overline M }_X}}}{{{{\overline M }_Y}}} = \dfrac{{x + y - ky}}{{x + y}} = \dfrac{{6,1818 \times 2}}{{13,6 \times 2}} = 0,4545\end{array}\) Như vậy cứ 1 mol hỗn hợp trước phản ứng thì sau phản ứng còn 0,4545 mol. Vậy cứ 1 mol hỗn hợp bị mất đi: 1 – 0,4545 = 0,5455 (mol) Xét hỗn hợp: \(\left\{ \begin{array}{l}x + y = 1\\ky = 0,5455\end{array} \right. \Leftrightarrow \left\{ \begin{array}{l}y = \dfrac{{0,5455}}{k}\\x = 1 - \dfrac{{0,5455}}{k}\end{array} \right.\)
Do đó: \(\left( {\dfrac{{0,5455}}{k}.{M_{{C_x}{H_y}}}} \right) + \left( {1 - \dfrac{{0,5455}}{k}} \right).2 = 6.1818 \times 2\) \(\begin{array}{l} \Leftrightarrow 0,5455{M_{{C_x}{H_y}}} + 2k - 1,09 = 12,3636k\\ \Leftrightarrow 0,5455{M_{{C_x}{H_y}}} = 10,3636k + 1,09\\ \Rightarrow 14n = 21k\end{array}\) + Nếu \(k = 1 \Rightarrow n = 1,5\) (loại) + Nếu \(k = 2 \Rightarrow n = 3 \Rightarrow \) CTPT A: C3H4 Câu 11. Gọi công thức tương đương của 2 anken: \({C_{\overline n }}{H_{2\overline n }}\) Phản ứng: \({C_{\overline n }}{H_{2\overline n }} + \dfrac{{3\overline n }}{2}{O_2}\xrightarrow{{t^\circ }}\overline n C{O_2} + \overline n {H_2}O\) Vì khi đốt anken thu được: \({n_{C{O_2}}} = {n_{{H_2}O}}\) \( \Leftrightarrow \dfrac{{a + 40}}{{44}} = \dfrac{{a + 14}}{{18}} \) \(\Leftrightarrow 18a + 720 = 44a + 616 \) \(\Rightarrow a = 4\left( {gam} \right).\) HocTot.Nam.Name.Vn
|