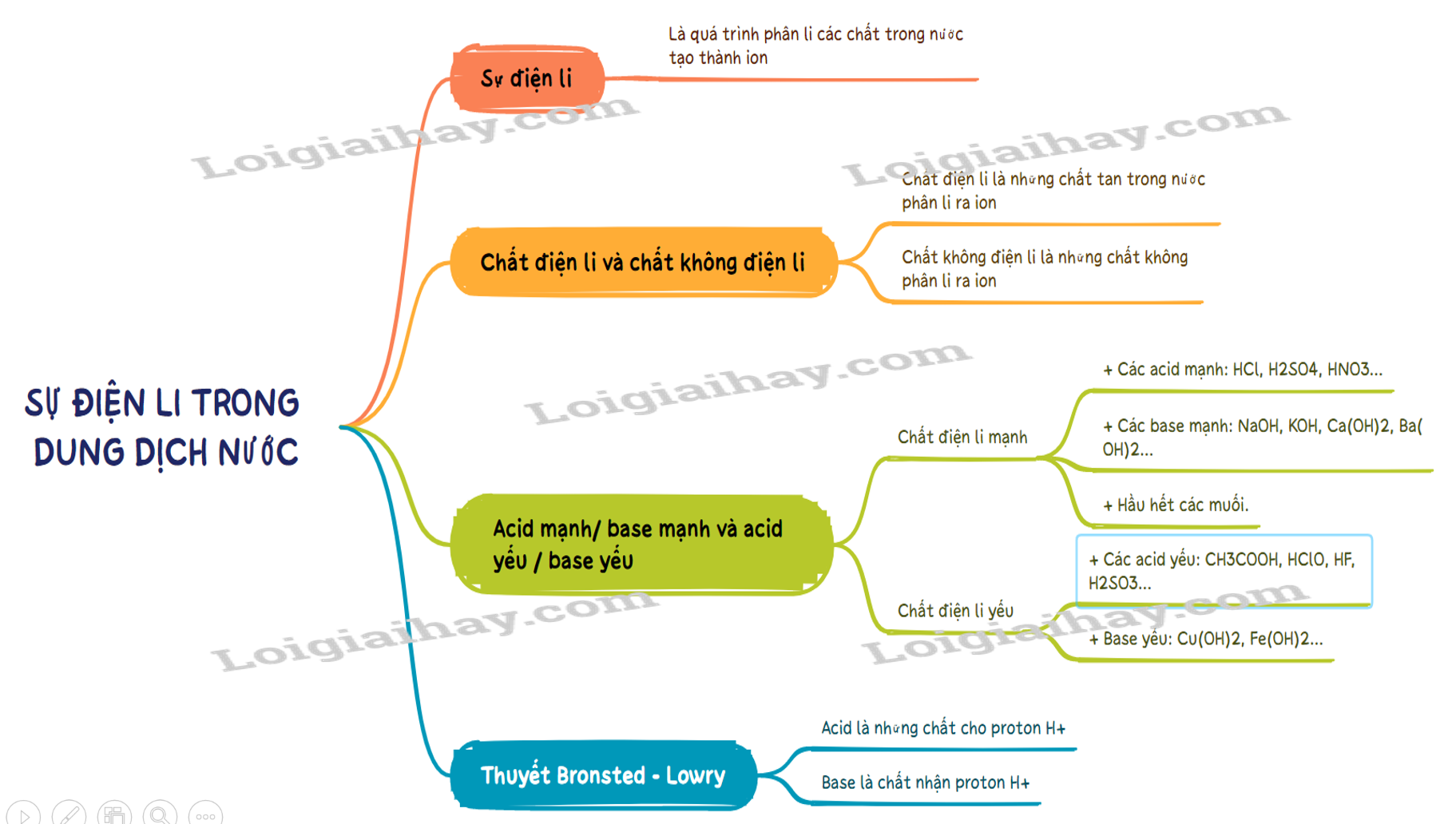
Lý thuyết Sự điện li trong dung dịch nước, thuyết Bronsted - Lowry về acid - base - Hóa học 11 - Cánh diều- Sự điện li là quá trình phân li các chất trong nước tạo thành ion. I. Sự điện li, chất điện li và chất không điện li 1. Sự điện li - Sự điện li là quá trình phân li các chất trong nước tạo thành ion. 2. Chất điện li và chất không điện li - Chất điện li là những chất khi tan trong nước phân li ra các ion - Chất điện li là những chất tan trong nước phân li ra các ion. VD: hydrochloric acid, sodium hydroxide, .. - Chất không điện li là chất không phân li ra các ion. VD: saccarose, ethanol…. II. Thuyết Bronsted – Lowry về acid – base 1. Thuyết Bronsted – Lowry về acid – base a. Khái niệm acid – base theo thuyết Bronsted – Lowry. - Acid là chất cho proton (H+). - Base là chất nhận proton (H+). b. Ưu điểm của thuyết Bronsted – Lowry. Tổng quát hơn thuyết Arhenius. (Phân tử không có nhóm –OH như NH3 hay CO3- cũng là base). 2. Acid mạnh / base mạnh và acid yếu / base yếu - Chất điện li mạnh là chất khi tan trong nước, hầu hết các phân tử chất tan đều phân li ra ion. Thường gặp là: + Các acid mạnh: HCl, H2SO4, HNO3… + Các base mạnh: NaOH, KOH, Ca(OH)2, Ba(OH)2… + Hầu hết các muối. Phản ứng: Một chiều. VD: HNO3 → H+ + NO3-. - Chất điện li yếu là chất khi tan trong nước chỉ có một phần phân tử chất tan phân li ra ion. Thường gặp là: + Các acid yếu: CH3COOH, HClO, HF, H2SO3… + Base yếu: Cu(OH)2, Fe(OH)2… Phản ứng: Thuận nghịch. Biểu diễn: Hai nửa mũi tên ngược nhau (⇆) VD: CH3COOH ⇆ CH3COO- + H+. SƠ ĐỒ TƯ DUY
|














Danh sách bình luận