Lý thuyết MetanI. TRẠNG THÁI TỰ NHIÊN, TÍNH CHẤT VẬT LÍ I. TRẠNG THÁI TỰ NHIÊN, TÍNH CHẤT VẬT LÍ - Trong tự nhiên, metan có nhiều trong các mỏ khí (khí thiên nhiên), trong mỏ dầu (khí mỏ dầu), trong các mỏ than (khí mỏ than). - Metan là chất khí, không màu, không mùi, nhẹ hơn không khí II. CẤU TẠO PHÂN TỬ - Trong phân từ metan chỉ có 4 liên kết đơn
- Những hiđrocacbon mạch hở, phân tử chỉ có liên kết đơn giống như metan gọi là ankan, có công thức chung CnH2n+2, với n > 0. III. TÍNH CHẤT HÓA HỌC 1. Tác dụng với oxi: - Khi đốt trong oxi, metan cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt. CH4 + 2O2 \(\xrightarrow{{{t^o}}}\) CO2 + 2H2O Hỗn hợp gồm một thể tích metan và hai thể tích oxi là hỗn hợp nổ mạnh. 2. Tác dụng với clo khi có ánh sáng:
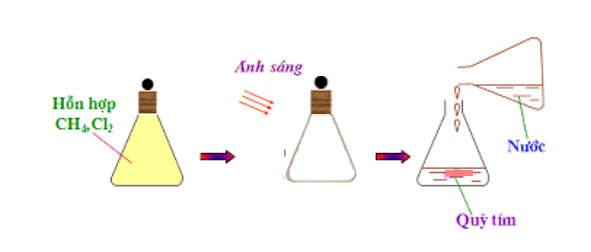
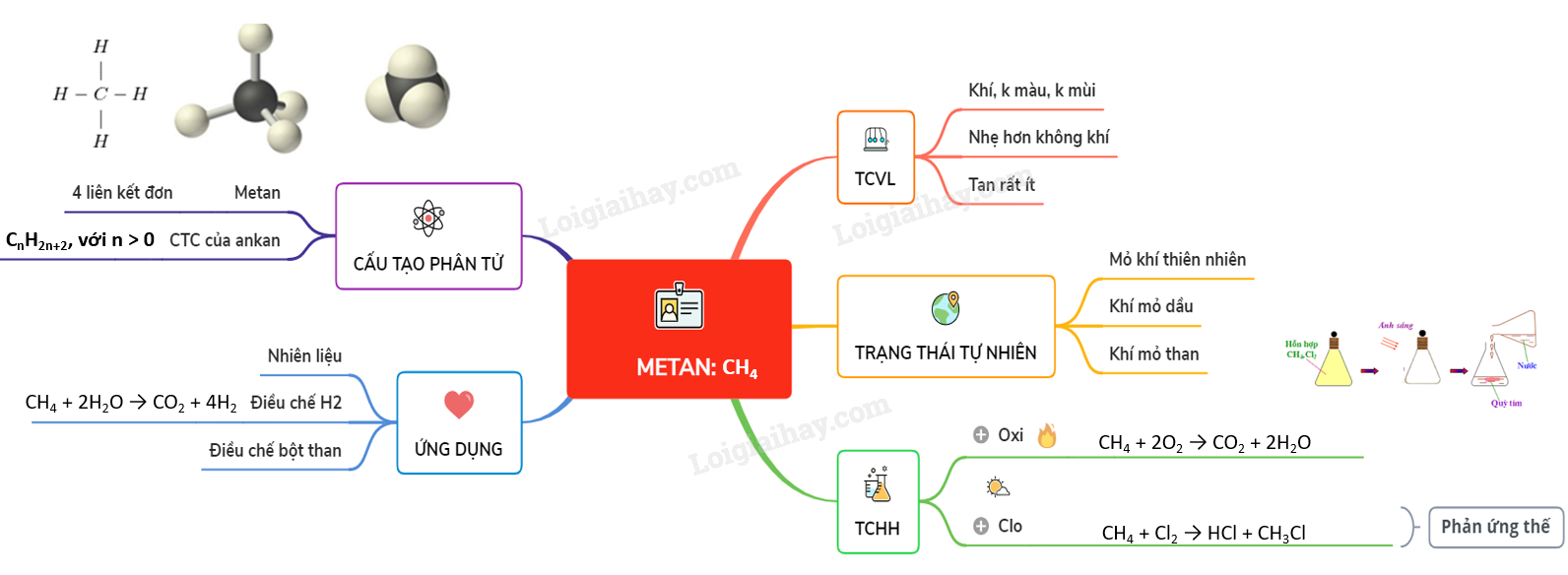
CH4 + Cl2 \(\xrightarrow{{{a/s}}}\) HCl + CH3Cl (metyl clorua) - Ở phản ứng này, nguyên tử H của metan được thay thế bởi nguyên tử Cl, vì vậy được gọi là phản ứng thế. IV. ỨNG DỤNG - Metan cháy tỏa nhiều nhiệt nên được đùng làm nhiên liệu. - Metan là nguyên liệu dùng điều chế hiđro theo sơ đồ: Metan + H2O \( \to\) cacbon đioxit + hiđro - Metan còn được dùng để điều chế bột than và nhiều chất khác. Sơ đồ tư duy: Metan
|













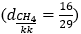 và tan rất ít trong nước.
và tan rất ít trong nước.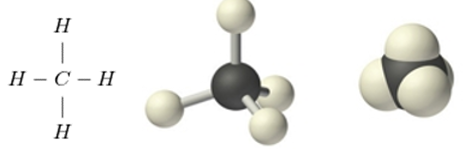

Danh sách bình luận