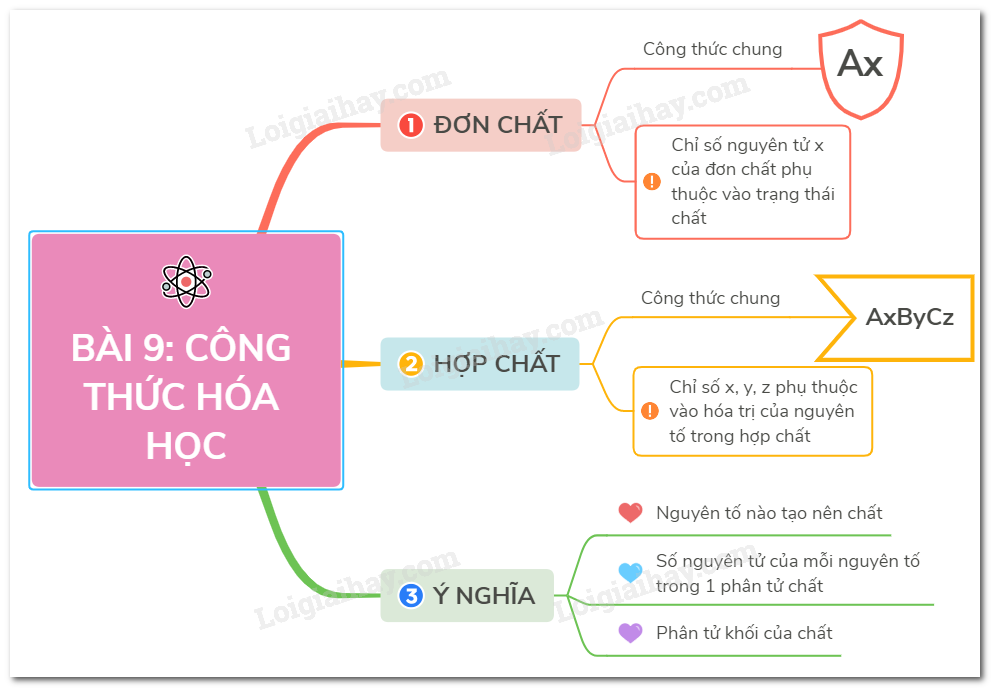
Lý thuyết công thức hóa họcLÝ THUYẾT CẦN NHỚ I. CÔNG THỨC HOÁ HỌC CỦA ĐƠN CHẤT 1. Đơn chất kim loại - Hạt hợp thành là nguyên tử: Ký hiệu hoá học được coi là công thức hoá học. Ví dụ: Cu, Na, Zn, Fe. 2. Đơn chất phi kim - Hạt hợp thành là nguyên tử : Ký hiệu hoá học là công thức hoá học. Ví dụ: C, P, S. - Hạt hợp thành là phân tử (thường là 2 nguyên tử): Thêm chỉ số ở chân ký hiệu. Ví dụ: O2, H2, N2. Kêt luận: Công thức chung của đơn chất là: An - Trong đó : A là kí hiệu hóa học của nguyên tố n là chỉ số (có thể là 1, 2, 3, 4…), nếu n = 1 thì không viết Ví dụ: Cu, H2, O2 II. CÔNG THỨC HOÁ HỌC CỦA HỢP CHẤT - Công thức dạng chung của hợp chất là: AxBy, AxByCz Trong đó: + A, B, C,… là kí hiệu hóa học của từng nguyên tố + x, y, z,… là các số nguyên, là chỉ số nguyên tử của nguyên tố trong một phân tử hợp chất. *Lưu ý: CaCO3 thì CO3 là nhóm nguyên tử. Ví dụ: - CTHH của nước là: H2O - CTHH của muối ăn là: NaCl - CTHH của khí cacbonic là: CO2 III. Ý NGHĨA CỦA CÔNG THỨC HÓA HỌC Mỗi công thức hóa học chỉ 1 phân tử của chất, cho biết - Nguyên tố nào tạo ra chất - Số nguyên tử của mỗi nguyên tố trong 1 phân tử chất - Phân tử khối của chất Ví dụ: Từ công thức hóa học của N2, ta biết được: - Đơn chất được tạo bởi nguyên tố Nitơ - Có 2 nguyên tử Nitơ tạo thành phân tử - Phân tử khối = 14.2 = 28 đvC IV. CÁCH DIỄN ĐẠT CÔNG THỨC HÓA HỌC nAx: n phân tử Ax nAxBy: n phân tử AxBy nA: n nguyên tử A Ví dụ: Sơ đồ tư duy: Công thức hóa học
|














Danh sách bình luận