Đề thi thử THPT chuyên Cao BằngĐề bài
Câu 1 :
Cho các phát biểu sau: (a) Sau khi mổ cá, có thể dùng chanh để giảm mùi tanh. (b) Dầu thực vật và dầu nhớt bôi trơn máy đều có thành phần chính là chất béo. (c) Cao su thiên nhiên là polime của isopren. (d) Khi làm trứng muối (ngâm trứng trong dung dịch NaCl bão hòa) xảy ra hiện tượng đông tụ protein. (e) Thành phần chính của tóc là protein. (g) Để giảm đau nhức khi bị kiến đốt, có thể bôi giấm vào vết đốt. Số phát biểu đúng là
Câu 2 :
Quặng nào sau đây có thành phần chính là Al2O3 ?
Câu 3 :
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất
Câu 4 :
Số đồng phân este ứng với công thức phân tử C3H6O2 là
Câu 5 :
Cho các phát biểu sau: (a) Điện phân dung dịch NaCl với điện cực trơ, thu được khí H2 ở catot (b) Dùng khí CO dư khử CuO nung nóng, thu được kim loại Cu (c) Để hợp kim Fe- Ni ngoài không khí ẩm thì kim loại Ni bị ăn mòn điện hóa học (d) Dùng dung dịch Fe2(SO4)3 dư có thể tách Ag ra khỏi hỗn hợp Ag và Cu (e) Cho Fe dư vào dung dịch AgNO3 sau phản ứng thu được dung dịch chứa hai muối Số phát biểu đúng là
Câu 6 :
Số liên kết peptit tron phân tử Ala – Gly – Ala – Gly là
Câu 7 :
Cho dãy chất : (a) NH3, (b) CH3NH2, (c) C6H5NH2(anilin). Thứ tự tăng dần bazo của các chất trong dãy là
Câu 8 :
Cho các chất sau: etyl fomat, anilin, glucozo, Gly – Ala. Số chất bị thủy phân trong môi trường kiềm là:
Câu 9 :
Một học sinh làm thí nghiệm với dung dịch X đựng trong lọ không dán nhãn và thu được kết quả như sau: X đều phản ứng với cả 3 dung dịch : NaHSO4 , Na2CO3, AgNO3 X không phản ứng với cả 3 dung dịch NaOH, Ba(NO3)2, HNO3 Vậy dung dịch X là dung dịch nào sau đây ?
Câu 10 :
Polime nào sau đây điều chế bằng phản ứng trùng ngưng
Câu 11 :
Hỗn hợp X gồm Al và Fe có tỉ lệ số mol tương ứng là 1:1. Cho 2,49 gam X vào dung dịch chứa 0,17 mol HCl, thu được dung dịch Y. Cho 200 ml dung dịch AgNO3 1M vào Y, thu được khí NO và m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn, NO là sản phẩm khử duy nhất của N+5. Giá trị của m gần nhất với giá trị nào sau đây
Câu 12 :
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hơp khí X, Cho toàn bộ khí X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Câu 13 :
Cho 7,3 gam lysin và 15 gam glyxin vào dung dịch chứa 0,3 mol KOH, thu được dung dịch Y. Cho Y tác dụng hoàn toàn với HCl dư thu được m gam muối. Giá trị của m là
Câu 14 :
Hỗn hợp X gồm axit axetic và metyl fomat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M. Giá trị của m là
Câu 15 :
Phát biểu nào sau đây là sai:
Câu 16 :
Cho các polime: poli(vinyl clorua), xenlulozo, policaproamit, polistiren, xenlulozo trinitrat, nilon – 6,6. Số polime tổng hợp là
Câu 17 :
Dung dịch nào sau đây tác dụng với dung dịch Ba(HCO3)2 vừa thu được kết tủa, vừa có khí thoát ra
Câu 18 :
Khi thủy phân tinh bột thu được sản phẩm cuối cùng là
Câu 19 :
Cho hỗn hợp gồm Zn, Mg và Ag vào dung dịch CuCl2, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp gồm 3 kim loại. Ba kim loại đó là:
Câu 20 :
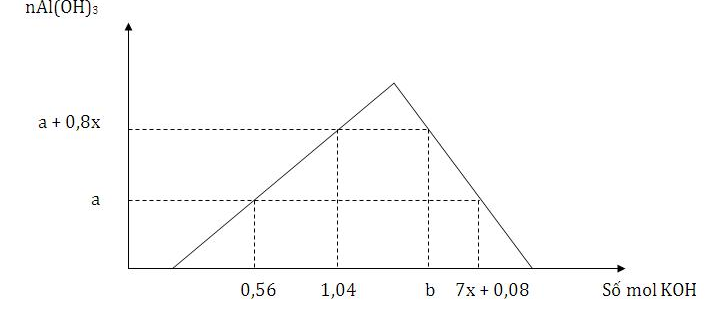
Cho từ từ đến dư dung dịch KOH vào dung dịch hỗn hợp x mol HNO3 và y mol Al(NO3)3, kết quả thí nghiệm được biểu diễn trên đồ thị sau Tỉ lệ của b : a có giá trị là
Câu 21 :
Cho 11,9 gam hỗn hợp Zn và Al phản ứng vừa đủ với dung dịch H2SO4 loãng thu được m gam muối trung hòa và 8,96 lít khí H2 đktc. Giá trị của m là
Câu 22 :
Một số loại khẩu trang y tế chứa hoạt chất bột màu đen có khả năng lọc không khí. Chất đó là
Câu 23 :
Đốt cháy hoàn toàn amin X no, đơn chức, mạch hở, thu được 0,2 mol CO2 và 0,05 mol N2. Công thức phân tử của X là
Câu 24 :
Thực hiện các thí nghiệm sau (a) Sục khí CO2 dư vào dung dịch BaCl2 (b) Cho dung dịch NH3 dư vào dung dịch AlCl3 (c) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 (d) Cho hỗn hợp Na2O và Al2O3 (tỉ lệ mol 1:1) vào nước dư (e) Cho dung dịch Ba(OH)2 dư vào dung dịch Cr2(SO4)3 (f) Cho hỗn hợp bột Cu và Fe3O4 (tỉ lệ mol 1:1) vào dung dịch HCl dư Sau khi các phản ứng xảy ra, số thí nghiệm thu được kết tủa là
Câu 25 :
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 3,26 mol O2, thu được 2,28 mol CO2 và 39,6 gam nước. Mặt khác thủy phân hoàn toàn a gam X trong dung dịch NaOH đun nóng, thu được dung dịch chứa b gam muối. Giá trị của b là
Câu 26 :
Công thức nào sau đây có thể là công thức của chất béo
Câu 27 :
Cho m gam bột Fe vào dung dịch X chứa 0,1 mol Fe(NO3)3 và 0,4 mol Cu(NO3)2. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch Y và m gam chất rắn Z. Giá trị của m là
Câu 28 :
Cho dung dịch NaOH vào dung dịch X, thu được kết tủa màu nâu đỏ. Chất X là
Câu 29 :
Este nào sau đây thủy phân trong môi trường axit thu được 2 chất hữu cơ đều tham gia phản ứng tráng gương?
Câu 30 :
Khi thủy phân hoàn toàn a gam saccarozo trong môi trường axit thu được 81 gam hỗn hợp glucozo và fructozo. Giá trị của a là
Câu 31 :
Cho dãy các chất sau : glucozo, xenlulozo, saccarozo, tinh bột, fructozo. Số chất trong dãy tham gia phản ứng tráng bạc là
Câu 32 :
Dung dịch hỗn hợp X gồm NaCl 0,6M và CuSO40,5M. Điện phân 100 ml dung dịch X (điện cực trơ, màng ngăn xốp, hiệu suất 100%, bỏ qua sự hòa tan của khí trong nước hay sự bay hơi của nước) với cường độ dòng điện không đổi 0,5A trong thời gian t giây. Dung dịch sau điện phân có khối lượng giảm 4,85 gam so với dung dịch ban đầu. Giá trị của t là
Câu 33 :
Hỗn hợp X gồm 2 este đơn chức. Cho 0,3 mol X tác dụng vừa đủ với 250 ml dung dịch KOH 2M, thu được chất hữu cơ Y (no, đơn chức, mạch hở, có tham gia phản ứng tráng bạc) và 53 gam hỗn hợp muối. Đốt cháy hoàn toàn Y cần dùng vừa đủ 5,6 lít khí O2 đktc. Khối lượng của 0,3 mol X là
Câu 34 :
Hòa tan hoàn toàn hỗn hợp K và Na vào nước, thu được dung dịch X và V lít khí H2 đktc. Trung hòa X cần 200 ml dung dịch H2SO4 0,1M. Giá trị của V là
Câu 35 :
Tiến hành các thí nghiệm sau (a) Nhúng thanh đồng nguyên chất vào dung dich FeCl3 (b) Cắt nguyên miếng sắt tây ( sắt tráng thiếc), để trong không khí ẩm (c) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịch CuSO4 (d) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc nước muối Trong các thí nghiệm trên số thí nghiệm chỉ xảy ra ăn mòn điện hóa là
Câu 36 :
Cho a mol este X(C9H10O2) tác dụng vừa đủ với 2a mol NaOH, thu được dung dịch không có phản ứng tráng bạc. Số công thức cấu tạo của X là
Câu 37 :
Cho sơ đồ chuyển hóa Glucozo → X → Y → CH3COOH. Hai chất X, Y là
Câu 38 :
Trong công nghiệp, kim loại nào sau đây chỉ được điều chế bằng phương pháp điện phân nóng chảy?
Câu 39 :
Hợp chất nào sau đây có tính lưỡng tính
Câu 40 :
Cho V ml dung dịch NaOH 2M vào 200 ml dung dịch AlCl3 1M, sau khi phản ứng xảy ra hoàn toàn thu được 3,9 gam kết tủa. Giá trị lớn nhất của V là
Lời giải và đáp án
Câu 1 :
Cho các phát biểu sau: (a) Sau khi mổ cá, có thể dùng chanh để giảm mùi tanh. (b) Dầu thực vật và dầu nhớt bôi trơn máy đều có thành phần chính là chất béo. (c) Cao su thiên nhiên là polime của isopren. (d) Khi làm trứng muối (ngâm trứng trong dung dịch NaCl bão hòa) xảy ra hiện tượng đông tụ protein. (e) Thành phần chính của tóc là protein. (g) Để giảm đau nhức khi bị kiến đốt, có thể bôi giấm vào vết đốt. Số phát biểu đúng là
Đáp án : B Lời giải chi tiết :
(a) đúng vì các amin sẽ phản ứng với chanh tạo muối và bị rửa trôi (b) sai vì dầu nhớt bôi trơn có thành phần chính là các hidrocacbon (c) đúng (d) đúng vì protein bị đông tụ khi đun nóng hoặc khi tiếp xúc với một số muối. (e) đúng (g) sai vì nọc kiến có chứa HCOOH nên bôi giấm (CH3COOH) không có tác dụng, ta nên bôi nước vôi trong Ca(OH)2 để giảm sưng tấy. Vậy có tất cả 4 phát biểu đúng
Câu 2 :
Quặng nào sau đây có thành phần chính là Al2O3 ?
Đáp án : C Lời giải chi tiết :
Quặng hematit đỏ là Fe2O3 Quặng manhetit là Fe3O4 Quặng boxit là Al2O3.2H2O Quặng criolit là Na3AlF6
Câu 3 :
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất
Đáp án : A Phương pháp giải :
Xem lại bài đại cương kim loại hóa 12 Lời giải chi tiết :
Ở nhiệt độ thường Hg là kim loại duy nhất tồn tại thể lỏng → đây là chất có nhiệt độ nóng chảy thấp nhất
Câu 4 :
Số đồng phân este ứng với công thức phân tử C3H6O2 là
Đáp án : C Phương pháp giải :
Viết CTCT của este Lời giải chi tiết :
Các CTCT của C3H6O2 là: HCOOCH2CH3 (1) ;CH3COOCH3(2)
Câu 5 :
Cho các phát biểu sau: (a) Điện phân dung dịch NaCl với điện cực trơ, thu được khí H2 ở catot (b) Dùng khí CO dư khử CuO nung nóng, thu được kim loại Cu (c) Để hợp kim Fe- Ni ngoài không khí ẩm thì kim loại Ni bị ăn mòn điện hóa học (d) Dùng dung dịch Fe2(SO4)3 dư có thể tách Ag ra khỏi hỗn hợp Ag và Cu (e) Cho Fe dư vào dung dịch AgNO3 sau phản ứng thu được dung dịch chứa hai muối Số phát biểu đúng là
Đáp án : C Phương pháp giải :
Xem lại lý thuyết tổng hợp hóa 12 Lời giải chi tiết :
(a) Đúng vì tại catot (-) có 2H2O + 2e → 2OH- + H2 (b) Đúng (c) Sai vì Fe mạnh hơn Ni trong dãy điện hóa nên xảy ra ăn mòn Fe (d) Đúng vì Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4 → tách Ag ra khỏi hỗn hợp Ag và Cu (e) Sai vì chỉ tạo muối Fe(NO3)2
Câu 6 :
Số liên kết peptit tron phân tử Ala – Gly – Ala – Gly là
Đáp án : D Phương pháp giải :
Số liên kết pepit = số mắt xích - 1 Lời giải chi tiết :
Số liên kết peptit trong phân tử Ala – Gly – Ala – Gly là 3
Câu 7 :
Cho dãy chất : (a) NH3, (b) CH3NH2, (c) C6H5NH2(anilin). Thứ tự tăng dần bazo của các chất trong dãy là
Đáp án : D Phương pháp giải :
Thứ tự tăng dần tính bazo : anilin < NH3 < amin bậc 1 ≈ amin bậc 3 (no) < amin bậc 2 (no) Lời giải chi tiết :
Thứ tự tăng dần tính bazo là C6H5NH2 < NH3 < CH3NH2
Câu 8 :
Cho các chất sau: etyl fomat, anilin, glucozo, Gly – Ala. Số chất bị thủy phân trong môi trường kiềm là:
Đáp án : B Phương pháp giải :
Các chất thủy phân trong môi trường kiềm là: este, peptit, axit, phenol Lời giải chi tiết :
Số chất bị thủy phân trong môi trường kiềm là:etyl fomat, Gly – Ala.
Câu 9 :
Một học sinh làm thí nghiệm với dung dịch X đựng trong lọ không dán nhãn và thu được kết quả như sau: X đều phản ứng với cả 3 dung dịch : NaHSO4 , Na2CO3, AgNO3 X không phản ứng với cả 3 dung dịch NaOH, Ba(NO3)2, HNO3 Vậy dung dịch X là dung dịch nào sau đây ?
Đáp án : D Phương pháp giải :
Dựa vào đáp án suy luận với kết quả thí nghiệm => từ đó chọn được X thỏa mãn Lời giải chi tiết :
Mg(NO3)2; CuSO4; FeCl2 không phản ứng với NaHSO4
Câu 10 :
Polime nào sau đây điều chế bằng phản ứng trùng ngưng
Đáp án : A Phương pháp giải :
Phản ứng trùng ngưng là phản ứng tổng hợp polyme dựa vào phản ứng của các monome chứa các nhóm chất, tạo thành liên kết mới và đồng thời sinh ra chất phụ như nước Lời giải chi tiết :
Polime điều chế bằng phản ứng trùng ngưng là poli(etylen terephtalat) Vì nC6H4(COOH)2 + nC2H4(OH)2 → -(O – CH2 –CH2 – O – CO – C6H4 – CO-)-n + 2nH2O
Câu 11 :
Hỗn hợp X gồm Al và Fe có tỉ lệ số mol tương ứng là 1:1. Cho 2,49 gam X vào dung dịch chứa 0,17 mol HCl, thu được dung dịch Y. Cho 200 ml dung dịch AgNO3 1M vào Y, thu được khí NO và m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn, NO là sản phẩm khử duy nhất của N+5. Giá trị của m gần nhất với giá trị nào sau đây
Đáp án : D Phương pháp giải :
X + 0,17 mol HCl thì 2 Al + 6HCl → 2AlCl3 + 3H2 Fe + 2HCl → FeCl2 + H2 → Dung dịch Y thu được có AlCl3 : ? mol ; FeCl2 : ? mol; HCl : ? mol Y + 0,2 mol AgNO3 thì : 3Fe2+ + 4H+ + NO3- → 3Fe3+ + 2H2O + NO Fe2+ + Ag+ → Fe3+ + Ag Ag+ + Cl- → AgCl Lời giải chi tiết :
Đặt số mol Al và Fe trong X là x mol thì mX = 27x + 56x = 2,49 → x = 0,03 mol X + 0,17 mol HCl thì 2 Al + 6HCl → 2AlCl3 + 3H2 Fe + 2HCl → FeCl2 + H2 → Dung dịch Y thu được có AlCl3 : 0,03 mol ; FeCl2 : 0,03 mol; HCl : 0,02 mol Y + 0,2 mol AgNO3 thì : 3Fe2+ + 4H+ + NO3- → 3Fe3+ + 2H2O + NO 0,015 mol ← 0,02 mol Fe2+ + Ag+ → Fe3+ + Ag 0,015 mol 0,015 mol Ag+ + Cl- → AgCl 0,17 mol 0,17 mol → mrắn = mAgCl + mAg = 0,17.143,5 + 0,015.108 = 24,395 + 1,62= 26,015 g → gần nhất với 26,0 g
Câu 12 :
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hơp khí X, Cho toàn bộ khí X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Đáp án : A Phương pháp giải :
CO + CuO → Cu + CO2 CO2 + Ca(OH)2 → CaCO3 + H2O => nCaCO3 = nCO = nCuO =? Lời giải chi tiết :
Ta có nCuO = 0,1 mol PTHH : CO + CuO → Cu + CO2 CO2 + Ca(OH)2 → CaCO3 + H2O → nCaCO3 = nCuO = 0,1 mol → mCaCO3 = 0,1 .100 =10 g
Câu 13 :
Cho 7,3 gam lysin và 15 gam glyxin vào dung dịch chứa 0,3 mol KOH, thu được dung dịch Y. Cho Y tác dụng hoàn toàn với HCl dư thu được m gam muối. Giá trị của m là
Đáp án : A Phương pháp giải :
KOH tác dụng với HCl BTKL: mlysin + mgly + mKOH + mHCl = mmuối + mH2O với nHCl = 2nlysin + ngly + nKOH nH2O = nlysin + ngly + nKOH Lời giải chi tiết :
nlysin = 0,05 mol nglyxin = 0,2 mol Khi cho lysin và glyxin phản ứng với KOH rồi đem sản phẩm tác dụng với HCl ta coi như hỗn hợp lysin, glyxin và KOH tác dụng với HCl H2N – [CH2]4 – CH(NH2) – COOH + 2HCl → ClNH3 – [CH2]4 – CH (NH3Cl)–COOH 0,05 0,05 H2N – CH2 – COOH + HCl → H3NCl – CH2 – COOH 0,2 0,2 KOH + HCl → KCl + H2O 0,3 0,3 → mmuối = 0,05.219 + 0,2.111,5 + 0,3.74,5 = 10,95 + 22,3 + 22,35 = 55,6g
Câu 14 :
Hỗn hợp X gồm axit axetic và metyl fomat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M. Giá trị của m là
Đáp án : D Phương pháp giải :
Thấy axit axetic và metyl fomat có cùng phân tử khối là 60 đvC Mặt khác ∑ nhh = ∑ nNaOH => ∑ mhh = 60. ∑ nhh = ? Lời giải chi tiết :
PTHH: HCOOCH3 + NaOH → HCOONa + CH3OH CH3COOH + NaOH → CH3COONa + H2O Ta thấy nC2H4O2 = nNaOH = 0,3 mol → mC2H4O2 =mX = 0,3.60 = 18g
Câu 15 :
Phát biểu nào sau đây là sai:
Đáp án : C Phương pháp giải :
Dựa vào tính chất về crom và hợp chất của crom Lời giải chi tiết :
A đúng B đúng C sai vì CrO3 là oxit axit D đúng
Câu 16 :
Cho các polime: poli(vinyl clorua), xenlulozo, policaproamit, polistiren, xenlulozo trinitrat, nilon – 6,6. Số polime tổng hợp là
Đáp án : B Phương pháp giải :
Polime phân làm 3 loại + polime thiên nhiên: có nguồn gốc hoàn toàn từ thiên nhiên + polime tổng hợp: 100% từ con người tạo ra + polime bán tổng hợp: 1 phần nguồn gốc từ nhiên nhiên, 1 phần nguồn gốc từ con người tổng hợp. Lời giải chi tiết :
Polime tổng hợp là: poli(vinyl clorua), policaproamit, polistiren, nilon – 6,6 Xenlulozo là polime tự nhiên còn xenlulozo trinitrat là polime bán tổng hợp Vậy có tất cả 4 polime tổng hợp trong dãy polime đã cho.
Câu 17 :
Dung dịch nào sau đây tác dụng với dung dịch Ba(HCO3)2 vừa thu được kết tủa, vừa có khí thoát ra
Đáp án : C Phương pháp giải :
Viết PTHH của Ba(HCO3)2 với các chất Lời giải chi tiết :
A. sai vì chỉ tạo khí CO2. 2HCl + Ba(HCO3)2 → BaCl2 + 2CO2↑ + 2H2O B. sai vì chỉ tạo kết tủa BaCO3 2NaOH + Ba(HCO3)2 → BaCO3↓ + Na2CO3 + 2H2O C. đúng vì Ba(HCO3)2 + H2SO4 → BaSO4↓ + 2H2O + 2CO2↑ D. sai vì chỉ có kết tủa là CaCO3 và BaCO3 Ca(OH)2 + Ba(HCO3)2 → BaCO3↓ + CaCO3↓ + 2H2O
Câu 18 :
Khi thủy phân tinh bột thu được sản phẩm cuối cùng là
Đáp án : A Phương pháp giải :
Xem lại TCHH của tinh bột Lời giải chi tiết :
Khi thủy phân tinh bột thu được sản phẩm cuối cùng là glucozo
Câu 19 :
Cho hỗn hợp gồm Zn, Mg và Ag vào dung dịch CuCl2, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp gồm 3 kim loại. Ba kim loại đó là:
Đáp án : A Phương pháp giải :
Viết PTHH theo thứ tự kim loại mạnh phản ứng với dd CuCl2 trước Lời giải chi tiết :
Khi cho hỗn hợp trên vào CuCl2 thì phản ứng theo thứ tự : Mg + CuCl2 → MgCl2 + Cu Zn + CuCl2 → ZnCl2 + Cu → rắn thu được có 3 kim loại nên 3 kim loại này là Ag, Cu, Zn dư
Câu 20 :
Cho từ từ đến dư dung dịch KOH vào dung dịch hỗn hợp x mol HNO3 và y mol Al(NO3)3, kết quả thí nghiệm được biểu diễn trên đồ thị sau Tỉ lệ của b : a có giá trị là
Đáp án : D Phương pháp giải :
Thứ tự xảy ra phản ứng KOH + HNO3 → KNO3 + H2O 3KOH + Al(NO3)3 → 3KNO3 + Al(OH)3 KOH + Al(OH)3 → KAlO2 + 2H2O Xét số mol KOH tại các thời điểm Lời giải chi tiết :
KOH + HNO3 → KNO3 + H2O 3KOH + Al(NO3)3 → 3KNO3 + Al(OH)3 KOH + Al(OH)3 → KAlO2 + 2H2O Xét tại các thời điểm +) có 0,56 mol KOH thì chỉ xảy ra 2 phản ứng đầu → nKOH = nHNO3 + 3nAl(OH)3 = x + 3a = 0,56 mol +) có 1,04 mol KOH thì chỉ có 2 phản ứng đầu xảy ra → nKOH = nHNO3 + 3nAl(OH)3 = x + 3(a + 0,8x ) =1,04 → x = 0,2 mol và a = 0,12 mol +) tại thời điểm b mol KOH thì xảy ra cả 3 phản ứng và thu được nAl(OH)3 = a + 0,8x = 0,28 mol → nKOH = nHNO3 + 3nAl(NO3)3 + nAl(OH)3 bị hòa tan = x + 3y + (y – 0,28) =0,2 + 4y – 0,28 = 4y – 0,08 (mol) = b(1) +) tại thời điểm (7x + 0,08) mol KOH hay 1,48 mol KOH thì nAl(OH)3 = 0,12 mol và cả 3 phản ứng xảy ra → nKOH = nHNO3 + 3nAl(NO3)3 + nAl(OH)3 bị hòa tan = x + 3y + (y – 0,12) = 4y + 0,08 = 1,48 → y = 0,35 (2) Từ (1) và (2) suy ra b = 1,32 mol → b : a = 1,32 : 0,12 = 11
Câu 21 :
Cho 11,9 gam hỗn hợp Zn và Al phản ứng vừa đủ với dung dịch H2SO4 loãng thu được m gam muối trung hòa và 8,96 lít khí H2 đktc. Giá trị của m là
Đáp án : C Phương pháp giải :
Kim loại + H2SO4 → muối + H2 Bảo toàn nguyên tố H ; Bảo toàn khối lượng Lời giải chi tiết :
Ta có kim loại + H2SO4 → muối + H2 nH2 = 0,4 mol Bảo toàn nguyên tố H có nH2 = nH2SO4 = 0,4 mol Bảo toàn khối lượng có mkim loại + mH2SO4 = mH2 + mmuối → 11,9 + 0,4.98 = 0,4.2 + m → m = 50,3
Câu 22 :
Một số loại khẩu trang y tế chứa hoạt chất bột màu đen có khả năng lọc không khí. Chất đó là
Đáp án : C Phương pháp giải :
Dựa vào kiến thức ứng dụng của cacbon Lời giải chi tiết :
Than hoạt tính là chất thường được sử dụng trong khẩu trang y tế do khả năng hấp phụ tốt nên có thể lọc không khí
Câu 23 :
Đốt cháy hoàn toàn amin X no, đơn chức, mạch hở, thu được 0,2 mol CO2 và 0,05 mol N2. Công thức phân tử của X là
Đáp án : A Phương pháp giải :
CTPT của X là CnH2n+3N Bảo toàn N => namin X = 2nN2 = ? => n = nCO2/ namin = ? Từ đó tìm được CTPT của X Lời giải chi tiết :
Vì X là amin đơn chức nên nX = 2nN2 = 2.0,05 = 0,1 mol X là amin no đơn chức mạch hở nên X có CTPT là CnH2n+3N : 0,1 mol → n = nCO2 : nX = 0,2 : 0,1 = 2 → X là C2H7N
Câu 24 :
Thực hiện các thí nghiệm sau (a) Sục khí CO2 dư vào dung dịch BaCl2 (b) Cho dung dịch NH3 dư vào dung dịch AlCl3 (c) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 (d) Cho hỗn hợp Na2O và Al2O3 (tỉ lệ mol 1:1) vào nước dư (e) Cho dung dịch Ba(OH)2 dư vào dung dịch Cr2(SO4)3 (f) Cho hỗn hợp bột Cu và Fe3O4 (tỉ lệ mol 1:1) vào dung dịch HCl dư Sau khi các phản ứng xảy ra, số thí nghiệm thu được kết tủa là
Đáp án : D Phương pháp giải :
Viết PTHH xảy ra, chọn các thí nghiệm thu được kết tủa Lời giải chi tiết :
(a) Phản ứng không xảy ra (b) Phản ứng tạo kết tủa Al(OH)3 do 3NH3 + AlCl3 +H2O → 3NH4Cl + Al(OH)3 (c) Phản ứng tạo kết tủa là Ag do Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag (d) Phản ứng không tạo kết tủa do : Na2O + H2O → 2NaOH và Al2O3 +2NaOH → 2NaAlO2 + H2O (e) Phản ứng tạo kết tủa : 4Ba(OH)2 + Cr2(SO4)3 → 3BaSO4 + Ba(CrO2)2 + 4H2O (f) Phản ứng không tạo kết tủa do : Fe3O4 + 8HCl → 2FeCl3 + FeCl2 +4H2O; 2FeCl3 + Cu → 2FeCl2 + CuCl2 Số thí nghiệm thu được kết tủa là 3
Câu 25 :
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 3,26 mol O2, thu được 2,28 mol CO2 và 39,6 gam nước. Mặt khác thủy phân hoàn toàn a gam X trong dung dịch NaOH đun nóng, thu được dung dịch chứa b gam muối. Giá trị của b là
Đáp án : B Phương pháp giải :
a g X + 3,26 mol O2 → 2,28 mol CO2 + 39,6 gam nước Bảo toàn khối lượng → a Bảo toàn nguyên tố O → nX X + 3NaOH → muối + C3H5(OH)3 Bảo toàn khối lượng → mmuối Lời giải chi tiết :
Ta có a g X + 3,26 mol O2 → 2,28 mol CO2 + 39,6 gam nước Bảo toàn khối lượng có a + 3,26.32 = 2,28.44 + 39,6 → a = 35,6 gam Bảo toàn nguyên tố O có nO(X) + 2nO2 = 2nCO2 + nH2O → nO(X) + 2.3,26 = 2.2,28 + 2,2 → nO(X) = 0,24 mol Vì X là triglixerit nên X chứa 6 O trong công thức phân tử nên nX = 0,04 mol Ta có a gam X + 3NaOH → muối + C3H5(OH)3 Ta có nNaOH = 3nX = 3.0,04 =0,12 mol nC3H5(OH)3 = 0,04 mol Bảo toàn khối lượng có mX + mNaOH =mmuối + mC3H5(OH)3 → 35,6 + 0,12.40 = 0,04.92 + mmuối → mmuối = 36,72 g
Câu 26 :
Công thức nào sau đây có thể là công thức của chất béo
Đáp án : D Phương pháp giải :
Chất béo là Trieste của axit béo và glixerol Trong đó các axit béo là các axit đơn chức mạch hở và có từ 12 C trở lên Lời giải chi tiết :
Công thức của chất béo (C17H33COO)3C3H5
Câu 27 :
Cho m gam bột Fe vào dung dịch X chứa 0,1 mol Fe(NO3)3 và 0,4 mol Cu(NO3)2. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch Y và m gam chất rắn Z. Giá trị của m là
Đáp án : D Phương pháp giải :
PTHH : Fe + 2Fe(NO3)3 → 3Fe(NO3)2 Fe + Cu(NO3n ứng + mCu → nFe phản ứng)2 → Fe(NO3)2 + Cu mrắn Z = m – mFe phả Lời giải chi tiết :
PTHH : Fe + 2Fe(NO3)3 → 3Fe(NO3)2 Fe + Cu(NO3)2 → Fe(NO3)2 + Cu Vì khối lượng rắn không đổi sau phản ứng nên xảy ra cả 2 phản ứng Đặt nCu tạo thành = x mol Ta có mrắn Z = m – mFe phản ứng + mCu = m – 56.(0,05 + x) + 64x = m → x = 0,35 mol → phản ứng dư Cu(NO3)2 → Fe phản ứng hết → m = 56.(0,35 + 0,05) = 22,4 g
Câu 28 :
Cho dung dịch NaOH vào dung dịch X, thu được kết tủa màu nâu đỏ. Chất X là
Đáp án : C Phương pháp giải :
Viết PTHH và nhận định màu kết tủa Cu(OH)2: màu xanh; Fe(OH)3: nâu đỏ Fe(OH)2 và Mg(OH)2 : màu trắng Lời giải chi tiết :
X là FeCl3 vì FeCl3 + 3NaOH → 3NaCl + Fe(OH)3 là kết tủa màu nâu đỏ
Câu 29 :
Este nào sau đây thủy phân trong môi trường axit thu được 2 chất hữu cơ đều tham gia phản ứng tráng gương?
Đáp án : A Phương pháp giải :
Este thủy phân trong môi trường axit thu được 2 chất hữu cơ đều tham gia phản ứng tráng gương → este tạo từ HCOOH và thủy phân tạo ra cả andehit Lời giải chi tiết :
A đúng vì thủy phân tạo ra HCOOH và CH3CHO đều có khả năng tráng bạc B sai vì tạo ra CH3COOH và C6H5OH đều không có khả năng tráng bạc C sai vì tạo ra CH3COOH và C2H5OH đều không có khả năng tráng bạc D sai vì tạo ra CH3COOH không có khả năng tráng bạc
Câu 30 :
Khi thủy phân hoàn toàn a gam saccarozo trong môi trường axit thu được 81 gam hỗn hợp glucozo và fructozo. Giá trị của a là
Đáp án : D Phương pháp giải :
Viết PTHH → tính Lời giải chi tiết :
Ta có C12H22O11 + H2O → C6H12O6(glucozo) + C6H12O6( fructozo) Ta có nglucozo = nfructozo = 81 : 2 : 180 = 0,225 mol → nsaccarozo = 0,225 mol → a = 0,225. 342= 76,95 g
Câu 31 :
Cho dãy các chất sau : glucozo, xenlulozo, saccarozo, tinh bột, fructozo. Số chất trong dãy tham gia phản ứng tráng bạc là
Đáp án : B Phương pháp giải :
Xem lại TCHH của tinh bột, glucozo, xenlulozo. Chất tham gia được phản ứng tráng bạc là chất có cấu tạo nhóm -CHO trong phân tử hoặc trong dd AgNO3/NH3 chuyển hóa thành chất có phản ứng tráng bạc. Lời giải chi tiết :
Chất trong dãy tham gia phản ứng tráng bạc là: glucozo,fructozo
Câu 32 :
Dung dịch hỗn hợp X gồm NaCl 0,6M và CuSO40,5M. Điện phân 100 ml dung dịch X (điện cực trơ, màng ngăn xốp, hiệu suất 100%, bỏ qua sự hòa tan của khí trong nước hay sự bay hơi của nước) với cường độ dòng điện không đổi 0,5A trong thời gian t giây. Dung dịch sau điện phân có khối lượng giảm 4,85 gam so với dung dịch ban đầu. Giá trị của t là
Đáp án : B Phương pháp giải :
Ban đầu dung dịch X chứa nNaCl = 0,06 mol và nCuSO4 = 0,05 mol Tại A : 2Cl- → Cl2 + 2e Tại K thì Cu+2 +2e → Cu Tại thời điểm Cl- hết mdd giảm = mCl2 + mCu = 0,03.71 + 0,03.64 = 4,05 g < 4,85 nên tại A xảy ra điện phân nước Tại thời điểm Cu2+ bị điện phân hết thì mdd giảm = mCl2 + mCu + mO2 = 0,03.71 + 0,05.64 + mO2 = 5,33 + mO2 > 4,85 Nên Cu2+ chưa điện phân hết Đặt nO2 = x mol thì theo bảo toàn e có nCu(2+) => lập phương trình mdd giảm tìm x Lời giải chi tiết :
Ban đầu dung dịch X chứa nNaCl = 0,06 mol và nCuSO4 = 0,05 mol Tại A : 2Cl- → Cl2 + 2e Tại K thì Cu+2 +2e → Cu Vì nCl < 2nCu nên điện phân thì Cl- hết trước Tại thời điểm Cl- hết thì nCu = nCl : 2 = 0,06 : 2 =0,03 mol Khi đó mdd giảm = mCl2 + mCu = 0,03.71 + 0,03.64 = 4,05 g < 4,85 g nên tại A xảy ra điện phân nước \(2{H_2}O \to 4{H^ + } + {O_2} + 4e\) Tại thời điểm Cu2+ bị điện phân hết thì mdd giảm = mCl2 + mCu + mO2 = 0,03.71 + 0,05.64 + mO2 = 5,33 + mO2 > 4,85 Nên Cu2+ chưa điện phân hết Đặt nO2 = x mol thì theo bảo toàn e có nCu(2+) = (nCl- + 4nO2) : 2 = (0,06 + 4x) : 2 =0,03 + 2x (mol) Khối lượng dung dịch sau điện phân giảm là mdd giảm = mCu + mCl2 + mO2 = (0,03 + 2x).64 + 0,03.71 + 32x = 4,85 => x = 0,005 mol => nCu = 0,03 + 0,005.2 = 0,04 mol => ne trao đổi = 2nCu = \(\dfrac{{I.t}}{F} = \dfrac{{0,5.t}}{{96500}}\) = 2.0,04 =0,08 nên t = 15440 (s)
Câu 33 :
Hỗn hợp X gồm 2 este đơn chức. Cho 0,3 mol X tác dụng vừa đủ với 250 ml dung dịch KOH 2M, thu được chất hữu cơ Y (no, đơn chức, mạch hở, có tham gia phản ứng tráng bạc) và 53 gam hỗn hợp muối. Đốt cháy hoàn toàn Y cần dùng vừa đủ 5,6 lít khí O2 đktc. Khối lượng của 0,3 mol X là
Đáp án : B Phương pháp giải :
Vì X là 2 este đơn chức nhưng X tác dụng với KOH theo tỉ lệ khác 1 :1 nên X có chứa 1 este là este của phenol Gọi A là este đơn chức thông thường còn B là este của phenol => số mol của từng loại este X + KOH tạo Y no đơn chức mạch hở có khả năng tráng bạc nên Y là andehit => nY theo số mol este vừa tìm được => anđehit Y Bảo toàn khối lượng tìm mX Lời giải chi tiết :
nKOH =0,5 mol Vì X là 2 este đơn chức nhưng X tác dụng với KOH theo tỉ lệ khác 1 :1 nên X có chứa 1 este là este của phenol Gọi A là este đơn chức thông thường còn B là este của phenol Thì nA + nB = nX = 0,3 mol nKOH = nA + 2nB = 0,5 mol nên nA = 0,1 mol và nB =0,2 mol X + KOH tạo Y no đơn chức mạch hở có khả năng tráng bạc nên Y là andehit (Y không phải muối nên không thể là muối của HCOOH) và Y được tạo từ A : nY = nA = 0,1 mol Xét Y có CTPT là CnH2nO \({C_n}{H_{2n}}O\; + {\text{ }}\frac{{3n - 1}}{2}{O_2}\xrightarrow{{{t^o}}}n\;C{O_2} + n{H_2}O\) Suy ra :\(0,1.\frac{{3n - 1}}{2} = {n_{{O_2}}} = 0,25 \to n = 2\) (C2H4O : 0,1 mol) Khi cho X + KOH thì : A + 0,1 mol KOH → muối + 0,1 mol C2H4O B + 0,4 mol KOH → muối + 0,2 mol H2O ( vì B là este của phenol nên nH2O = nB) Bảo toàn khối lượng có mX + mKOH = mmuối + mC2H4O + mH2O nên mX + 0,5.56 = 53 + 0,1.44+0,2.18 => mX = 33 (g)
Câu 34 :
Hòa tan hoàn toàn hỗn hợp K và Na vào nước, thu được dung dịch X và V lít khí H2 đktc. Trung hòa X cần 200 ml dung dịch H2SO4 0,1M. Giá trị của V là
Đáp án : A Phương pháp giải :
Tính theo PTHH K + H2O → KOH + ½ H2 Na + H2O → NaOH + ½ H2 OH- + H+ → H2O Lời giải chi tiết :
Ta có K + H2O → KOH + ½ H2 Na + H2O → NaOH + ½ H2 OH- + H+ → H2O nH2SO4 = 0,02 mol nên nH+ = 0,04 mol → nOH- = 0,04 mol theo PTHH thì nOH = 2nH2 => nH2 = 0,02 mol => V = 0,02.22,4 =0,448 lít
Câu 35 :
Tiến hành các thí nghiệm sau (a) Nhúng thanh đồng nguyên chất vào dung dich FeCl3 (b) Cắt nguyên miếng sắt tây ( sắt tráng thiếc), để trong không khí ẩm (c) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịch CuSO4 (d) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc nước muối Trong các thí nghiệm trên số thí nghiệm chỉ xảy ra ăn mòn điện hóa là
Đáp án : D Phương pháp giải :
Ăn mòn điện hóa xảy ra khi: + Xuất hiện 2 cặp kim loại có bản chất khác nhau + Các chất tiếp xúc trực tiếp hoặc gián tiếp với nhau thông qua dây dẫn + Các chất cùng nhúng trong 1 dung dịch chất điện li Lời giải chi tiết :
(a) không xảy ra ăn mòn điện hóa chỉ xảy ra ăn mòn hóa học (b) Xảy ra ăn mòn điện hóa học (c) xảy ra ăn mòn hóa học trước tạo Cu rồi mới có ăn mòn điện hóa (d) ăn mòn điện hóa học
Câu 36 :
Cho a mol este X(C9H10O2) tác dụng vừa đủ với 2a mol NaOH, thu được dung dịch không có phản ứng tráng bạc. Số công thức cấu tạo của X là
Đáp án : B Phương pháp giải :
X tác dụng với NaOH theo tỉ lệ 1 : 2 nên X là este của phenol Sản phẩm thu được không có khả năng tráng bạc nên X không tạo từ HCOOH Lời giải chi tiết :
X tác dụng với NaOH theo tỉ lệ 1 : 2 nên X là este của phenol Sản phẩm thu được khôn có khả năng tráng bạc nên X không tạo từ HCOOH Các CTHH thỏa mãn X : CH3COOC6H4-CH3 (3 CTCT tại vị trí m, o, p) và C2H5COOC6H5 => có 4 CTCT thỏa mãn
Câu 37 :
Cho sơ đồ chuyển hóa Glucozo → X → Y → CH3COOH. Hai chất X, Y là
Đáp án : A Phương pháp giải :
Xem lại bài glucozo Viết PTHH Lời giải chi tiết :
\(Glucozo\xrightarrow{{(1)}}\underbrace {{C_2}{H_5}OH}_X\xrightarrow{{(2)}}\underbrace {C{H_3}CHO}_Y\xrightarrow{{(3)}}C{H_3}COOH\) \(\begin{gathered}(1){C_6}{H_{12}}{O_6}\xrightarrow{{lên\,men\,rượu}}2{C_2}{H_5}OH + 2C{O_2} \\(2){C_2}{H_5}OH + CuO\xrightarrow{{{t^0}}}C{H_3}CHO + Cu + {H_2}O \\(3)C{H_3}CHO + \frac{1}{2}{O_2}\xrightarrow{{M{n^{2 + }}}}C{H_3}COOH \\\end{gathered} \)
Câu 38 :
Trong công nghiệp, kim loại nào sau đây chỉ được điều chế bằng phương pháp điện phân nóng chảy?
Đáp án : B Phương pháp giải :
Kim loại có tính khử mạnh thường sẽ được điều chế bằng điện phân nóng chảy như Na, K, Li ... Lời giải chi tiết :
Trong công nghiệp, kim loại được điều chế bằng phương pháp điện phân nóng chảy Mg
Câu 39 :
Hợp chất nào sau đây có tính lưỡng tính
Đáp án : D Phương pháp giải :
Chất có tính lưỡng tính là chất tác dụng với cả axit và bazo Lời giải chi tiết :
Hợp chất nào sau đây có tính lưỡng tính Cr(OH)3 – hidroxit lưỡng tính A sai vì NaOH không tác dụng với bazo B sai vì CrCl3 không tác dụng với axit C sai vì KOH không tác dụng với bazo
Câu 40 :
Cho V ml dung dịch NaOH 2M vào 200 ml dung dịch AlCl3 1M, sau khi phản ứng xảy ra hoàn toàn thu được 3,9 gam kết tủa. Giá trị lớn nhất của V là
Đáp án : C Phương pháp giải :
3NaOH + AlCl3 → 3NaCl + Al(OH)3 Al(OH)3 + NaOH → NaAlO2 + 2H2O Vì nAl(OH)3 < nAlCl3 nên xảy ra 2 trường hợp : kết tủa chưa tạo thành tối đa hoặc kết tủa tối đa rồi tan một phần Để NaOH lớn nhất thì kết tủa tạo thành tối đa rồi tan một phần Lời giải chi tiết :
3NaOH + AlCl3 → 3NaCl + Al(OH)3 Al(OH)3 + NaOH → NaAlO2 + 2H2O nAlCl3 = 0,2 mol và nAl(OH)3 = 0,05 mol Vì nAl(OH)3 < nAlCl3 nên xảy ra 2 trường hợp : kết tủa chưa tạo thành tối đa hoặc kết tủa tối đa rồi tan một phần Để NaOH lớn nhất thì kết tủa tạo thành tối đa rồi tan một phần => nNaOH = 3nAlCl3 + nAl(OH)3 bị hòa tan = 3.0,2 + (0,2 – 0,05 ) = 0,75 mol => V = 0,75 : 2 =0,375 lít = 375 ml |