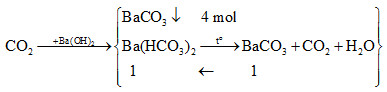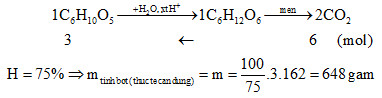30 bài tập về lên men tinh bột, quá trình quang hợp có lời giảiLàm bàiCâu hỏi 1 : Cho m gam tinh bột lên men để sản xuất ancol etylic, toàn bộ lượng CO2 sinh ra cho qua dung dịch Ca(OH)2 dư thu được 750 gam kết tủa. Biết hiệu suất mỗi giai đoạn là 80%. Giá trị của m là
Đáp án: B Phương pháp giải: Để đơn giản ta coi tinh bột là C6H10O5 + Viết sơ đồ: C6H10O5 → C6H12O6 → 2CO2 + nC6H10O5 = ½ nCO2 = ½ nCaCO3 + mThực tế = (mlý thuyết : %H ).100% Với %H = %H1.%H2 Lời giải chi tiết: Để đơn giản ta coi tinh bột là C6H10O5 Các giai đoạn của quá trình: C6H10O5 → C6H12O6→ 2CO2 Từ sơ đồ: nC6H10O5 = ½ nCO2 = ½ nCaCO3 = 3,75 mol mC6H10O5 lý thuyết = 3,75.162 = 607,5 gam Tuy nhiên do hiệu suất chỉ là 80% nên thực tế cần phải dùng lượng nhiều hơn => mC6H10O5 thực tế = mC6H10O5 lý thuyết.(100/80).(100/80) = 607,5.(100/80)2 = 949,2 gam Đáp án B Câu hỏi 2 : Phản ứng tổng hợp glucozo trong cây xanh cần được cung cấp năng lượng 2813 kJ cho mỗi mol glucozo tạo thành: 6CO2 + 6H2O \(\overset{a/s,clorophin}{\rightarrow}\) C6H12O6 + O2 Nếu trong 1 phút mỗi cm2 lá xanh nhận được khoảng 2,09 J năng lượng từ mặt trời nhưng chỉ có 10% được sử dụng vào phản ứng tổng hợp glucozo. Với 1 ngày nắng (từ 6h - 17h) diện tích lá xanh là 1 m2, lượng glucozo tổng hợp được là bao nhiêu?
Đáp án: B Phương pháp giải: Lời giải chi tiết: - Thời gian chiếu sáng trong 1 ngày là: 17 - 6 = 11 (giờ) = 660 phút - Năng lượng mặt trời 1 cm2 lá xanh nhận được từ mặt trời là: 2,09.660 = 1379,4 (J) - Năng lượng mặt trời 1 m2 = 104 cm2 lá xanh nhận được từ mặt trời là: 1379,4.104 = 13794 (kJ) - Năng lượng sử dụng cho phản ứng tổng hợp glucozo là: 13794.10% = 1379,4 (kJ) - Số mol glucozo tổng hợp được là: 1379,4 : 2813 = 0,490366 mol - Khối lượng glucozo tổng hợp được là: 0,49.180 = 88,2659 gam ≈ 88,3 gam Đáp án B Câu hỏi 3 : Cho m gam tinh bột lên men thành ancol etylic với hiệu suất 81%. Toàn bộ lượng CO2 sinh ra được hấp thụ hoàn toàn vào dung dịch Ca(OH)2, thu được 550 gam kết tủa và dung dịch X. Đun kĩ dung dịch X thu thêm được 100 gam kết tủa. Giá trị của m là
Đáp án: C Phương pháp giải: Do đun dung dịch X thu thêm được kết tủa nên dd X có chứa Ca(HCO3)2. - Sơ đồ lên men tinh bột thành CO2: C6H10O5 → C6H12O6 → 2CO2 - Sục CO2 vào dd Ca(OH)2: CO2 + Ca(OH)2 → CaCO3 + H2O 2CO2 + Ca(OH)2 → Ca(HCO3)2 Ca(HCO3)2 → CaCO3 + CO2 + H2O Đặt số mol kết tủa lần và lần 2 vào PTHH ta xác định được số mol CO2 Theo (1) => nC6H10O5 = 0,5nCO2 => mC6H10O5 Do hiệu suất lên men là 81% nên lượng tinh bột cần dùng lớn hơn lượng tính toán => m C6H10O5 cần dùng Lời giải chi tiết: nCaCO3 (lần 1) = 5,5 mol; nCaCO3 (lần 2) = 1 mol Do đun dung dịch X thu thêm được kết tủa nên dd X có chứa Ca(HCO3)2. - Sơ đồ lên men tinh bột thành CO2: C6H10O5 → C6H12O6 → 2CO2 - Sục CO2 vào dd Ca(OH)2: CO2 + Ca(OH)2 → CaCO3 + H2O 5,5 ← 5,5 2CO2 + Ca(OH)2 → Ca(HCO3)2 2 ← 1 Ca(HCO3)2 → CaCO3 + CO2 + H2O 1 ← 1 => nCO2 = 5,5 + 2 = 7,5 mol Theo (1) => nC6H10O5 = 0,5nCO2 = 3,75 mol => mC6H10O5 = 3,75.162 = 607,5 gam Do hiệu suất lên men là 81% nên lượng tinh bột cần dùng lớn hơn lượng tính toán => m C6H10O5 cần dùng = 607,5.(100/81) = 750 gam Câu hỏi 4 : Từ 81 gam tinh bột, bằng phương pháp lên men rượu, thu được a gam etanol với hiệu suất 80%. Oxi hóa hoàn toàn 0,1a gam etanol bằng phương pháp lên men giấm với hiệu suất h% thu được hỗn hợp X. Để trung hòa X cần vừa đủ 60 ml dung dịch NaOH 1M, giá trị của h là
Đáp án: B Phương pháp giải: - Phản ứng thủy phân tinh bột (H = 80%): Để đơn giản ta coi tinh bột là C6H10O5 Tính được: nC6H10O5 pư = nC6H10O5 bđ.80% PTHH: C6H10O5 → 2 C2H5OH + 2CO2 => nC2H5OH = 2nC6H10O5 pư - Oxi hóa 0,1a gam C2H5OH (hiệu suất H% = h): C2H5OH + O2 \(\overset{men\,giam}{\rightarrow}\) CH3COOH + H2O CH3COOH + NaOH → CH3COONa + H2O => nC2H5OH pư = nCH3COOH = nNaOH => h Lời giải chi tiết: - Phản ứng thủy phân tinh bột (H = 80%): Để đơn giản ta coi tinh bột là C6H10O5 nC6H10O5 = 81/162 = 0,5 mol => nC6H10O5 pư = 0,5.80% = 0,4 mol PTHH: C6H10O5 → 2 C2H5OH + 2CO2 => nC2H5OH = 2nC6H10O5 = 0,8 mol - Oxi hóa 0,1a gam (0,08 mol) C2H5OH (hiệu suất H% = h): C2H5OH + O2 \(\overset{men\,giam}{\rightarrow}\) CH3COOH + H2O CH3COOH + NaOH → CH3COONa + H2O nC2H5OH pư = nCH3COOH = nNaOH = 0,06 mol => h = \(\frac{{0,06}}{{0,08}}.100\% \) = 75% Đáp án B Câu hỏi 5 : Cho m gam tinh bột lên men thành ancol etylic với hiệu suất 81%. Toàn bộ lượng CO2 hấp thụ vào dung dịch nước vôi trong thu được 275g kết tủa và dung dịch Y. Đun kĩ dung dịch Y thu thêm 150g kết tủa nữa. Khối lượng m là?
Đáp án: D Phương pháp giải: + Bảo toàn nguyên tố Cacbon: nCO2 = nCaCO3 + 2nCa(HCO3)2 = nCaCO3 ↓(1) + 2nCaCO3↓ (2) Lời giải chi tiết: Ta có \(\sum {nCO_{_3}^{2 - }} = 1,5.2 + 2,75 = 5,75mol\) \( \to {m_{{\text{tinh bot}}}} = \frac{{5,75}}{2}.\frac{1}{{81\% }}.162 = 575gam\) Vậy khối lượng tinh bột là 575 gam Đáp án D Câu hỏi 6 : Cho m gam tinh bột lên men để sản xuất ancol etylic, toàn bộ lượng CO2 sinh ra cho qua dung dịch Ca(OH)2 dư, thu được 750 gam kết tủa. Biết hiệu suất toàn bộ quá trình là 64%. Giá trị của m là:
Đáp án: A Phương pháp giải: phản ứng thủy phân xenlulozơ hoặc tinh bột (C6H10O5)n H1% H2% (C6H10O5)n -> nC6H12O6 -> 2nCO2 + 2nC2H5OH 162n 180n 88n 92n Lưu ý: 1) A -> B ( Hlà hiệu suất phản ứng)
nB = nA. H%
2) A -> B -> C ( H1, H2 là hiệu suất phản ứng A -> B và B -> C)
nC = nB. H2% = nA . H1%. H2%
Lời giải chi tiết: C6H10O5 -> C6H12O6 -> 2CO2 -> 2CaCO3 n. 64% -> 1,28n = 7,5 Mol => n = 0,5859 mol => m = 949,2g Đáp án A Câu hỏi 7 : Lên men m gam tinh bột (Hiệu suất toàn bộ quá trình là 80%). Lượng CO2 hấp thụ vào dung dịch NaOH thu được dung dịch X. Chia X thành 2 phần bằng nhau: - Phần 1: :Cho tác dụng với dd CaCl2 dư thu được 7,5 gam kết tủa - Phần 2: Cho tác dụng với dung dịch CaCl2 dư đun nóng thu được 8,5 gam kết tủa Giá trị m là:
Đáp án: D Phương pháp giải: Tính toán theo PTHH Lời giải chi tiết: P1: nCO3 2-=nCaCO3=0,075 mol P2: CaCl2 + Na2CO3 → CaCO3+2NaCl 0,075 ← 0,075 Ca(HCO3)2 → CaCO3 + H2O + CO2 0,01← 0,01 BTNT C: nCO2 (1 phần)=nCO32-+nHCO3-=0,075+0,01.2=0,095 mol=>nCO2 (2P)=0,19 mol n tinh bột=0,5nCO2=0,095 mol m=0,095.162.100/80=19,2375 gam Đáp án D Câu hỏi 8 : Ancol etylic được điều chế từ tinh bột bằng phương pháp lên men với hiệu suất toàn bộ quá trình là 90%. Hấp thụ toàn bộ lượng CO2 sinh ra khi lên men m gam tinh bột vào nước vôi trong thu được 165 gam kết tủa và dung dịch X. Biết khối lượng dung dịch X giảm đi 66,0 gam so với khối lượng nước vôi trong ban đầu. Giá trị của m là
Đáp án: B Phương pháp giải: + m dd giảm=m kết tủa – mCO2=>mCO2 + Tinh bột → 2CO2 + Công thức hiệu suất Lời giải chi tiết: m dd giảm=m kết tủa – mCO2=>mCO2=m kết tủa-m dd giảm=165-66=99 gam => nCO2=99/44=2,25 mol Tinh bột → 2CO2 1,125 ← 2,25 mol m=1,125.162.100/90=202,5 gam Đáp án B Câu hỏi 9 : Từ 16,2 kg gạo có chứa 81% tinh bột có thể sản xuất được V lít ancol etylic 230, biết hiệu suất của cả quá trình lên men đạt 75%, khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml. Giá trị của V là
Đáp án: A Phương pháp giải: Lời giải chi tiết: Khối lượng tinh bột là: mtinh bột=16,2.81/100=13,122 (g). \({({C_6}{H_{10}}{O_5})_n} \to n{C_6}{H_{12}}{O_6} \to 2n{C_2}{H_5}OH\) Theo sơ đồ trên số mol rượu theo lí thuyết điều chế được là: \({n_{{C_2}{H_{10}}{O_5}(LT)}} = \frac{{13,122}}{{162}}.2 = 0,162(kmol) \to {n_{{C_2}{H_{10}}{O_5}(TT)}} = 0,162.\frac{{75}}{{100}} = 0,1215(kmol)\) Thể tích của rượu nguyên chất là:\({V_{{C_2}{H_5}OH}} = \frac{m}{d} = \frac{{0,1215.46}}{{0,8}} = 6,98625(l).\) Thể tích rượu 23o thu được là: \(6,9825.\frac{{100}}{{23}} = 30,375(l).\) Đáp án A. Câu hỏi 10 : Lên men m gam tinh bột thành ancol etylic với hiệu suất 81%, hấp thụ toàn bộ khí CO2 sinh ra vào dung dịch chứa 0,05 mol Ba(OH)2, thu được kết tủa và dung dịch X. Cho từ từ dung dịch NaOH vào X, đến khi kết tủa lớn nhất thì cần ít nhất 10 ml dung dịch NaOH 1M. Giá trị của m là
Đáp án: A Phương pháp giải: + Bảo toàn nguyên tố + Công thức tính hiệu suất:\(\% H = \frac{{{m_{thucte}}}}{{m{\,_{li\,thuyet}}}}.100\% \)với lượng tin bột cần lấy là lượng lí thuyết. Lời giải chi tiết: (C6H10O5)n + nH2O → 2nC2H5OH + 2nCO2 \(C{O_2} + 0,05mol\,Ba{(OH)_2}\xrightarrow{{}}\left\langle \begin{gathered} Vì NaOH tối thiểu cho vào Ba(HCO3)2 để thu được kết tủa cực đại nên phản ứng xảy ra theo tỉ lệ 1:1 NaOH + Ba(HCO3)2 → BaCO3↓ + NaHCO3 + H2O 0,01 → 0,01 BTNT Ba: => nBaCO3 (1) = nBa(OH)2 – nBa(HCO3)2 = 0,05 – 0,01 = 0,04 (mol) BTNT C: nCO2 = nBaCO3 (1) + 2nBa(HCO3)2 = 0,04 + 2.0,01 = 0,06 (mol) ntinh bột = 1/2 nCO2 = 0,03 (mol) mtinh bột cần lấy = mtinh bột thực tế : %H = 0,03. 162 : 0,81 = 6 (gam) Đáp án A Câu hỏi 11 : Từ 20kg gạo nếp chứa 81% tinh bột, khi lên men thu được bao nhiêu lít ancol 960? Biết hiệu suất của quá trình lên men đạt 81% và ancol etylic có khối lượng riêng D=0,789mg/l.
Đáp án: A Phương pháp giải: + Viết sơ đồ điều chế: (C6H10O5)n → nC6H12O6 → 2nC2H5OH + Tính toán theo sơ đồ, bỏ qua hệ số n để thuận tiện tính toán Lời giải chi tiết: Quá trình: (C6H10O5)n → nC6H12O6 → 2nC2H5OH . %H = 81% Bỏ qua hệ số n trong quá trình tính toán để thuận tiện ntb = 20. 0,81: 162 = 0,1 (kmol) => nancol = 2ntb = 0,2 (kmol) ( theo lí thuyết) Vì H = 81% => nancol thực tế = 0,2. 0,81 = 0,162 (kmol) => mancol = 0,162.103.46 = 7452 (g) \({V_r} = \frac{{{m_r}}}{D} = \frac{{7452}}{{0,789}} \approx 9444,9(ml) = 9,445(l)\) Độ rượu = \(\frac{{{V_r}}}{{V{\,_{{\text{dd}}\,r}}}}.100\% = > \,{V_{dd\,r}} = \frac{{9,445.100\% }}{{{{96}^0}}} = 9,838(l)\) Đáp án A Câu hỏi 12 : Từ m gam tinh bột điều chế ancol etylic bằng phương pháp lên men với hiệu suất của cả quá trình là 85%. Lượng CO2 sinh ra từ quá trình trên được hấp thụ hoàn toàn vào dung dịch Ca(OH)2 thu được 40g kết tủa và dung dịch X. Thêm dung dịch NaOH 1M vào X , để lượng kết tủa thu được là lớn nhất thì cần tối thiểu 200 ml dung dịch NaOH 1M. Giá trị của m là :
Đáp án: C Phương pháp giải: phản ứng thủy phân xenlulozơ hoặc tinh bột (C6H10O5)n H1% H2% (C6H10O5)n -> nC6H12O6 -> 2nCO2 + 2nC2H5OH 162n 180n 88n 92n Lưu ý: 1) A -> B ( Hlà hiệu suất phản ứng)
nB = nA. H%
2) A -> B -> C ( H1, H2 là hiệu suất phản ứng A -> B và B -> C)
nC = nB. H2% = nA . H1%. H2% Lời giải chi tiết: X + NaOH có thêm kết tủa => X có HCO3- CO2 + Ca(OH)2 -> CaCO3 + H2O 0,4 2CO2 + Ca(OH)2 -> Ca(HCO3)2 Ca(HCO3)2 + NaOH -> CaCO3 + NaHCO3 + H2O Kết tủa max ó nNaOH = nCa(HCO3)2 = 0,2 mol => nCO2 bđ = 0,4 + 0,2 = 0,6 mol Quá trình : C6H10O5 -> C6H12O6 -> 2CO2 Mol x -> 2x.85% = 0,6 mol => x = 0,353 mol => m = 57,18g Đáp án C Câu hỏi 13 : Trong thực tế người ta thường nấu rượu ( ancol etylic) từ gạo ( chứa 81% tinh bột). Tinh bột chuyển hóa thành ancol etylic qua 2 giai đoạn: Tinh bột → glucozơ → ancol. Biết hiệu suất mỗi giai đoạn là 80%, khối lượng riêng của C2H5OH là 0,8 g/ml. Thể tích ancol etylic 460 thu được từ 10 kg gạo là
Đáp án: B Phương pháp giải: Viết sơ đồ phản ứng: \({({C_6}{H_{10}}{O_5})_n}\xrightarrow{{{H_1} = 80\% }}n{C_6}{H_{12}}{O_6}\xrightarrow{{{H_2} = 80\% }}2n{C_2}{H_5}OH\) Tính toán theo sơ đồ phản ứng chú ý đến hiệu suất phản ứng. Lời giải chi tiết: \({({C_6}{H_{10}}{O_5})_n}\xrightarrow{{{H_1} = 80\% }}n{C_6}{H_{12}}{O_6}\xrightarrow{{{H_2} = 80\% }}2n{C_2}{H_5}OH\) Để thuận tiện cho tính toán ta bỏ qua hệ số n mtb = 10.0,81 = 8,1 (kg) => ntb = 8,1 : 162 = 0,05 (Kmol) => nancol = 2ntb = 0,1 (Kmol) Vì quá trình sản xuất có hiệu suất => nancol thực tế thu được = nancol lí thuyết. %H = 0,1. (0,8. 0,8) = 0,064 (Kmol) = 64 (mol) => mancol thực tế = 64. 46 = 2900 (g) \(\begin{gathered}
Đáp án B Câu hỏi 14 : Từ 12 kg gạo nếp chưa 84% tinh bột người ta lên men và chưng cất ở điều kiện thích hợp thu được V lít côn 90o. Biết khối lượng riêng của C2H5OH là 0,8g/ml, hiệu suất của quá trình thủy phân và phản ứng lên men là 83% và 71%. Giá trị của V là
Đáp án: D Phương pháp giải: C6H10O5) → nC6H12O6 → 2nC2H5OH H quá trình =0,83.0,71=0,5893 mtinh bột =12.0,84=10,08kg →Theo lý thuyết mC2H5OH = 10,08 : 162 .2.46 = 5,7244 kg → thực tế mC2H5OH =3,373 kg → V Lời giải chi tiết:
(C6H10O5) → nC6H12O6 → 2nC2H5OH H quá trình =0,83.0,71=0,5893 mtinh bột =12.0,84=10,08kg →Theo lý thuyết mC2H5OH = 10,08 : 162 .2.46 = 5,7244 kg → thực tế mC2H5OH =5,7244.0,5893 = 3,373 kg → Vancol = 3373 :0,8 =4216,8 ml → Vcồn 90 độ = 4216,8 :0,9=4685 ml =4,685 lít Đáp án D Câu hỏi 15 : Lên men m gam tinh bột thành ancol etylic với hiệu suất 75%, hấp thụ toàn bộ khí CO2 sinh ra vào dung dịch chứa 0,03 mol Ba(OH)2, thu được kết tủa và dung dịch X. Cho từ từ dung dịch NaOH vào X, đến khi kết tủa lớn nhất thì cần ít nhất 6 ml dung dịch NaOH 1M. Giá trị của m là
Đáp án: D Phương pháp giải: (C6H10O5)n → nC6H12O6 → 2nC2H5OH +2nCO2 ( %H = 75%) \(C{O_2} + \underbrace {Ba{{(OH)}_2}}_{0,03\,mol}\xrightarrow{{}}\left\{ \begin{gathered} Vì lượng NaOH cần dùng ít nhất để thu được kết tủa lớn nhất => phản ứng xảy ra theo tỉ lệ mol NaOH : Ba(HCO3) = 1 : 1 Ba(HCO3)2 + NaOH → BaCO3↓ + NaHCO3 + H2O BTNT Ba => nBaCO3 (1) = nBa(OH)2 – nBa(HCO3) = ? (mol) BTNT C => nCO2 = nBaCO3(1) + 2nBa(HCO3) = ? (mol) Từ sơ đồ => ntb = ½ nCO2 = ? (mol) Vì H = 75% => mtb thực tế cần lấy = mtb lí thuyết : 0,75 = ? (g) Lời giải chi tiết: (C6H10O5)n → nC6H12O6 → 2nC2H5OH +2nCO2 ( %H = 75%) \(C{O_2} + \underbrace {Ba{{(OH)}_2}}_{0,03\,mol}\xrightarrow{{}}\left\{ \begin{gathered} Vì lượng NaOH cần dùng ít nhất để thu được kết tủa lớn nhất => phản ứng xảy ra theo tỉ lệ mol NaOH : Ba(HCO3) = 1 : 1 Ba(HCO3)2 + NaOH → BaCO3↓ + NaHCO3 + H2O 0,006 (mol)←0,006 (mol) BTNT Ba => nBaCO3 (1) = nBa(OH)2 – nBa(HCO3) = 0,03 – 0,006=0,024 (mol) BTNT C => nCO2 = nBaCO3(1) + 2nBa(HCO3) = 0,024 + 2.0,006 = 0,036 (mol) Từ sơ đồ => ntb = ½ nCO2 = 0,018 (mol) => mtb lí thuyết = 0,018.162=2,916 (g) Vì H = 75% => mtb thực tế cần lấy = mtb lí thuyết : 0,75 = 3,888(g) Đáp án D Câu hỏi 16 : Lên men m gam tinh bột thành ancol etylic với hiệu suất của cả quá trình là 75%. Lượng CO2 sinh ra hấp thụ hoàn toàn vào dung dịch Ca(OH)2, thu được 60 gam kết tủa và dung dịch X. Thêm dung dịch NaOH 1,2M vào X, thu được kết tủa. Để lượng kết tủa thu được là lớn nhất thì cần tối thiểu 100 ml dung dịch NaOH. Giá trị của m là
Đáp án: B Phương pháp giải: Dd X chứa Ca(HCO3)2 + NaOH => Để lượng kết tủa thu được lớn nhất, cần ít nhất 0,12 mol NaOH vậy phản ứng NaOH + Ca(HCO3)2 xảy ra theo tỉ lệ mol 1:1 Bảo toàn nguyên tố C Chú ý đến hiệu suất phản ứng Lời giải chi tiết: \(\frac{1}{2}({C_6}{H_{10}}{O_5})n\xrightarrow{{\% H = 75\% }}\left\{ \begin{gathered} Để lượng kết tủa thu được lớn nhất, cần ít nhất 0,12 mol NaOH vậy phản ứng NaOH + Ca(HCO3)2 xảy ra theo tỉ lệ mol 1:1 NaOH + Ca(HCO3)2 → CaCO3↓ + NaHCO3 + H2O 0,12 → 0,12 (mol) BTNT: C => nCO2 = nCaCO3 + 2nCa(HCO3)2 = 0,6 + 2. 0,12 = 0,84 (mol) ntb = ½ nCO2 = 0,84/2 = 0,42 (mol) => mtb lí thuyết = 0,42. 162 = 68,04 (g) Vì H =75% => mtb thực tế cần lấy là: 68,04 :%H = 68,04 : 0,75 = 90,72 (g) Đáp án B Câu hỏi 17 : Lấy m kg gạo (chứa 75% tinh bột) lên men thành ancol etylic. Cho toàn bộ lượng CO2 sinh ra hấp thụ hết vào dung dịch Ca(OH)2, thu được 600 gam kết tủa đồng thời khối lượng dung dịch sau phản ứng giảm 138 gam so với khối lượng dung dịch nước vôi trong ban đầu. Nếu hiệu suất quá trình lên men đạt 80% thì giá trị của m gần với giá trị nào sau đây nhất là
Đáp án: C Phương pháp giải: \({\text{ }}{({C_6}{H_{10}}{O_5})_n}\xrightarrow{{ + {H_2}O,xt{\text{ }}{{\text{H}}^ + }}}n{C_6}{H_{12}}{O_6}\xrightarrow[{}]{{{\text{ men}}}}2nC{O_2}\) Để đơn giản, chọn n = 1. Cho CO2 hấp thụ hết vào dung dịch Ca(OH)2. Đề bài cho biết CO2 được hấp thụ hết vào dung dịch nước vôi trong, cho biết khối lượng kết tủa tạo thành (chú ý có thể tạo 2 muối) và độ tăng giảm khối lượng dung dịch lúc trước và sau. Do đó, ta sẽ áp dụng định luật bảo toàn khối lượng để tìm khối lượng CO2. mCO2 + mdung dịch Ca(OH)2 banđầu = mdung dịch sau + mkết tủa → mdung dịch Ca(OH)2 banđầu - mdung dịch sau = mkết tủa - mCO2 → số mol CO2 → số mol/ khối lượng tinh bột (chú ý hiệu suất) → khối lượng khoai cần lấy. Lời giải chi tiết: + Cho toàn bộ CO2 thu được sau quá trình lên men hấp thụ hết vào dung dịch nước vôi trong: Áp dụng định luật bảo toàn khối lượng: mCO2 + mdung dịch Ca(OH)2 banđầu = mdung dịch sau + mkết tủa → mdung dịch Ca(OH)2 banđầu - mdung dịch sau = mkết tủa - mCO2 → 138 = 600 - mCO2 → mCO2 = 462 gam → nCO2 = 10,5 mol. + Xét quá trình: C6H10O5 \(\overset{+H_2O,\,xt\,H^+}{\rightarrow}\) C6H12O6 \(\rightarrow\) 2CO2 nC6H10O5 = nCO2/2 = 10,5/2 = 5,25 (mol) \(\begin{array}{l}H = 80\% \Rightarrow {m_{tinh\,bot\,(thuc\,te\,can\,dung)}} = \frac{{100}}{{80}}.5,25.162 = 1063,125\,gam\\ \Rightarrow m = \frac{{100}}{{75}}.1063,125 = 1417,5\,gam.\end{array}\) Đáp án C Câu hỏi 18 : Từ m gam tinh bột điều chế ancol etylic bằng phương pháp lên men với hiệu suất của cả quá trình là 72%. Lượng CO2 sinh ra từ quá trình trên được hấp thụ hoàn toàn vào dung dịch Ba(OH)2 thu được 118,2 gam kết tủa và dung dịch X. Thêm dung dịch NaOH 1M vào X, để lượng kết tủa thu được là lớn nhất thì cần tối thiểu 100 ml dung dịch NaOH 1M. Giá trị của m là
Đáp án: D Phương pháp giải: \({\text{ }}{({C_6}{H_{10}}{O_5})_n}\xrightarrow{{ + {H_2}O,xt{\text{ }}{{\text{H}}^ + }}}n{C_6}{H_{12}}{O_6}\xrightarrow[{}]{{{\text{ men}}}}2nC{O_2}\) Để đơn giản, chọn n = 1. Thêm NaOH vào dung dịch X thấy có kết tủa xuất hiện → phản ứng giữa CO2 và Ba(OH)2 tạo ra 2 muối: BaCO3 0,6 mol; Ba(HCO3)2 0,1 mol. Bảo toàn C → nCO2 → số mol tinh bột (chú ý hiệu suất phản ứng) Lời giải chi tiết: Khi thêm NaOH vào dung dịch X có xuất hiện kết tủa, do đó CO2 phản ứng với Ba(OH)2 tạo ra 2 muối. \(C{O_2}\) \(\overset{+Ba(OH)_2}{\rightarrow}\) \(\left\{ \begin{array}{l}BaC{O_3} \downarrow {\rm{ 0,6 mol}}\\{\rm{Ba(HC}}{{\rm{O}}_3}{)_2}{\rm{ x mol}}\end{array} \right\}(1)\) Để thu được lượng kết tủa lớn nhất thì cần ít nhất 0,1 mol NaOH → x = 0,1 (vì nếu chỉ dùng 0,1 mol NaOH thì lượng CO32- tạo ra tối đa là 0,1 mol). Bảo toàn nguyên tố C cho quá trình (1), ta được: \({n_{C{O_2}}} = {n_{BaC{O_3}}} + 2{n_{Ba{{(HC{O_3})}_2}}} = 0,6 + 2x = 0,6 + 2,0,1 = 0,8{\rm{ mol}}\) C6H10O5 \(\overset{+H_2O,\,xt\,H^+}{\rightarrow}\) C6H12O6 \(\rightarrow \) 2CO2 => nC6H10O5 = nCO2/2 = 0,8/2 = 0,4 mol \(H = 72\% \Rightarrow {m_{tinh\,bot\,(thuc\,te\,can\,dung)}} = \frac{{100}}{{72}}.0,4.162 = 90\,gam\) Đáp án D Câu hỏi 19 : Từ 10 kg ngô (chứa 65% tinh bột) lên men thu được V lít ancol etylic 350. Biết khối lượng riêng của C2H5OH là 0,8g/ml, hiệu suất quá trình thủy phân và phản ứng lên men lần lượt là 80% và 72%. Giá trị của V là
Đáp án: D Phương pháp giải: Rượu 35o: 100 ml rượu 35o chứa 35 ml rượu etylic nguyên chất. \({V_{ruou\,{{35}^o}}} = \frac{{100}}{{35}}.{V_{{C_2}{H_5}OH}} = \frac{{100}}{{35}}.\frac{{{m_{{C_2}{H_5}OH}}}}{D} = \frac{{100}}{{35}}.\frac{{46.{n_{{C_2}{H_5}OH}}}}{{0,8}}\,(1)\) (C6H10O5)n \(\overset{+H_2O,\,xt\,H^+}{\rightarrow}\) nC6H12O6 \(\overset{men\,ruou}{\rightarrow}\) 2nC2H5OH Để đơn giản, chọn n=1. Tính số mol tinh bột → số mol C2H5OH (chú ý hiệu suất phản ứng) → thay vào (1) để tìm V. Lời giải chi tiết: \({m_{tinh\,bot}} = \frac{{65}}{{100}}.10\, = 6,5\,kg \Rightarrow {n_{tinh\,bot}} = \frac{{13}}{{324}}\,kmol.\) (C6H10O5)n \(\xrightarrow[H=80\%]{+H_2O,\,xt\,H^+}\) nC6H12O6 \(\xrightarrow[H=72\%]{men\,ruou}\) 2nC2H5OH => nC2H5OH = 2.nC6H10O5 = 2.(13/324) = 13/162 (kmol) \(\begin{array}{l}H = {H_1}.{H_2} = 57,6\% \Rightarrow {m_{{C_2}{H_5}OH}} = \frac{{57,6}}{{100}}.\frac{{13}}{{162}}.46 = 2,1262\,kg.\\{V_{ruou\,{{35}^o}}} = \frac{{100}}{{35}}.{V_{{C_2}{H_5}OH}} = \frac{{100}}{{35}}.\frac{{{m_{{C_2}{H_5}OH}}}}{D} = \frac{{100}}{{35}}.\frac{{2,1262}}{{0,8}} = 7,594lit.\end{array}\) Đáp án D Câu hỏi 20 : Cho m gam tinh bột lên men thành ancol etylic với hiệu suất toàn bộ quá trình là 75%. Toàn bộ lượng CO2 sinh ra được hấp thụ hoàn toàn vào dung dịch Ba(OH)2, thu được 788 gam kết tủa và dung dịch X. Đun kĩ dung dịch X thu thêm được 197 gam kết tủa. Giá trị của m là
Đáp án: C Phương pháp giải: \({({C_6}{H_{10}}{O_5})_n}\xrightarrow{{ + {H_2}O,xt{\text{ }}{{\text{H}}^ + }}}n{C_6}{H_{12}}{O_6}\xrightarrow[{}]{{{\text{ men}}}}2nC{O_2}\) Để đơn giản, chọn n = 1. Khi đun nóng dung dịch X thấy có kết tủa xuất hiện → phản ứng giữa CO2 và Ba(OH)2 tạo ra 2 muối. → tính được nCO2 → số mol tinh bột (chú ý hiệu suất phản ứng) Lời giải chi tiết: + Khi đun nóng dung dịch X thấy có kết tủa xuất hiện → phản ứng giữa CO2 và Ba(OH)2 tạo ra 2 muối.
Bảo toàn nguyên tố C: nCO2 = nBaCO3 + 2nBa(HCO3)2 = 4 + 2.1 = 6 mol. + Xét quá trình lên men tinh bột:
Đáp án C Câu hỏi 21 : Ancol etylic được điều chế bằng cách lên men tinh bột theo sơ đồ: (C6H10O5)n\(\xrightarrow{xt}\)C6H12O6\(\xrightarrow{xt}\)C2H5OH Để điều chế 10 lít rượu etylic 46o cần m kg gạo (chứa 75% tinh bột, còn lại là tạp chất trơ). Biết hiệu suất của cả quá trình là 80% và khối lượng riêng của ancol etylic nguyên chất là 0,8g/ml. Giá trị của m là
Đáp án: D Phương pháp giải:
Lời giải chi tiết: m = 10.(46/100).0,8:46:2.162.(100/80).(100/75) = 10,8 gam Đáp án D Câu hỏi 22 : Trong một nhà máy rượu, người ta dùng nguyên liệu là mùn cưa chứa 50% xenlulozo để sản xuất ancol etylic với hiệu suất 70%. Để sản xuất 1 tấn ancol etylic nguyên chất thì khối lượng mùn cưa cần dùng là
Đáp án: B Phương pháp giải: C6H10O5 → C6H12O6 → 2C2H5OH + 2CO2 Lời giải chi tiết: m mùn cưa = (1000 : 46) : 2 . 162 . (100/70) . (100/50) = 5031 kg Đáp án B Câu hỏi 23 : Ancol etylic được điều chế từ tinh bột bằng phương pháp lên men với hiệu suất toàn bộ quá trình là 90%, Hấp thụ toàn bộ lượng CO2, sinh ra khi lên men m gam tinh bột vào nước vôi trong, thu được 330 gam kết tủa và dung dịch X. Biết khối lượng X giảm đi so với khối lượng nước vôi trong ban đầu là 132 gam. Giá trị của m là:
Đáp án: B Phương pháp giải: C6H10O5 → C6H12O6 → 2C2H5OH + 2CO2 m dd giảm = mCaCO3 – mCO2 => mCO2 = mCaCO3 – mdd giảm = ? => m = ? Lời giải chi tiết: C6H10O5 → C6H12O6 → 2C2H5OH + 2CO2 m dd giảm = mCaCO3 – mCO2 => mCO2 = mCaCO3 – mdd giảm = 330 – 132 = 198 gam => nCO2 = 198 : 44 = 4,5 mol => m = 4,5:2.162.100/90 = 405 gam Đáp án B Câu hỏi 24 : Ancol etylic được điều chế từ tinh bột bằng phương pháp lên men với hiệu suất toàn bộ quá trình là 90%. Hấp thụ toàn bộ lượng CO2 sinh ra khi lên men m gam tinh bột vào nước vôi trong thu được 330 gam kết tủa và dung dịch X. Biết khối lượng X giảm đi so với khối lượng nước vôi trong ban đầu là 132 gam. Giá trị của m là:
Đáp án: B Phương pháp giải: *Hấp thụ CO2 vào Ca(OH)2: m dd giảm = mCaCO3 – mCO2 => mCO2 = mCaCO3 – mdd giảm = ? *Phản ứng lên men: C6H10O5 → 2CO2 nC6H10O5 = 0,5nCO2 = ? => m tinh bột = ? Chú ý hiệu suất. Lời giải chi tiết: *Hấp thụ CO2 vào Ca(OH)2: m dd giảm = mCaCO3 – mCO2 => mCO2 = mCaCO3 – mdd giảm = 330 – 132 = 198 gam => nCO2 = 198 : 44 = 4,5 mol *Phản ứng lên men: C6H10O5 → 2CO2 nC6H10O5 = 0,5nCO2 = 0,5.4,5 = 2,25 mol => m tinh bột = 2,25.162 = 364,5 gam Do hiệu suất thực tế là 90% nên lượng tinh bột đã dùng là: 364,5.(100/90) = 405 gam Đáp án B Câu hỏi 25 : Lên men m gam tinh bột thành ancol etylic với hiệu suất của cả quá trình là 75%. Lượng CO2 sinh ra được hấp thụ hoàn toàn vào dung dịch Ca(OH)2 thu được 50 g kết tủa và dung dịch X. Thêm NaOH 1M vào X, thu được kết tủa. Để lượng kết tủa thu được là lớn nhất cần tối thiểu 100 ml dung dịch NaOH. Gía trị của m là
Đáp án: D Phương pháp giải: \({({C_6}H{}_{10}{O_5})_n} \to 2n{C_2}{H_6}O + 2nC{O_2}\) Vì dung dịch thu được vừa tạo kết tủa vừa phản ứng với NaOH tạo kết tủa nên xảy ra 2 phản ứng CO2 + Ca(OH)2 → CaCO3 + H2O 2CO2 + Ca(OH)2 → Ca(HCO3)2 Ca(HCO3)2 + 2NaOH → CaCO3 + Na2CO3 + H2O Lời giải chi tiết: \({({C_6}H{}_{10}{O_5})_n} \to 2n{C_2}{H_6}O + 2nC{O_2}\) CO2 + Ca(OH)2 → CaCO3 + H2O 2CO2 + Ca(OH)2 → Ca(HCO3)2 Ca(HCO3)2 + 2NaOH → CaCO3 + Na2CO3 + H2O nCO2 = nCaCO3 + nNaOH = 0,5 + 0,1 = 0,6 mol → mtinh bôt (lt) = 0,3 .162 = 48,6 g → mtinh bột (tt)= mtinh bột (lt) : H% . 100% = 64,8 g Đáp án D Câu hỏi 26 : Khi lên men m kg ngô chứa 65% tinh bột với hiệu suất toàn quá trình là 80% thì thu được 5 lít rượu etylic 200 và V m3 khí CO2 (đktc). Cho khối lượng riêng của C2H5OH nguyên chất là 0,8 g/ml. Giá trị của m và V lần lượt là:
Đáp án: D Phương pháp giải: Bài toán hiệu suất (tính theo chất phản ứng): nTT = nLT . (100/H) Lời giải chi tiết: Vancol = Vrượu.ĐR = 5.20% = 1 lít = 1000 ml => mancol = 1000.0,8 = 800 gam => nC2H5OH = 17,39 mol C6H10O5 + H2O → 2C2H5OH + 2CO2 => nCO2 = nC2H5OH = 17,39 mol => VCO2 = 17,39.22,4 = 389,6 lít = 0,39 m3 ntinh bột LT = nC2H5OH : 2 = 8,7 mol => nTT = nLT . (100/H) = 10,7 mol => mngô = 162.10,7.(100/65) = 2709 gam = 2,7 kg Đáp án D Câu hỏi 27 : Khối lượng của tinh bột cần dùng trong quá trình lên men để tạo thành 5 lít rượu (ancol etylic) 46o là (biết hiệu suất của cả quá trình là 72% và khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml)
Đáp án: D Phương pháp giải: V rượu nguyên chất = V dd rượu.(ĐR/100) => mC2H5OH = D.V => nC2H5OH Để đơn giản ta coi tinh bột là C6H10O5: C6H10O5 → C6H12O6 → 2C2H5OH => n tinh bột = 0,5.nC2H5OH => m tinh bột (tính toán) Tuy nhiên hiệu suất cả quá trình là 72% nên lượng tinh bột thực tế cần dùng phải lớn hơn lượng tính toán: => m tinh bột cần dùng = m tinh bột (tính toán).(100/H) Lời giải chi tiết: V rượu nguyên chất = V dd rượu.(ĐR/100) = 5.(46/100) = 2,3 lít => mC2H5OH = D.V = 0,8.2,3 = 1,84 kg => nC2H5OH = 1,84/46 = 0,04 kmol Để đơn giản ta coi tinh bột là C6H10O5: C6H10O5 → C6H12O6 → 2C2H5OH => n tinh bột = 0,5.nC2H5OH = 0,02 kmol => m tinh bột = 0,02.162 = 3,24 kg Tuy nhiên hiệu suất cả quá trình là 72% nên lượng tinh bột thực tế cần dùng phải lớn hơn lượng tính toán: => m tinh bột cần dùng = 3,24.(100/72) = 4,5 kg Đáp án D Câu hỏi 28 : Lên mem m gam tinh bột thành ancol etylic với hiệu suất của cả quá trình là 80%. Lượng CO2 sinh ra được hấp thụ hoàn toàn vào dung dịch nước vôi trong, thu được 20 g kết tủa và dung dịch X. Cho dung dịch NaOH dư vào dung dịch X thấy thu thêm được 10 g kết tủa nữa. Giá trị của m là
Đáp án: A Phương pháp giải: Tinh bột → Glucozo C6H12O6 → 2C2H5OH + 2CO2 CO2 + Ca(OH)2 → BaCO3 + H2O 2CO2 + Ca(OH)2 → Ca(HCO3)2 Ca(HCO3)2 + 2NaOH → CaCO3 + Na2CO3 + 2H2O nBaCO3 = 0,2 mol và nBa(HCO3)2 = n↓ lần 2 = 0,1 mol → nCO2 = 0,2+ 2.0,1 = 0,4 mol Lời giải chi tiết: Tinh bột → Glucozo C6H12O6 → 2C2H5OH + 2CO2 CO2 + Ca(OH)2 → BaCO3 + H2O 2CO2 + Ca(OH)2 → Ca(HCO3)2 Ca(HCO3)2 + 2NaOH → CaCO3 + Na2CO3 + 2H2O nBaCO3 = 0,2 mol và nBa(HCO3)2 = n↓ lần 2 = 0,1 mol → nCO2 = 0,2+ 2.0,1 = 0,4 mol → thực tế thì : ntinh bôt = 0,2 : 0,8 = 0,25 mol → m = 40,5 g Chọn A Câu hỏi 29 : Cho m gam tinh bột lên men thành ancol etylic (rượu) với hiệu suất 81%. Toàn bộ lượng CO2 sinh ra được hấp thu hoàn toàn vào dung dịch Ca(OH)2 thu được 550 g kết tủa và dung dịch X. Đun kỹ dung dịch X thì thu được thêm 100 g kết tủa . Giá trị của m là:
Đáp án: B Phương pháp giải: Bài toán hiệu suất: nThực tế = nLT.H% Lời giải chi tiết: Vì khi đun sôi dung dịch tạo thêm kết tủa chứng tỏ trong dung dịch có Ca(HCO3)2 Ca(OH)2 + CO2 → CaCO3 + H2O Mol 5,5 \(\leftarrow \) 550/100 Ca(HCO3)2 \(\overset{t^{0}}{\rightarrow}\) CaCO3 + CO2 + H2O Mol 1 \(\leftarrow \) 100/100 Bảo toàn nguyên tố C: nCO2 = nCaCO3 bđ + 2nCa(HCO3)2 = 5,5 + 2.1 = 7,5 mol - Xét phản ứng lên men: C6H10O5 + H2O \(\overset{Len.men}{\rightarrow}\)2CO2 + 2C2H5OH Mol 3,75 \(\leftarrow \) 7,5 nLT.H% = nThực => nLT.81% = 3,75 => nLT = 4,63 mol => m = 4,63.162 = 750g Đáp án B Câu hỏi 30 : Khối lượng của tinh bột cần dùng trong quá trình lên men để tạo thành 5 lít rượu (ancol) etylic 460 là bao nhiêu (biết hiệu suất của cả quá trình là 72% và khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml)
Đáp án: D Phương pháp giải: Đổi VC2H5OH = VddC2H5OH.độ rượu :100 = ? (lít) → đổi ra đơn vị (ml) Đổi mC2H5OH = VC2H5OH.d = ? (gam) → nC2H5OH = ? (mol) Tính khối lượng tinh bột lí thuyết cần lấy theo sơ đồ sau: (C6H10O5)n → nC6H12O6 → 2nC2H5OH + 2nCO2 Vì %H = 72% nên mC6H10O5 thực tế = mC6H10O5 lí thuyết.100% :%H = ? Lời giải chi tiết: \(\eqalign{ Sơ đồ: (C6H10O5)n → nC6H12O6 → 2nC2H5OH + 2nCO2 20 ← 40 (mol) Theo PTHH: nC6H10O5 = 1/2nC2H5OH = 20 (mol) → mC6H10O5 lí thuyết = 20.162 = 3240 (g) Vì %H = 72% nên mC6H10O5 thực tế = mC6H10O5 lí thuyết.100% :%H = 3240.100%: 72% = 4500 (g) = 4,5 (kg) Đáp án D
|