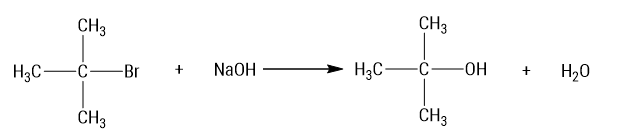
Khi đun nóng ester của acetic acid trong dung dịch NaOH xảy ra phản ứng hóa học sau:
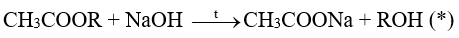
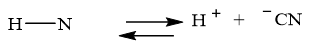
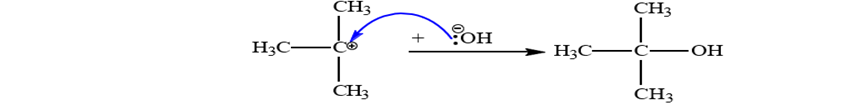
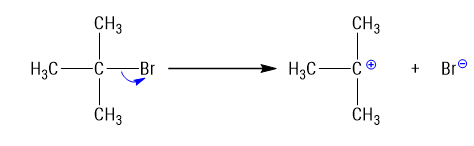
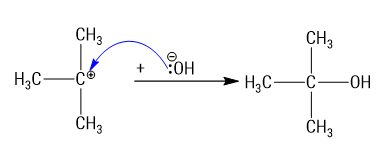
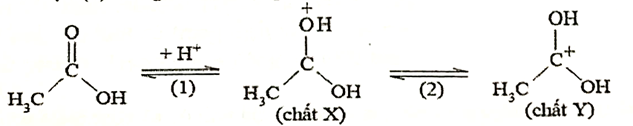
Cơ chế của phản ứng xảy ra như sau:
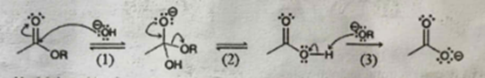
Nhận định nào sau đây không đúng?
-
A.
Giai đoạn (3) là phản ứng acid – base theo bronsted – Lowry.
-
B.
Giai đoạn (2) có sự thay thế nhóm OH bằng nhóm OR.
-
C.
Giai đoạn (1) có sự phá vỡ liên kết hình thành liên kết \(\sigma \).
-
D.
Phản ứng (*) là phản ứng thủy phân ester trong môi trường kiềm.
Dựa vào cơ chế phản ứng thế nucleophile.
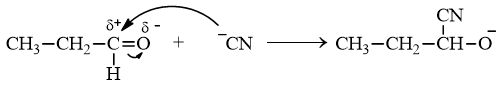
Cơ chế giai đoạn 1: Dưới tác động của tác nhân nucleophile (-OH) tấn công vào liên kết pi (C=O) để chuyển thành liên kết xích ma, - OH liên kết với carbocation → C đúng.
Cơ chế giai đoạn 2: O- đẩy electron vào vị trí carbon đang liên kết, làm phân tách liên kết giữa C – OR → B sai, vì giai đoạn (2) là sự phân tách – OH.
Cơ chế giai đoạn 3: ion – OR tấn công vào liên kết O – H, O hút electron đẩy H+ ra khỏi liên kết tạo thành ion O- → A đúng
Phản ứng (*) là phản ứng thủy phân ester trong môi trường kiềm
Chọn B.
Đáp án : B













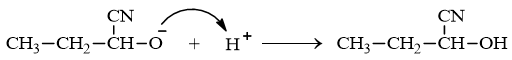
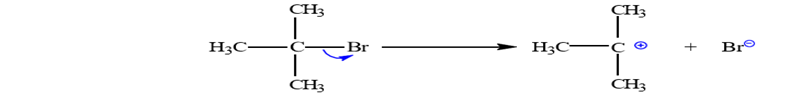
Danh sách bình luận