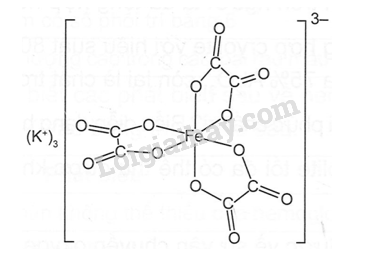
Hoà tan 1,61 g FeCl3 vào 10 mL nước thu được dung dịch (I). Hoà tan 5,52g K2C2O4 vào 30 mL nước thu được dung dịch (II). Cho từ từ dung dịch (II) vào dung dịch (I) và khuấy liên tục. Sau một thời gian thêm ethanol vào dung dịch phản ứng thì xuất hiện tinh thể. Lọc, thu tinh thể sạch của phức chất có công thức là K3[FeC2O4]3H2O với khối lượng là 3,51g. Phương trình hoá học của phản ứng diễn ra là:
FeCl3+3K2C2O4 + 3H2O→ K3[Fe(C2O4)3]3H2O + 3KCI Hiệu suất của phản ứng hình thành phức chất trên là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Đáp án:
Đáp án:
Từ kết quả so sánh số mol FeCl3 và số mol của K2Cr2O7 chọn tính toán lí thuyết theo số
mol FeCl3. Số mol phức chất thu được theo lí thuyết bằng số mol FeCl3 và là:
1,61 : 162,5 = 9,9 . 10-3 (mol).
Khối lượng phức chất thu được theo lí thuyết là:
491 . 9,9. 10-3 = 4,86 (g).
Hiệu suất phản ứng là:
(3,51 : 4,86) . 100% = 72,2%.














Danh sách bình luận