Nội dung từ Loigiaihay.Com
Một bình phản ứng có dung tích không đổi, chứa hỗn hợp khí N2 và H2 với nồng độ tương ứng là 0,3M và 0,7M. Sau khi phản ứng tổng hợp NH3 đạt trạng thái cân bằng ở toC, H2 chiếm 50% thể tích hỗn hợp thu được. Hằng số cân bằng KC ở toC của phản ứng có giá trị là:
-
A.
2,500.
-
B.
3,125.
-
C.
0,609.
-
D.
0,500.
Dựa vào kiến thức về hằng số cân bằng.
aA + bB → cC + dD
Ở trạng thái cân bằng, hằng số cân bằng KC của phản ứng được xác định theo biểu thức:
\({K_C} = \frac{{{{{\rm{(}}C{\rm{)}}}^{\rm{c}}}{{{\rm{(}}D{\rm{)}}}^d}}}{{{{{\rm{(}}A)}^a}{{(B{\rm{)}}}^b}}}\)
Ta có: \({N_{2(k)}} + 3{H_{2(k)}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2N{H_{3(k)}}\)(1)
Gọi (N2) phản ứng là a => theo phản ứng (1): (H2) phản ứng là 3a; (NH3) phản ứng là 2a.
Ở trạng thái cân bằng: (N2) = 0,3-a; (H2) = 0,7-a
Để đơn giản ta xét 1 lít hỗn hợp.
Sau khi phản ứng cân bằng: 0,3 – a + 0,7 – 3a + 2a= 1 – 2a
Mặt khác % thể tích H2 = 50% = \(\frac{{0,7 - 3a}}{{1 - 2a}}\).100 => a = 0,1.
Khi đạt cân bằng (N2) = 0,3 – 0,1 = 0,2 (M)
(H2) = 0,7 – 0,3 = 0,4 (M)
(NH3) = 0,2 (M).
Vậy \({K_C} = \frac{{{{{\rm{(0,2)}}}^2}}}{{{\rm{(0,2}}){{{\rm{(}}0,4)}^3}}} = \)= 3,125
Đáp án : B

Các bài tập cùng chuyên đề
Cho cân bằng: \(2S{O_{2(k)}} + {O_{2(k)}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2S{O_{3(k)}}\)
Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu đúng khi nói về cân bằng này
Cho cân bằng hóa học:
\({N_{2(k)}} + 3{H_{2(k)}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2N{H_{3(k)}}\)
Phản ứng thuận là phản ứng tỏa nhiệt. Cân bằng hóa học không bị chuyển dịch khi:
Cho cân bằng hóa học sau: \(2S{O_{2(k)}} + {O_{2(k)}} \to 2S{O_{3(k)}}\); ∆H<0
Yếu tố nào sau đây làm cân bằng chuyển dịch theo chiều thuận
(1) tăng nhiệt độ
(2) hạ nhiệt độ
(3) tăng áp suất
(4) giảm nồng độ SO2
(5) tăng nồng độ SO2
(6) thêm chất xúc tác
Cho cân bằng hóa học: \({H_{2(k)}} + {I_{2(k)}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2H{I_{(k)}}\)∆H>0.
Cân bằng không bị chuyển dịch khi:
Cho cân bằng sau trong bình kín:
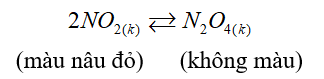
Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có:
Cho phản ứng hóa học sau:
\({H_{2(k)}} + {I_{2(k)}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2H{I_{(k)}}\)
Nồng độ các chất lúc cân bằng ở nhiệt độ 430℃ như sau:
(H2) = (I2) = 0,107M; (HI)=0,768M
Tính hằng số cân bằng KC của phản ứng ở 430℃.
Một bình phản ứng có dung tích không đổi, chứa hỗn hợp khí N2 và H2 với nồng độ tương ứng là 0,3M và 0,7M. Sau khi phản ứng tổng hợp NH3 đạt trạng thái cân bằng ở toC, H2 chiếm 50% thể tích hỗn hợp thu được. Hằng số cân bằng KC ở toC của phản ứng có giá trị là:
Cho cân bằng hóa học sau: \(2S{O_{2(k)}} + {O_{2(k)}} \to 2S{O_{3(k)}}\); ∆H<0
Các yếu tố nào sau đây làm cân bằng chuyển dịch theo chiều thuận:
(1) Tăng nhiệt độ
(2) Hạ nhiệt độ
(3) Tăng áp suất
(4) Thêm xúc tác
(5) Tăng nồng độ SO2
(6) Tăng nồng độ SO3
Cho cân bằng: \(2S{O_{2(k)}} + {O_{2(k)}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2S{O_{3(k)}}\)
Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu đúng khi nói về cân bằng này
Cho cân bằng hóa học:
\({N_{2(k)}} + 3{H_{2(k)}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2N{H_{3(k)}}\)
Phản ứng thuận là phản ứng tỏa nhiệt. Cân bằng hóa học không bị chuyển dịch khi:
Cho cân bằng hóa học: \({N_{2(k)}} + 3{H_{2(k)}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2N{H_{3(k)}}\)
Cân bằng trên chuyển dịch theo chiều thuận khi:
Người ta cho N2 và H2 vào trong bình kín dung tích không đổi và thực hiện phản ứng:
\({N_2}(g) + 3{H_2} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2N{H_3}\)
Sau một thời gian, nồng độ các chất trong bình như sau: [N2] = 2M; [H2] = 3M; [NH3] = 2M. Nồng độ mol/l của N2 và H2 ban đầu lần lượt là:
Cho biết mối quan hệ giữa các giá trị KC của các phản ứng sau:
(1) \(2S{O_2}(g) + {O_2}(g) \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2S{O_3}(g)\)
(2) \(S{O_2}(g) + \frac{1}{2}{O_2}(g) \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} S{O_3}(g)\)
(3) \(2S{O_3}(g) \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2S{O_2}(g) + {O_2}(g)\)












