Bài 4 trang 79 SGK Hóa học 8Có phương trình hóa học sau: Đề bài Có phương trình hóa học sau : a) Tính khối lượng canxi clorua thu được khi cho 10 g canxi cacbonat tác dụng với axit clohiđric dư. b) Tính thể tích khí cacbonic thu được trong phòng khi làm thí nghiệm, nếu có 5 g canxi cacbonat tác dụng hết với axit. Biết 1 mol khí ở điều kiện phòng có thể tích là 24 lít. Video hướng dẫn giải Phương pháp giải - Xem chi tiết Viết PTHH và tính toán theo PTHH. Lời giải chi tiết Phương trình hóa học: CaCO3 + 2HCl → CaCl2 + CO2 + H2O 1 mol 1 mol 1 mol a) Số mol canxi cacbonat tham gia phản ứng là: \(n_{CaCO_{3}}\) = \(\dfrac{10}{100}\) = 0,1 mol Theo phương trình hóa học, ta có: \(n_{CaCl_{2}}\) = \(n_{CaCO_{3}}\) = 0,1 mol Khối lượng của canxi clorua thu được là: \(m_{CaCl_{2}}\) = 0,1 . (40 + 71) = 11,1 g b) Số mol canxi cacbonat tham gia phản ứng là: \(n_{CaCO_{3}}\) = \(\dfrac{5}{100}\) = 0,05 mol Theo phương trình hóa học, ta có: \(n_{CO_{2}}\) = \(n_{CaCO_{3}}\) = 0,05 mol Thể tích khí CO2 thu được ở điều kiện phòng là: \(V_{CO_{2}}\) = 24 . 0,05 = 1,2 lít HocTot.Nam.Name.Vn
|













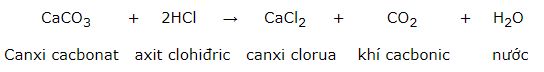

Danh sách bình luận